Clear Sky Science · nl
Multimodale antigenontsnapping aan GPRC5D‑gerichte T‑cel engageren bij multipl myeloom
Als kanker precieze immunotherapie te slim af is
Krachtige nieuwe immuun-gebaseerde middelen veranderen de behandeling van multipel myeloom, een bloedkanker die voor de meeste patiënten nog steeds niet te genezen is. Deze therapieën laten de eigen T‑cellen van het lichaam gericht tumorcellen opsporen en vernietigen aan de hand van specifieke “vlaggen” op hun oppervlak. Een veelbelovende vlag is het molecuul GPRC5D. Zoals bij veel gerichte behandelingen kunnen tumoren echter evolueren en ontsnappen aan de therapie. Deze studie legt, in ongekende detail, bloot hoe myeloomcellen de GPRC5D‑vlag veranderen of verbergen om te ontkomen aan zeer effectieve T‑cel‑engagerende geneesmiddelen.
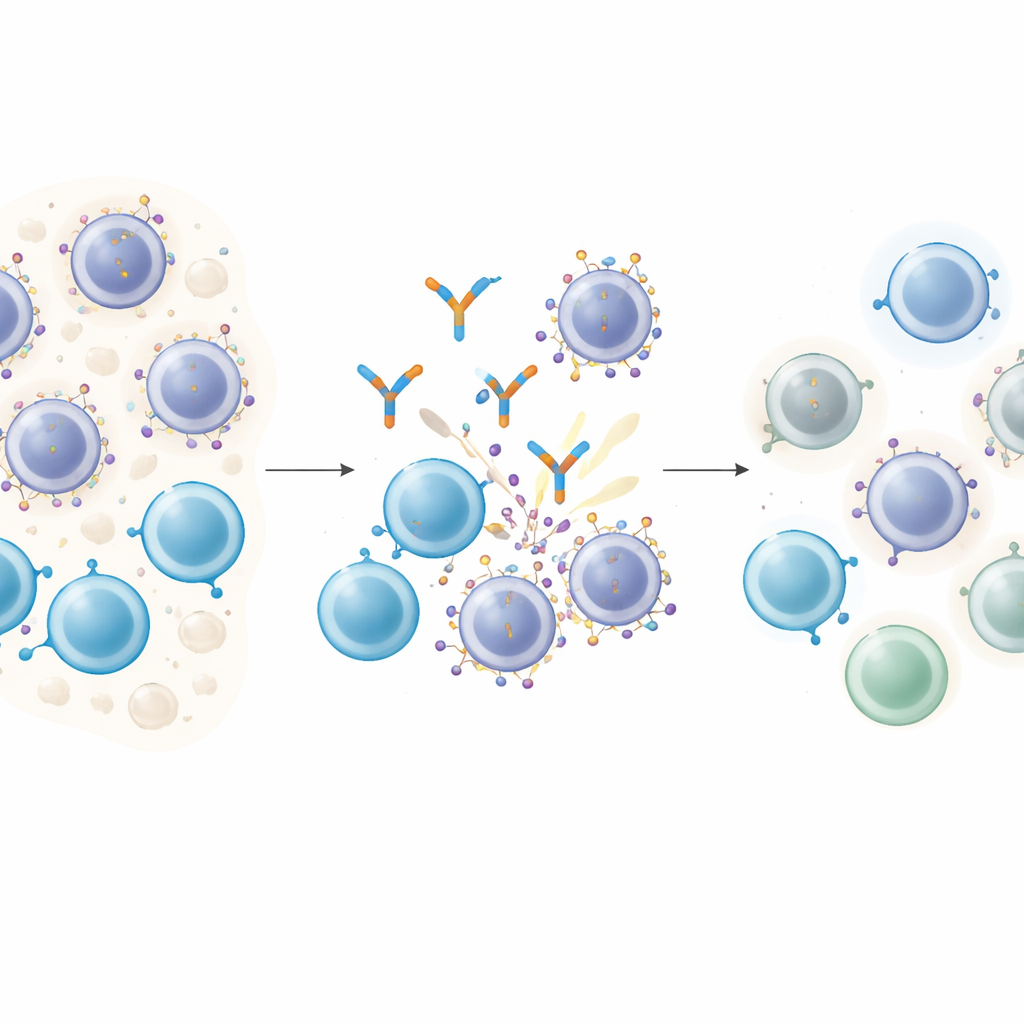
Hoe slimme medicijnen zich vastklampen aan kankercellen
T‑cel‑engagerende antilichamen werken als moleculaire koppelaars: het ene uiteinde grijpt een T‑cel, het andere hecht aan een doelmolecuul op de kankercel, waardoor de twee in direct contact komen zodat de T‑cel de prooi kan doden. Bij multipel myeloom is GPRC5D een aantrekkelijk doel omdat het overvloedig aanwezig is op maligne plasmacellen maar nauwelijks op de meeste normale weefsels. Patiënten die behandeld zijn met een GPRC5D‑gericht middel genaamd talquetamab bereiken vaak diepe remissies. Toch krijgt vrijwel iedereen uiteindelijk een terugval, wat een cruciale vraag oproept: veranderen de kankercellen het doelwit waarop deze middelen vertrouwen?
De evolutie van tumoren in real time volgen
De onderzoekers volgden 21 mensen met moeilijk te behandelen myeloom die talquetamab kregen. Ze verzamelden beenmergmonsters voor de behandeling bij sommige patiënten en opnieuw bij terugval, en gebruikten meerdere lagen DNA‑, RNA‑ en chromatineanalyse om de tumorcellen te onderzoeken. Dit ultra‑gedetailleerde beeld toonde aan dat bij ongeveer twee derde van de teruggevallen patiënten de kanker GPRC5D op manieren had aangepast die het effect van het middel zouden verminderen of blokkeren. Opvallend was dat meerdere verschillende resistente subclonen—genetisch verschillende takken van de tumor—vaak naast elkaar in dezelfde persoon bestonden, wat aantoont dat evolutie richting ontsnapping tegelijk langs meerdere wegen kan verlopen.
Drie hoofdmanieren waarop tumoren het doel verbergen
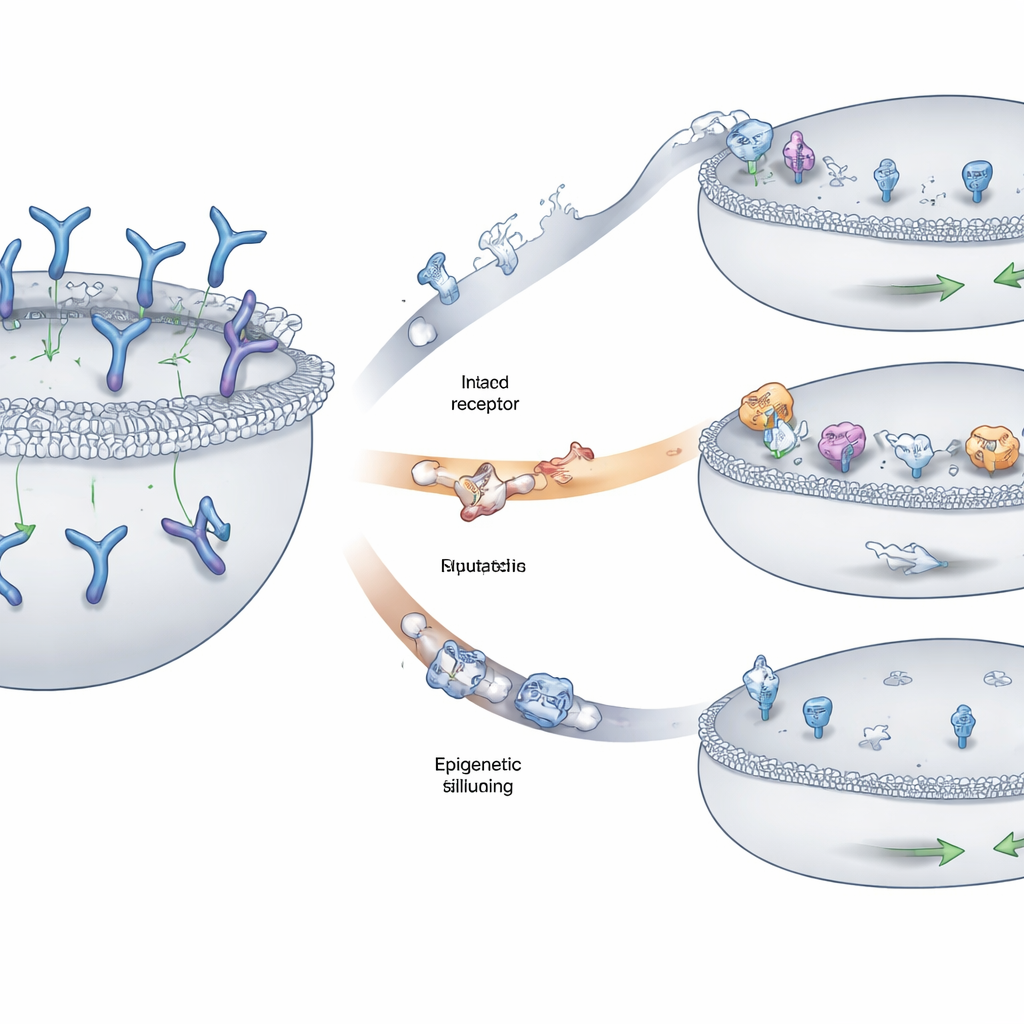
Het team vond drie terugkerende patronen waarmee myeloomcellen herkenning ontliepen. Bij sommige patiënten waren stukken van het chromosoom met het GPRC5D‑gen op beide kopieën verwijderd, waardoor de vlag volledig van het celoppervlak verdween. Bij anderen zorgden kleinere veranderingen—enkele letters in het DNA verwisseld of kleine inserties en deleties—voor vervorming van belangrijke regio’s van het GPRC5D‑eiwit. Veel van deze veranderingen verstoorden delen van het eiwit die nodig zijn om correct van binnen de cel naar het buitenmembraan te reizen, waardoor GPRC5D vast kwam te zitten in een intern compartiment in plaats van te worden getoond waar het middel het kon zien. Een derde route betrof epigenetische stilte: het DNA rond GPRC5D werd strak ingepakt en chemisch gemarkeerd zodat het gen nauwelijks werd afgelezen, hoewel de onderliggende sequentie grotendeels intact bleef. Tumorcellen die deze strategie gebruikten, maakten weinig tot geen GPRC5D meer aan.
Wanneer de vlag er wel is maar het slot niet meer past
Niet alle ontsnappingsroutes verwijderden GPRC5D van het celoppervlak. In sommige gevallen leek het eiwit normaal bij standaardlaboratoriumtests, maar paste het niet meer op het middel als een sleutel in een slot. Het team reconstrueerde specifieke patiëntafgeleide mutaties in laboratoriumcelijnen en testte hoe goed verschillende GPRC5D‑gerichte antilichamen zich aan deze cellen konden binden en ze konden doden. Eén mutatie veranderde subtiel de exacte plek waar talquetamab aan de receptor grijpt, wat de bindings- en celdodend vermogen van het middel sterk verminderde, hoewel de receptor zichtbaar bleef bij routinematige kleuring. Intrigerend genoeg bleef een ander GPRC5D‑gericht middel dat zich op twee plaatsen aan de receptor vastzet effectief tegen meerdere van deze mutants, wat benadrukt hoe geneesmiddelontwerp—bijvoorbeeld multivalente of multi‑epitoopbinding—kan bepalen of resistente klonen overleven.
Buiten het doel: andere beperkingen van immuunaanval
Hoewel bij de meeste terugvallen enige vorm van GPRC5D‑verlies of wijziging werd gezien, herstelden een minderheid van patiënten zonder duidelijke veranderingen in het doel zelf. In deze gevallen leek het probleem te liggen bij de T‑cellen: ze waren minder fit en minder in staat kankercellen te doden in laboratoriumtesten, wat suggereert dat langdurige continue blootstelling aan engager‑therapie het immuunsysteem kan uitputten. De studie ontdekte ook dat een bepaald genetisch subtype van myeloom (met een chromosomale verwisseling genoemd t(11;14)) van nature het GPRC5D‑gen in een meer “gesloten” chromatine‑toestand houdt, met een lagere basisexpressie. Dit suggereert dat sommige patiënten mogelijk een slechtere respons hebben omdat hun tumoren van meet af aan met gedempte niveaus van de doelvlag beginnen.
Wat dit betekent voor patiënten en toekomstige behandelingen
Voor patiënten en clinici verklaart dit werk waarom zelfs zeer krachtige GPRC5D‑gerichte therapieën nog geen genezingen zijn: myeloomcellen kunnen de vlag die deze middelen nodig hebben verwijderen, herschikken, verkeerd routen of uitschakelen, en ze doen dat vaak op meerdere manieren tegelijk. De bevindingen suggereren dat het monitoren van tumor‑DNA, in plaats van alleen eiwitniveaus te meten, belangrijk zal zijn om opkomende ontsnappingsmutaties te detecteren die standaardtests kunnen missen. Ze wijzen ook op strategieën voor de volgende generatie—zoals middelen die GPRC5D op meerdere plaatsen steviger binden, combinaties die meer dan één doel tegelijk stimuleren, of agentia die gesilenceerde genen opnieuw openen—om de tumorontwikkeling voor te blijven. In wezen brengt deze studie de ontsnappingsroutes in kaart die myeloom gebruikt, zodat toekomstige therapieën ontworpen kunnen worden om ze te blokkeren en T‑celgebaseerde behandelingen langer effectief te houden.
Bronvermelding: Lee, H., Ahn, S., Gonzales, G.A. et al. Multimodal antigenic escape to GPRC5D-targeted T cell engagers in multiple myeloma. Nat Med 32, 964–977 (2026). https://doi.org/10.1038/s41591-025-04175-8
Trefwoorden: multipel myeloom, T‑cel engageren, GPRC5D, antigeenontsnapping, kankerimmunotherapie