Clear Sky Science · nl
Linavonkibart en pembrolizumab bij gevorderde solide tumoren resistent tegen immuuncheckpointremming: een fase 1‑onderzoek
Waarom hardnekkige kankers ons allemaal aangaan
Immunotherapieën die de remmen van het immuunsysteem wegnemen, hebben de behandeling van vele kankers veranderd, maar de meeste patiënten profiteren er nooit van of hun tumoren groeien uiteindelijk weer. Deze studie onderzoekt een nieuw antilichaammiddel, linavonkibart, dat ontworpen is om een krachtige beschermingsmantel te blokkeren die tumoren gebruiken om zich te verbergen voor immuunaanvallen, en combineert het met een bestaande immunotherapie, pembrolizumab. De resultaten geven een vroege indicatie dat het zelfs bij patiënten van wie de kanker gestopt was met reageren op checkpointmiddelen mogelijk kan zijn om de immuuncontrole te herstellen, terwijl de bijwerkingen beheersbaar blijven.
Een verborgen schild rond tumoren
Veel moderne immunotherapieën werken door zogenoemde checkpoint‑moleculen zoals PD‑1 te blokkeren, die normaal T‑cellen remmen. Wanneer deze remmen worden losgelaten, kunnen immuuncellen de kanker krachtiger aanvallen. Tumoren passen zich echter vaak aan door een vijandige omgeving te creëren die cytotoxische T‑cellen buiten houdt of verzwakt zodra ze binnenkomen. Een belangrijke bouwer van deze beschermende bubbel is een signaalproteïne genaamd TGFβ1, die zowel door kankercellen als door nabije ondersteunende cellen wordt geproduceerd. Eerdere pogingen om de gehele TGFβ‑familie te remmen lieten veelbelovende resultaten zien maar veroorzaakten ernstige hart‑ en bloedingsproblemen, omdat andere familiesubtypen belangrijk zijn voor gezonde weefsels. Linavonkibart is ontwikkeld om hier omheen te werken door selectief alleen de latente, inactieve vorm van TGFβ1 te neutraliseren voordat deze actief wordt, terwijl nauwverwante moleculen die het lichaam nodig heeft ongemoeid blijven.
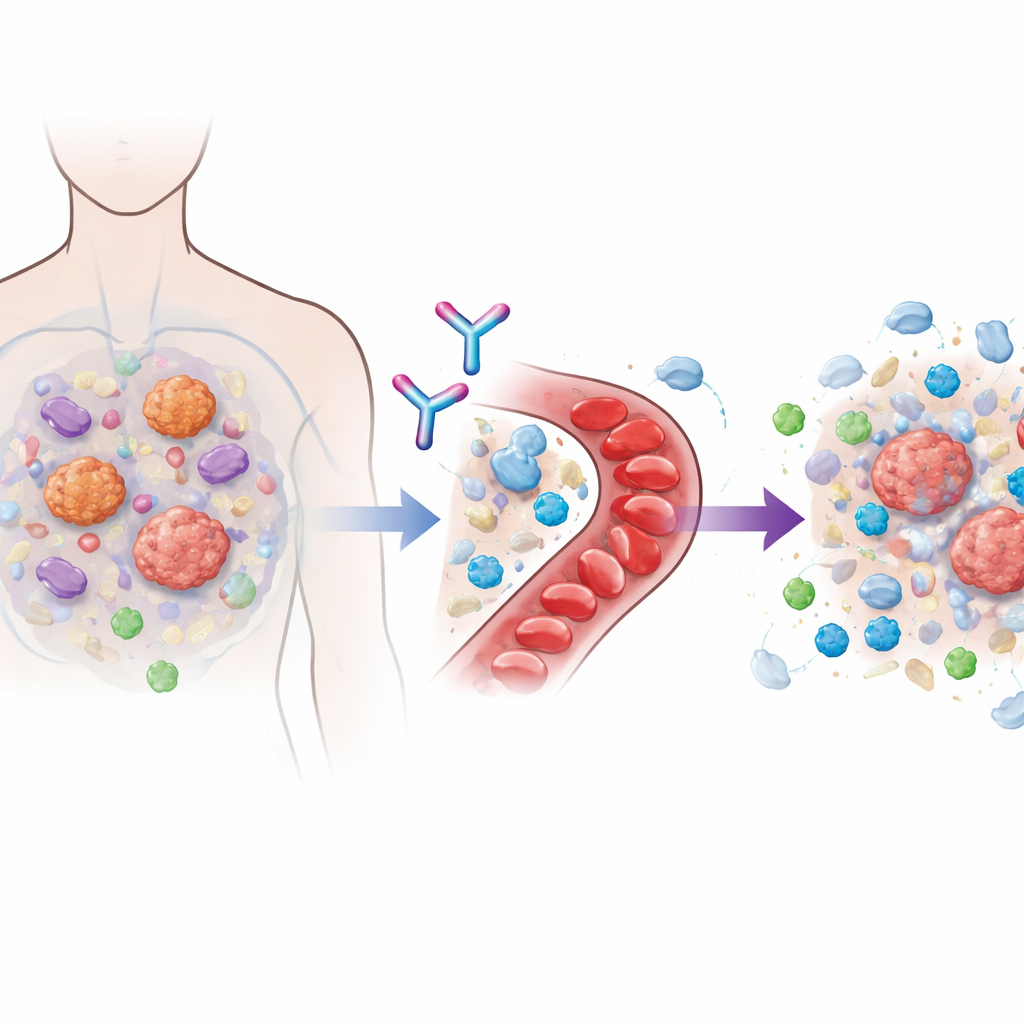
Een zorgvuldig eerste‑in‑mens onderzoek ontwerpen
De DRAGON‑trial was een multicentrisch fase‑1‑onderzoek uitgevoerd in 22 ziekenhuizen in de Verenigde Staten en Zuid‑Korea. Er werden 112 volwassenen met gevorderde solide tumoren opgenomen, die allemaal beperkte behandelingsopties hadden. In het eerste deel van de studie kreeg linavonkibart alleen toegediend in oplopende doses aan kleine patiëntengroepen, of gecombineerd met hun eerdere PD‑1‑gebaseerde middel. Deze stapsgewijze aanpak werd gebruikt om veiligheid, de farmacokinetiek en farmacodynamiek en de keuze van een dosis voor bredere toetsing in kaart te brengen. In het tweede deel kregen 78 patiënten wiens tumoren al resistent waren tegen ten minste één kuur PD‑1‑immunotherapie een vaste dosis linavonkibart samen met pembrolizumab. Deze patiënten hadden moeilijk te behandelen tumoren, waaronder heldercel‑nierkanker, melanoom, hoofd‑ en halskanker, urotheel (blaas)‑kanker en longkanker, en de meesten hadden meerdere voorafgaande behandelingen ondergaan.
Veiligheid eerst: wat gebeurde er met patiënten
Het belangrijkste doel van dit vroege fase‑onderzoek was veiligheid, en linavonkibart leverde op dat punt bemoedigende resultaten. Over alle dosisniveaus werd geen maximale verdraagbare dosis bereikt, en er werden geen dodelijke of dosisbegrenzende bijwerkingen gerelateerd aan het middel gezien. Wanneer linavonkibart werd gecombineerd met pembrolizumab op de fase‑2‑dosis, ervoer ongeveer driekwart van de patiënten enige door de behandeling veroorzaakte bijwerking, vergelijkbaar met wat vaak wordt gezien bij immunotherapie alleen. Huiduitslag en jeuk waren de meest voorkomende aanvullende problemen, en een klein aantal patiënten ontwikkelde ernstigere huid‑ of longontstekingen. Belangrijk is dat het gevaarlijke immuunoverreactiesyndroom, de cytokine release‑syndroom, dat bij sommige antilichaamtherapieën kan optreden, niet werd waargenomen, en het algemene veiligheidsbeeld grotendeels overeenkwam met dat van pembrolizumab alleen.
Signalen dat het immuunsysteem heractiveerbaar is
Hoewel dit geen groot, definitief werkzaamheidsonderzoek was, wezen meerdere tekenen erop dat het uitschakelen van TGFβ1 kan helpen de respons op PD‑1‑blokkade te laten heropleven. In de expansiefase krimpten meetbare tumoren onder de combinatie linavonkibart–pembrolizumab bij een opvallend deel van de patiënten die eerder gestopt waren met profiteren van PD‑1‑middelen. Bevestigde responspercentages waren 20% bij heldercel‑nierkanker, 18,2% bij melanoom en iets meer dan 9% bij hoofd‑en‑hals‑ en urothele tumoren, waarbij één nierkankerpatiënt een volledige verdwijning van zichtbaar ziektebeeld bereikte. Veel van deze responsen duurden maandenlang, en reagerende patiënten bleven over het algemeen veel langer op de combinatie dan op hun eerdere PD‑1‑therapie. Biopten afgenomen voor en na behandeling boden een biologische verklaring: tumoren toonden grotere infiltratie van CD8 “killer” T‑cellen, hogere niveaus van geactiveerde T‑cellen, minder onderdrukkende regulatoire T‑cellen en myeloïde cellen, en een algehele verschuiving naar een meer ontstoken, aanvalsklare micro‑omgeving.
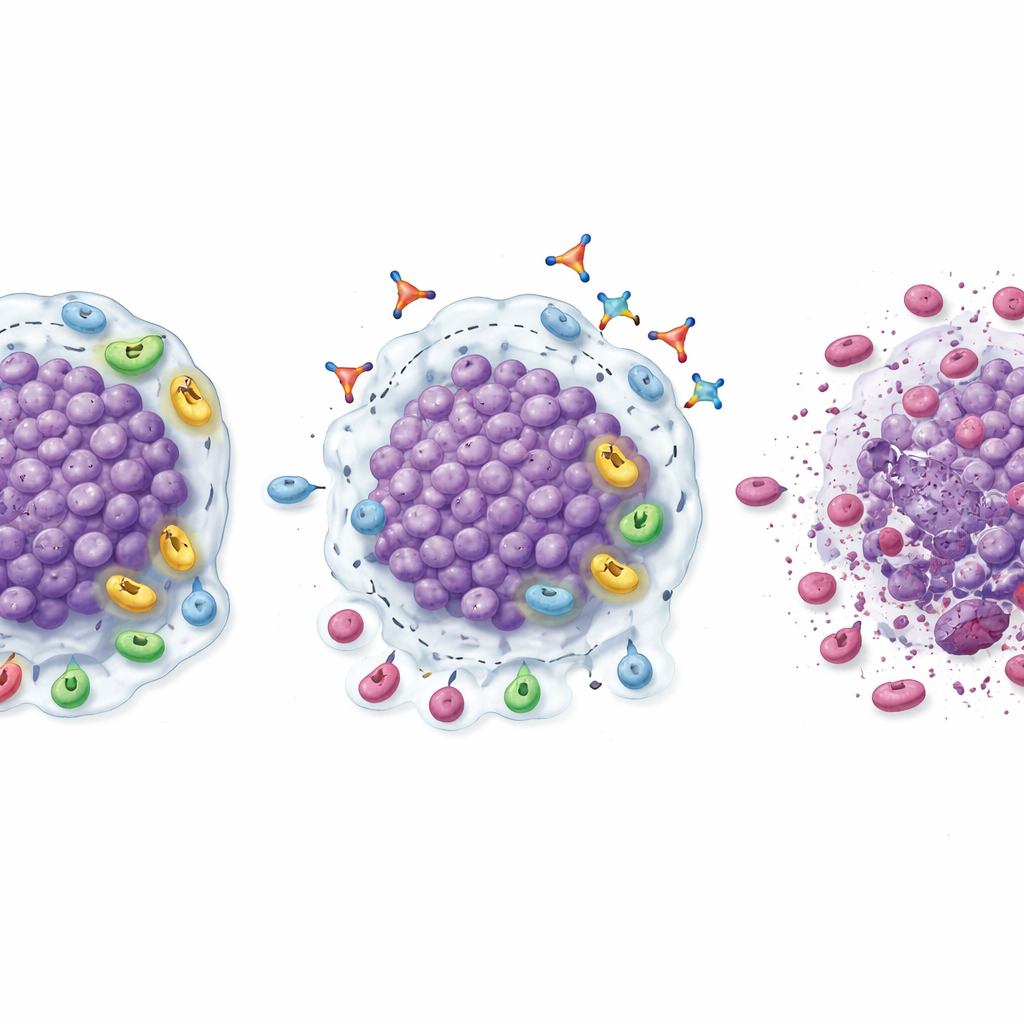
Wie heeft het meeste baat?
De onderzoekers onderzochten ook welke patiënten bijzonder waarschijnlijk zouden reageren. Bij heldercel‑nierkanker waren tumoren die bij aanvang al veel CD8‑T‑cellen bevatten — maar ook rijk waren aan regulatoire T‑cellen en hoge TGFβ1‑expressie toonden — vaker kleiner geworden onder de combinatietherapie. Bij deze patiënten waren responspercentages en progressievrije overleving duidelijk hoger dan in de bredere nierkankergroep. Dit patroon suggereert een “sweet spot”: tumoren met veel aanwezige immuunsoldaten maar die geremd worden door TGFβ1‑gemedieerde suppressie kunnen ideale kandidaten zijn voor linavonkibart plus PD‑1‑blokkade. Als dit wordt bevestigd in grotere onderzoeken, zouden eenvoudige weefseltesten voor deze markers artsen kunnen helpen de patiënten te selecteren die het meest waarschijnlijk profiteren.
Wat dit werk voortaan betekent
Voor mensen met gevorderde kankers die al resistent zijn geworden tegen immunotherapie, is het vooruitzicht om hun eigen immuunsysteem opnieuw aan te wakkeren zonder ernstige toxiciteit toe te voegen aantrekkelijk. Deze eerste‑in‑mens‑trial levert vroege aanwijzingen dat het selectief uitschakelen van het TGFβ1‑schild met linavonkibart veilig kan gebeuren en mogelijk zinvolle tumorcontrole kan herstellen wanneer het wordt gecombineerd met een PD‑1‑remmer, met name bij bepaalde nierkankers. Hoewel de studie klein en niet-gerandomiseerd was, vormen het veiligheidsprofiel, de biologische bevindingen en de duurzame responsen samen een sterke motivatie voor grotere fase‑2‑onderzoeken. Als vervolgonderzoek deze bevindingen bevestigt, kan deze benadering de kring van patiënten die baat hebben bij immunotherapie uitbreiden en sommige momenteel hardnekkige kankers weer kwetsbaar maken voor de eigen afweer van het lichaam.
Bronvermelding: Yap, T.A., Sweis, R.F., Vaishampayan, U. et al. Linavonkibart and pembrolizumab in immune checkpoint blockade-resistant advanced solid tumors: a phase 1 trial. Nat Med 32, 992–1001 (2026). https://doi.org/10.1038/s41591-025-04157-w
Trefwoorden: kankerimmunotherapie, TGFβ1‑remming, resistentie tegen immuuncheckpoints, heldercel niercelcarcinoom, tumormicro‑omgeving