Clear Sky Science · nl
Aangeboren antivirale en immuunfuncties gekoppeld aan het krimpen van het HIV-reservoir na anti-PD-1-therapie
Waarom dit onderzoek belangrijk is
Moderne hiv-medicijnen kunnen het virus tientallen jaren onder controle houden, maar ze kunnen het niet volledig uitroeien. Een klein "reservoir" van geïnfecteerde cellen ligt sluimerend in het lichaam en kan de infectie opnieuw op gang brengen als behandeling stopt. Deze studie onderzoekt of een vorm van kankerimmunotherapie die de remmen van het immuunsysteem loslaat, ook kan helpen dit verborgen hiv-reservoir te verkleinen en wijst op biologische aanwijzingen die kunnen voorspellen wie het meest baat zal hebben.
Verborgen virus en een nieuw soort medicijn
Mensen die vandaag de dag met hiv leven, gebruiken vaak antiretrovirale therapie (ART), die het virus in het bloed tot niet-detecteerbare niveaus terugbrengt. Toch blijft het virus aanwezig in een kleine populatie immuuncellen, vooral geheugen-CD4-T-cellen, waar het stil ligt en buiten bereik van medicijnen. Veel van deze cellen tonen een oppervlakte-eiwit genaamd PD-1, onderdeel van een remsysteem dat normaal voorkomt dat het immuunsysteem overreageert. Kankermedicijnen die PD-1 blokkeren hebben de behandeling van verschillende tumoren veranderd door immuuncellen te heractiveren. Omdat PD-1 ook op hiv-dragende cellen en op uitgeputte virusbestrijdende cellen voorkomt, vroegen onderzoekers zich af of dezelfde medicijnen kunnen helpen de grip van hiv te versoepelen.
Een onderzoek bij mensen met zowel hiv als kanker
In deze studie kregen 30 volwassenen met hiv en verschillende kankers elke drie weken het PD-1-blokkerende antilichaam pembrolizumab, bovenop hun gebruikelijke ART. De behandeling was over het algemeen veilig en sommige deelnemers behaalden gedeeltelijke of volledige tumorreducties. De onderzoekers verzamelden bloed vóór de behandeling, 24 uur later, een week later en aan het einde van de therapie, wat vele maanden later kon zijn. Ze maten hiv-DNA in immuuncellen als marker van het latente reservoir, hiv-RNA als teken van virale activiteit, en een uitgebreide set immuunsignalen met RNA-sequencing, eiwitmetingen en single-cellanalyses. 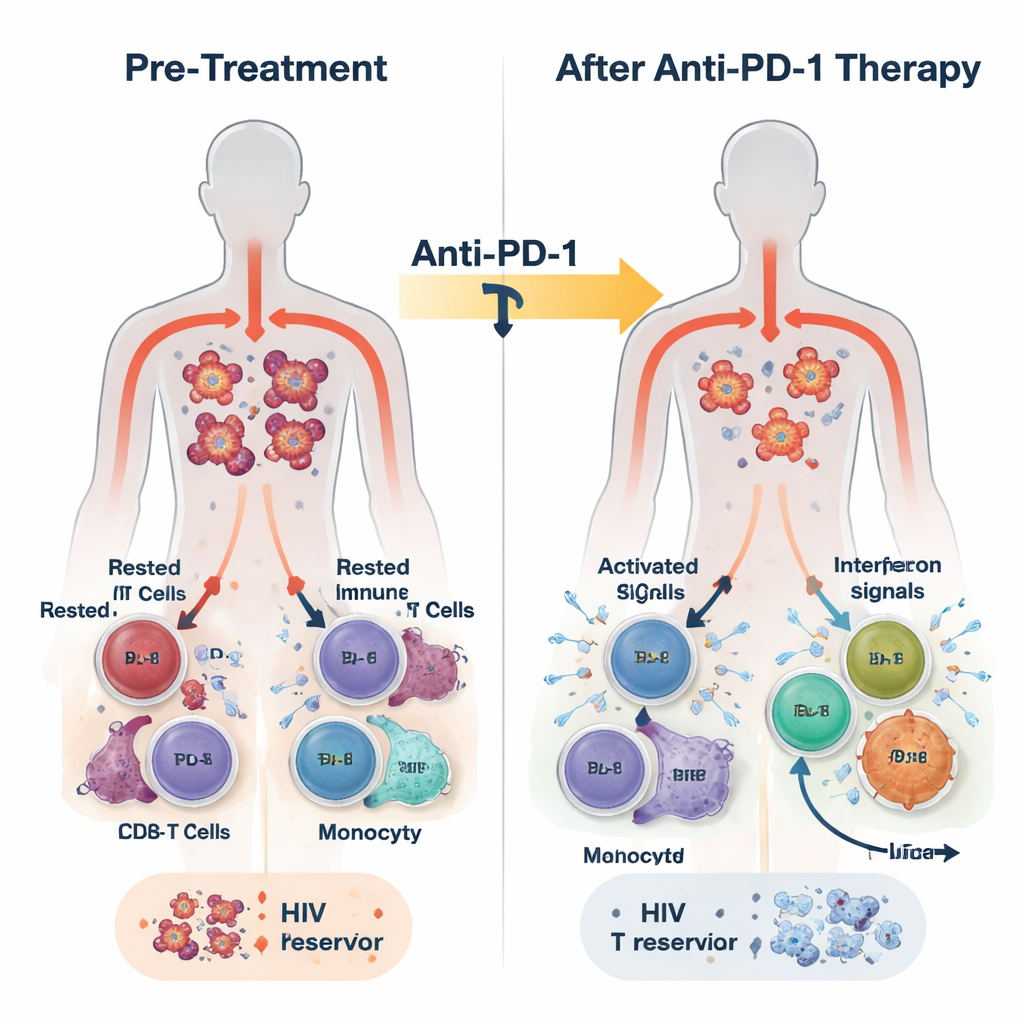
Een vroege antivirale "alarmfase" bij sommige deelnemers
Al binnen 24 uur na de eerste dosis toonde bloed van de meeste deelnemers een uitbarsting van aangeboren immuunactiviteit. Gehalten van ontstekingsboodschappers zoals interferonen (de klassieke antivirale alarmsignalen van het lichaam) en IL-6 stegen, terwijl een onderdrukkende stof genaamd TGF-beta daalde. Tegelijkertijd werden genprogramma’s gekoppeld aan antivirale verdediging, monocytenactiviteit en effectorfunctie van CD8-T-cellen geactiveerd in de witte bloedcellen. Nauwkeuriger onderzoek liet zien dat deze respons niet uniform was. Aan het einde van de behandeling konden de deelnemers op basis van de sterkte en persistentie van interferon-gestimuleerde genactiviteiten (ISG) in twee groepen worden verdeeld: een ISG-hoog groep die deze antivirale programma’s bleef voeren, en een ISG-laag groep waarin ze vervaagden.
Immuunpatronen gekoppeld aan het verkleinen van HIV-reservoirs
De ISG-hoog deelnemers begonnen met lagere hoeveelheden hiv-DNA in hun CD4-T-cellen dan de ISG-laag groep en ervaarden vervolgens een verdere, ongeveer tweevoudige daling van dit latente reservoir in de loop van de tijd. Ze hadden ook de neiging minder CD4-T-cellen te tonen die hiv in laboratoriumtests konden heractiveren tegen het einde van de therapie. Daarentegen vertoonden deelnemers in de ISG-laag groep weinig of geen verandering in hiv-DNA en hadden ze vaak meer cellen die geïnduceerd konden worden om hiv-RNA te produceren. Hoogresolutie single-cellstudies boden een mechanistisch beeld: een subset van monocyten verhoogde snel de expressie van antivirale genen; hiv-specifieke CD8-T-cellen breidden zich uit en werden meer proliferaat; en bepaalde CD4-T-celsubsets upreguleerden antivirale verdedigingen terwijl andere die geassocieerd zijn met aanhoudende virale transcriptie afnamen. Experimenten in cellen van gezonde donoren bevestigden dat het stimuleren van aangeboren sensoren of interferonroutes zowel antivirale eiwitten in CD4-T-cellen kan verhogen als hun vatbaarheid voor hiv-infectie kan verminderen. 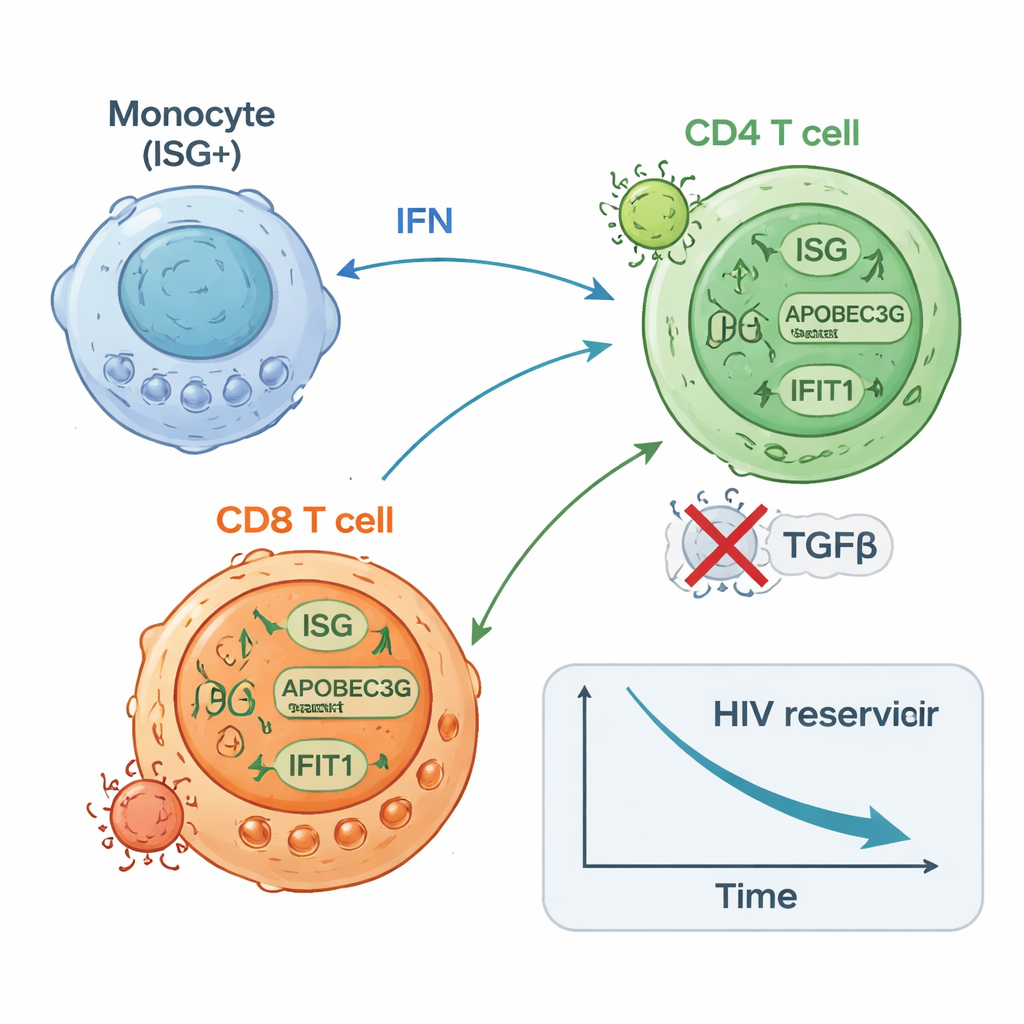
Aanwijzingen voor het kiezen en verbeteren van toekomstige therapieën
Intrigerend genoeg komen dezelfde antivirale genpatronen die in de ISG-hoog groep werden gezien ook voor in bloed van sommige mensen met andere kankers of infecties, wat suggereert dat een van nature “geprimede” immuunstatus bij een subset van individuen kan bestaan. In deze studie was die geprimede staat — gedefinieerd door sterke interferonprogramma’s in myeloïde cellen en T-cellen en lage activiteit van regulerende paden zoals WNT-signaalgeving en TGF-beta — gekoppeld aan zowel een veiligere controle van het hiv-reservoir als aan kenmerken die in andere onderzoeken met betere kankeruitkomsten geassocieerd werden. De auteurs stellen voor dat het combineren van PD-1-blokkade met zorgvuldig getimede versterking van interferonroutes, of met medicijnen die TGF-beta blokkeren, het verminderen van het hiv-reservoir verder zou kunnen versterken terwijl kanker nog steeds onder controle blijft.
Wat dit betekent voor mensen met hiv
Dit werk biedt nog geen genezing en PD-1-blokkerende medicijnen blijven krachtige therapieën die het best gereserveerd zijn voor ernstige aandoeningen zoals kanker. Maar het levert belangrijk bewijs dat het tijdelijk opheffen van immuunremmen een snelle, gecoördineerde antivirale respons kan uitlokken die de voorraad hiv-geïnfecteerde cellen bij sommige personen op ART meetbaar verkleint. Even belangrijk is dat het een set bloedgebaseerde immuunsignaturen schetst waarmee artsen mogelijk mensen kunnen identificeren die het meest waarschijnlijk baat hebben bij dergelijke benaderingen, en waarmee combinatiestrategieën ontworpen kunnen worden die het immuunsysteem stimuleren om meer van hiv’s laatste schuilplaatsen bloot te leggen en op te ruimen.
Bronvermelding: Talla, A., Azevedo, J.L.L.C., Latif, M.B. et al. Innate antiviral and immune functions associated with the HIV reservoir decay after anti-PD-1 therapy. Nat Med 32, 505–517 (2026). https://doi.org/10.1038/s41591-025-04139-y
Trefwoorden: HIV-reservoir, PD-1-blokkade, interferonrespons, kankerimmunotherapie, antiretrovirale therapie