Clear Sky Science · nl
Genotype-gestratificeerde aanvullende dexamethason bij tuberculeuze meningitis bij hiv-negatieve volwassenen: een gerandomiseerde fase 3‑trial
Waarom deze herseninfectiestudie ertoe doet
Tuberculeuze meningitis is de dodelijkste vorm van tuberculose en valt de hersenen en hun beschermende membranen aan. Artsen wereldwijd voegen routinematig een krachtig ontstekingsremmend middel, dexamethason, toe aan de tuberculosebehandeling in de hoop meer levens te redden. Toch is het voordeel beperkt en ongelijk verdeeld, wat een dringende vraag oproept: kunnen we iemands genen gebruiken om te bepalen wie dit middel echt nodig heeft en wie er veilig zonder kan? Deze grote Vietnamese trial had tot doel dat idee rechtstreeks te testen.
Een gevaarlijke infectie van de hersenen
Tuberculeuze meningitis begint wanneer tuberculosebacteriën zich vanuit de longen naar de hersenen verspreiden. Wanneer het immuunsysteem reageert, ontstaat zwelling en ontsteking rond de hersenen en het ruggenmerg, wat hoofdpijn, koorts, verwardheid en zonder behandeling vaak de dood veroorzaakt. De standaardzorg combineert maandenlange antibiotica om de bacteriën te doden met steroïden om schadelijke ontsteking te dempen. Eerdere studies toonden aan dat dexamethason de sterfte licht verlaagde in het geheel, maar niet in elke patiëntengroep, waardoor onduidelijk bleef wanneer het middel echt helpt.
Een genetische aanwijzing voor steroidrespons
Eerder onderzoek wees op een gen genaamd LTA4H, dat helpt te bepalen hoe sterk het immuunsysteem reageert tijdens tuberculose. Mensen erven verschillende varianten, of genotypen, van dit gen, aangeduid als CC, CT en TT. Kleinere eerdere studies suggereerden dat patiënten met het TT-type een zeer sterke ontstekingsreactie hadden maar duidelijk profijt van dexamethason, terwijl degenen met CC- of CT-typen mogelijk geen voordeel hadden en in sommige gevallen zelfs schade konden ondervinden. Als dat waar zou zijn, zouden artsen het steroidgebruik kunnen afstemmen op een snel genetisch testje aan het bed van de patiënt.
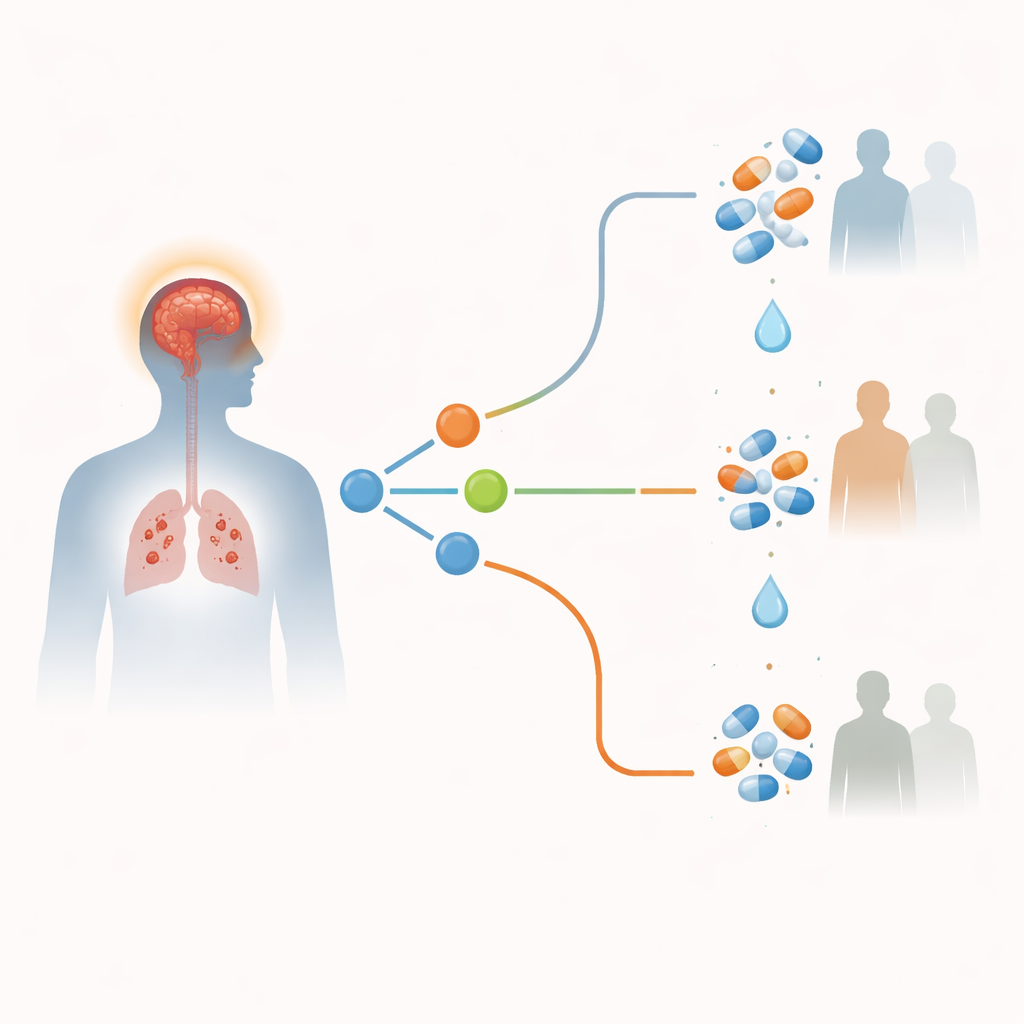
Een genotyperichte klinische trial
Om dit idee rigoureus te testen voerden onderzoekers een grote fase 3‑trial uit in twee ziekenhuizen in Ho Chi Minhstad. Ze schreven 720 volwassenen in met vermoedelijke tuberculeuze meningitis die geen hiv hadden. Allen kregen standaard tuberculoseantibiotica. Na een snelle bloedtest om hun LTA4H‑genotype te bepalen, werden 613 patiënten met de veelvoorkomende CC- of CT‑typen willekeurig toegewezen om gedurende 6–8 weken dexamethason of een bijpassende placebo te krijgen. Omdat eerdere data een sterk voordeel suggereerden, kregen de 89 patiënten met het zeldzame TT‑type allemaal open‑label dexamethason en werden zij niet gerandomiseerd. De belangrijkste uitkomst was of patiënten binnen 12 maanden overleden of een nieuw ernstig hersenprobleem ontwikkelden, zoals een groot bewustzijnsverlies of nieuwe verlamming.
Wat de trial vond
Bij CC‑ en CT‑patiënten waren de uitkomsten opvallend gelijk, ongeacht of ze dexamethason kregen. Ongeveer een op de drie patiënten in elke groep stierf of kreeg binnen een jaar een nieuw ernstig hersengebeuren. Statistische toetsen konden niet aantonen dat het overslaan van dexamethason “niet slechter was” dan het gebruik ervan, maar lieten evenmin zien dat dexamethason duidelijk de overleving of het uitblijven van invaliditeit verbeterde bij deze genotypen. Ernstige bijwerkingen — zoals ernstige infecties of bloedingen — kwamen ongeveer even vaak voor bij dexamethason en placebo, wat suggereert dat het middel in deze setting over het algemeen veilig was. TT‑patiënten, die allemaal dexamethason ontvingen, hadden in het geheel vergelijkbare uitkomsten als de andere groepen, hoewel er aanwijzingen waren dat zij mogelijk beter af waren dan anderen wanneer hun ziekte zeer ernstig was.
De immuunrespons in de hersenen onderzocht
Het team onderzocht ook ruggenmergvocht- en bloedmonsters om te zien hoe dexamethason en het LTA4H‑genotype de ontsteking beïnvloedden. Dexamethason verminderde duidelijk verschillende inflammatoire eiwitten en immuunroutes in het ruggenmergvocht van CC‑patiënten, en in mindere mate bij CT‑patiënten, gedurende de eerste behandelingsmaand. In het bloed waren sterker door steroïden gedreven veranderingen vooral zichtbaar bij CT‑patiënten. Ondanks deze meetbare verschuivingen was er geen eenvoudig patroon dat de omvang van de ontstekingsreactie koppelde aan wie overleefde of stierf, wat aantoont hoe complex de ziekte is.
Wat dit vandaag betekent voor patiënten
Toen de onderzoekers de data van deze trial combineerden met een eerdere Vietnamese studie met hetzelfde steroidregime, vonden ze dat dexamethason de totale sterfte bij hiv‑negatieve volwassenen met tuberculeuze meningitis bescheiden verlaagde. Samen ondersteunen de resultaten het voortzetten van dexamethason voor deze patiënten, ongeacht hun LTA4H‑genotype. Tegelijkertijd bleek de gehoopte eenvoudige genetische regel — alleen steroïden geven aan TT‑patiënten en ze vermijden bij anderen — niet stand te houden. Het werk laat zien dat onze immuunrespons op hersentuberculose door veel factoren wordt bepaald, niet slechts door één gen, en dat nieuwe, nauwkeuriger gerichte ontstekingsremmende behandelingen nodig zijn. Voorlopig blijven vroege diagnose, snelle antibiotica en standaard dexamethason de best bewezen strategie om de overleving bij deze verwoestende ziekte te verbeteren.
Bronvermelding: Donovan, J., Duc Bang, N., Dong, H.K.T. et al. Genotype-stratified adjunctive dexamethasone for tuberculous meningitis in HIV-negative adults: a randomized controlled phase 3 trial. Nat Med 32, 849–858 (2026). https://doi.org/10.1038/s41591-025-04138-z
Trefwoorden: tuberculeuze meningitis, dexamethason, gastheer genetica, neuro-inflammatie, klinische trial