Clear Sky Science · nl
Interpreteerbaar ontstekingslandschap van circulerende immuuncellen
Waarom ontsteking in het bloed voor u van belang is
Ontsteking ligt ten grondslag aan veel ziekten, van artritis en astma tot COVID-19 en kanker. Toch hebben artsen moeite om de ontstekingssignalen van het lichaam zo te interpreteren dat duidelijk wordt wat er misgaat en welke behandeling het beste werkt. Deze studie bouwt een omvangelijke "kaart" van immuuncellen die in het bloed circuleren en toont aan hoe deze cellen kunnen dienen als levende, gemakkelijk te bemonsteren biomarkers om een breed scala aan ontstekingsziekten te classificeren.
Het bouwen van een gigantische kaart van immuuncellen
Om dit landschap in kaart te brengen, analyseerden de onderzoekers meer dan 6,5 miljoen immuuncellen afkomstig van het bloed van 1.047 mensen. Deze vrijwilligers vertegenwoordigden 19 aandoeningen, waaronder auto-immuunziekten zoals lupus en reumatoïde artritis, chronische longziekten zoals astma en COPD, infecties zoals COVID-19 en HIV, en verschillende vormen van kanker, naast gezonde donoren. Met single-cell RNA sequencing maten ze welke genen in elke individuele cel aan stonden, en gebruikten vervolgens geavanceerde statistische methoden om technische verschillen tussen studies te corrigeren en cellen in 64 afzonderlijke immuunceltoestanden te groeperen. Deze "Ontstekingsatlas" bevat zowel bekende spelers—zoals T-cellen, B-cellen en monocyten—als meer gespecialiseerde subtypen die verschuiven met ziektebeeld.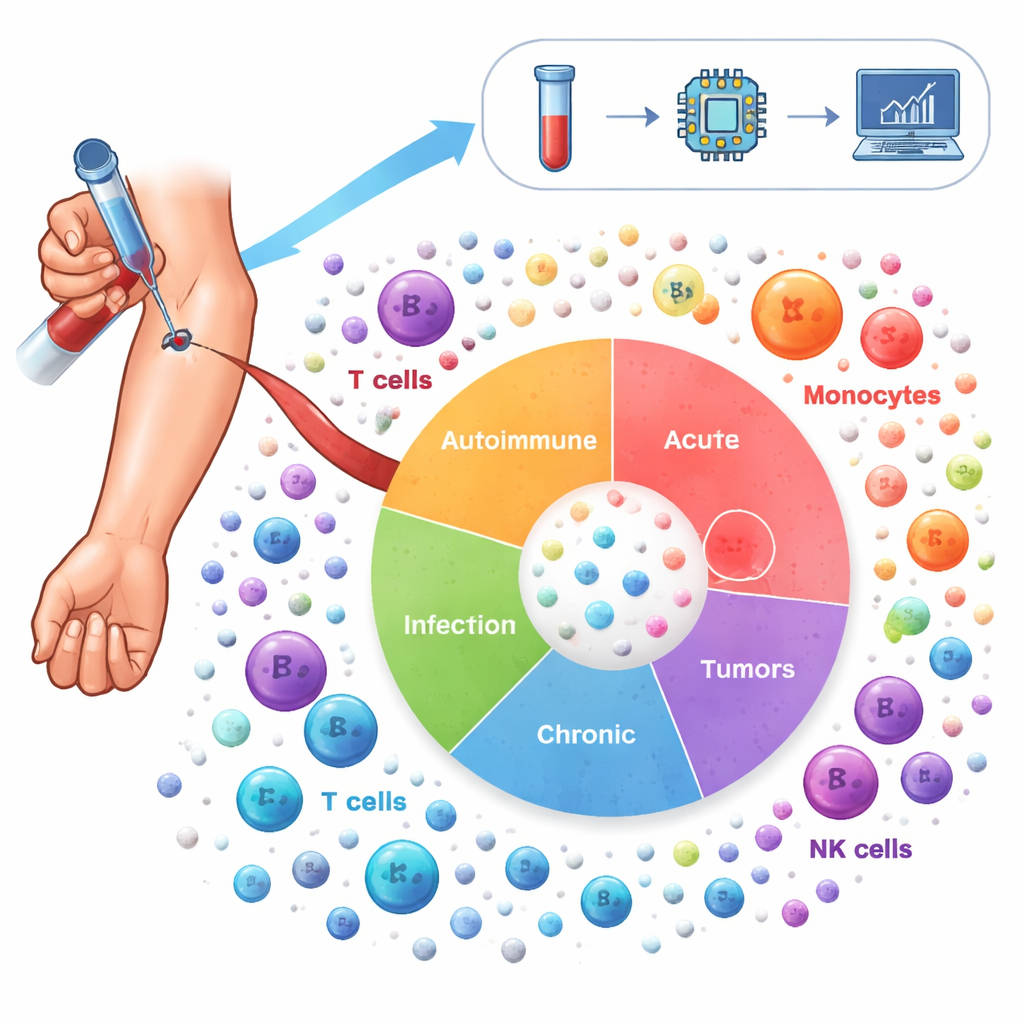
Het aflezen van de ontstekingshandtekeningen van het lichaam
Het team richtte zich vervolgens op genen die bepalen hoe immuuncellen geactiveerd raken, door het lichaam bewegen, antigenen presenteren en reageren op signaalmoleculen zoals interferonen en tumor necrosefactor. Ze groepeerden deze genen in 21 biologische "handtekeningen" en verfijnden ze per belangrijk celtype. Door patiënten te vergelijken met gezonde donoren konden ze zien welke handtekeningen in verschillende ziekten omhoog of omlaag waren bijgesteld. Zo vertoonden veel immuungemedieerde ontstekingsziekten sterkere activiteit van adhesiemoleculen en antigen-presentatie-machinerie, terwijl interferonresponsen in de meeste celtypen verlaagd waren maar verhoogd in bepaalde CD8 T-cellen. Virusinfecties zoals griep en COVID-19 versterkten interferon-geïnduceerde programma’s, terwijl chronische infecties zoals HIV en hepatitis B deze verzwakten.
Inzoomen op sleutelgenen en regelingsschakelaars
Aangezien brede handtekeningen belangrijke details verbergen, doken de onderzoekers dieper naar individuele genen en hun regulatoren. In niet-naïeve CD8 T-cellen vonden ze dat twee genen, FGFBP2 en GZMB, bijzonder actief waren in specifieke effector geheugen-subtypen, met name bij colitis ulcerosa. Deze genen zijn in verband gebracht met schade aan epitheliale oppervlakken, en hun sterke signaal in bloed suggereert dat deze agressieve cellen al geprimed zijn voordat ze weefsels binnengaan. Een afzonderlijke analyse van genregulerende netwerken benadrukte twee transcriptiefactoren, STAT1 en SP1, als centrale regelaars van interferon-geïnduceerde programma’s. Hun activiteitspatronen verschilden tussen ziekten en celtypes—bijvoorbeeld tegengesteld gedrag in monocyten versus CD8 T-cellen bij lupus, en verschuivingen tussen opvlamming en niet-opvlamming—wat aangeeft hoe dezelfde pathways in de ene context beschermend en in een andere schadelijk kunnen zijn.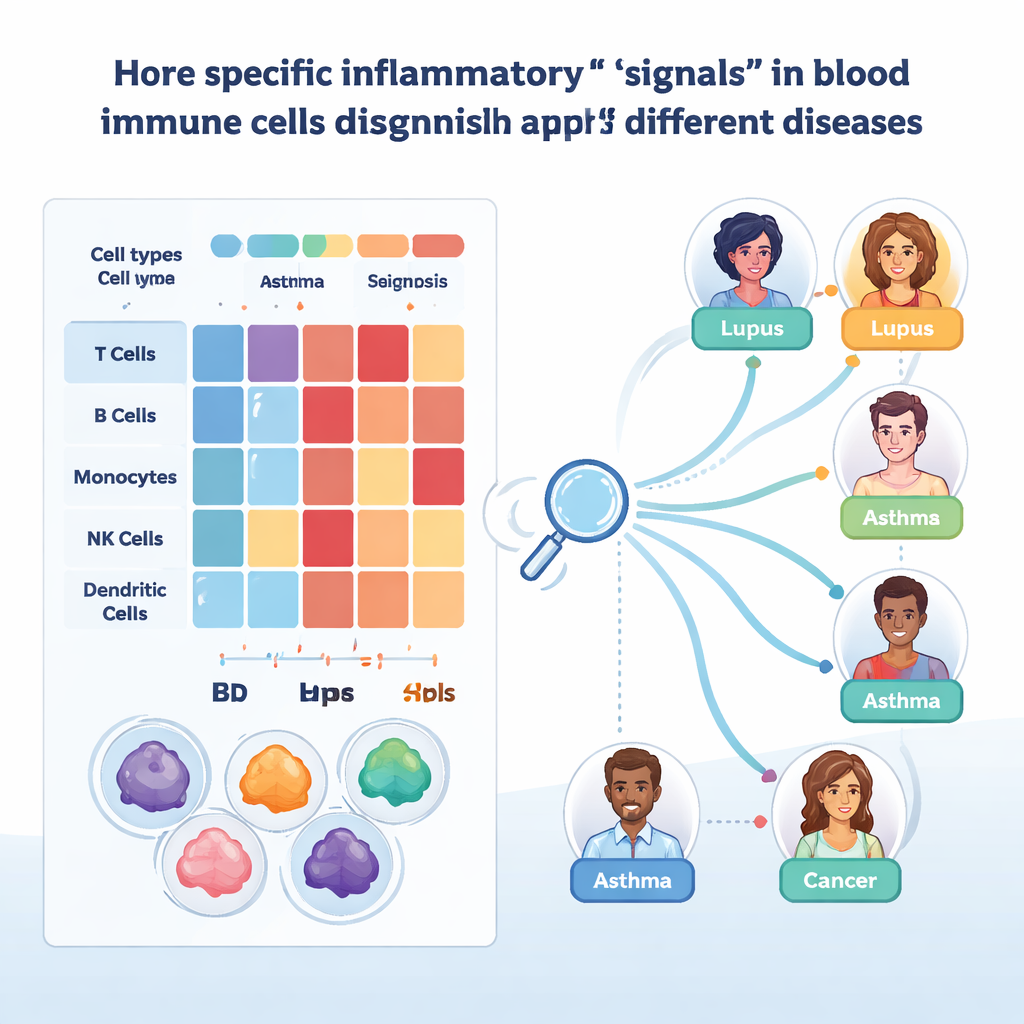
Machines trainen om ziekte te herkennen aan bloedcellen
Om van deze atlas een praktisch hulpmiddel te maken, pasten de onderzoekers interpreteerbare machine learning toe. Ze trainden gradient-boosted decision tree-modellen apart voor elk belangrijk celtype en lieten de algoritmen individuele cellen labelen met de juiste ziekte op basis van hun genexpressie. Deze modellen bereikten hoge nauwkeurigheid bij tests op achtergehouden monsters, vooral na correctie voor technische verschillen. Met behulp van SHAP, een methode die uitlegt welke genen elke beslissing aandrijven, konden de onderzoekers kandidaat-biomarkers identificeren. Een voorbeeld is CYBA in monocyten, waarvan de niveaus hielpen huidziekten zoals psoriasis te onderscheiden van darmontsteking bij ziekte van Crohn en colitis ulcerosa. Een ander voorbeeld is IFITM1 in bepaalde T-cellen en innate lymfoïde cellen, waarmee astma van COPD te scheiden viel en dat verschillende patronen van chronische antivirale verdediging suggereert.
Op weg naar een bloedgebaseerd diagnostisch kompas
Tot slot vroegen de auteurs zich af of gehele patiënten—niet alleen individuele cellen—geclassificeerd konden worden op basis van hun circulerende immuunprofielen. Ze projecteerden de data van elke cel in een gecomprimeerde "embedding"-ruimte, gemiddeldes van deze embeddings per celtype per patiënt berekend, en trainden classificatiemodellen om ziekte te voorspellen. Wanneer nieuwe patiënten leken op degenen in de trainingsdata, was de prestatie uitstekend. Maar wanneer monsters uit volledig onafhankelijke studies met andere laboratoriummethoden kwamen, daalde de nauwkeurigheid sterk, wat aantoont hoe gevoelig dergelijke hulpmiddelen zijn voor technische variabiliteit. Een meer gecontroleerde "gecentraliseerde" dataset, gegenereerd in één centrum met één sequencing-chemie, herstelde veel van de prestaties, wat wijst op de noodzaak van gestandaardiseerde protocollen of zeer grote, diverse trainingssets.
Wat dit betekent voor toekomstige diagnose en behandeling
Voor leken is de kernboodschap dat uw circulerende immuuncellen een rijk vingerafdruk dragen van hoe uw lichaam ontstoken is. Door deze vingerafdrukken cel voor cel af te lezen, laat dit werk zien dat het mogelijk is om veel ziekten te onderscheiden, genen te ontdekken die specifieke symptomen kunnen aansturen en te beginnen met het bouwen van universele bloedtesten die ontstekingsziekten classificeren. De studie is nog geen kant-en-klare klinische test—technische verschillen tussen studies beperken de betrouwbaarheid—maar ze legt de basis voor toekomstige "liquid biopsy"-hulpmiddelen die artsen kunnen helpen de juiste diagnose en behandeling eerder vast te stellen met een eenvoudige bloedafname.
Bronvermelding: Jiménez-Gracia, L., Maspero, D., Aguilar-Fernández, S. et al. Interpretable inflammation landscape of circulating immune cells. Nat Med 32, 633–644 (2026). https://doi.org/10.1038/s41591-025-04126-3
Trefwoorden: ontsteking, immuuncellen, single-cell RNA sequencing, biomerkers, machine learning