Clear Sky Science · nl
Repotrectinib bij NTRK-fusie–positieve gevorderde solide tumoren: een fase 1/2‑onderzoek
Nieuwe hoop uit een gerichte kankerpil
Kankerbehandelingen worden steeds vaker ontworpen als precisiegereedschap in plaats van als botte instrumenten. Deze studie onderzoekt repotrectinib, een gerichte pil voor mensen wiens tumoren zeldzame genetische veranderingen dragen die NTRK‑fusies worden genoemd. Hoewel deze fusies bij minder dan 1 op de 100 solide tumoren voorkomen, kunnen ze in veel organen optreden — van long tot schildklier tot zacht weefsel — en reageren ze vaak dramatisch op speciaal ontwikkelde geneesmiddelen. Het probleem is dat eerdere medicijnen uiteindelijk stoppen met werken. Deze trial stelt een eenvoudige vraag met grote consequenties: kan een slimmer, volgende‑generatie geneesmiddel kanker voor langer onder controle houden, zelfs nadat andere gerichte therapieën zijn gefaald?
Een zeldzame maar krachtige kankerschakelaar
Sommige kankers worden aangedreven door fusies in genen die NTRK1, NTRK2 en NTRK3 heten. Deze fusies werken als vastgezette groeischakelaars in tumorcellen. Geneesmiddelen van de eerste generatie die de resulterende TRK‑eiwitten blokkeren, hebben al veel patiënten geholpen, maar na verloop van tijd leert de kanker ze vaak te ontwijken door nieuwe mutaties in de precieze bindingstas van het medicijn te verwerven. Repotrectinib is ontworpen om kleiner en compacter te zijn, zodat het zelfs na zulke veranderingen nog in die bindingstas kan passen. De internationale TRIDENT‑1‑trial testte dit middel bij volwassenen met gevorderde solide tumoren met NTRK‑fusies, waaronder mensen die nog nooit een TRK‑blokkerend middel hadden gekregen en zij wier kanker al was ontsnapt aan één of twee eerdere TRK‑remmers.
Wat de trial deed
Het onderzoek schreef 144 patiënten met NTRK‑fusie–positieve solide tumoren in bij centra wereldwijd; 120 van hen vormden de hoofdgroep voor het meten van werkzaamheid. Hun kankers besloegen minstens 18 verschillende typen, het vaakst niet‑kleincellige longkanker, schildklierkanker, tumoren van de speekselklier en zachte weefsel‑sarcomen. Allen hadden lokaal gevorderde of gemetastaseerde ziekte, en velen hadden al meerdere andere behandelingen geprobeerd, waaronder chemotherapie, immunotherapie of eerdere TRK‑remmers. Patiënten namen repotrectinib dagelijks oraal volgens een doseringsschema dat in een eerdere fase van de trial was vastgesteld. Onderzoekers volgden hoeveel patiënten een krimp van de tumor zagen, hoe lang die responsen duurden, hoelang patiënten leefden zonder verslechtering van de ziekte en hoe goed het middel werd verdragen.
Sterke en langdurige responsen
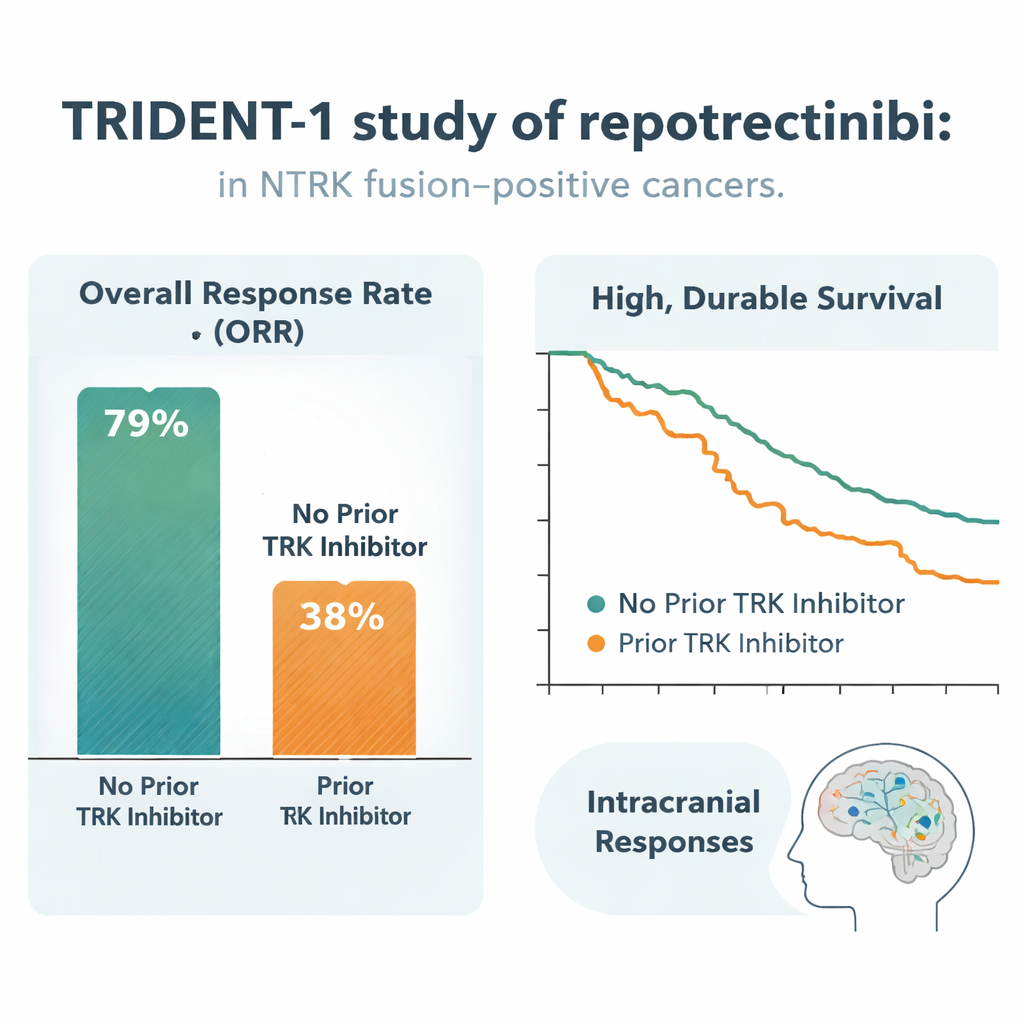
Onder 51 patiënten die nog nooit een TRK‑remmer hadden gekregen, had 59% een tumorkrimp die voldeed aan de criteria voor een objectieve respons, en 16% zag hun tumoren op scans verdwijnen. Reacties verschenen vaak snel — binnen ongeveer twee maanden — en waren opmerkelijk langdurig: na twee jaar profiteerde naar schatting 85% van de responders nog steeds, en ongeveer 60% van de hele groep had de ziekte nog niet zien verergeren. Zelfs in de zwaarder eerder behandelde groep van 69 patiënten wier kanker al was doorgebroken na een andere TRK‑remmer, reageerde 48% op repotrectinib, met een typische responsduur van ongeveer 10 maanden en ongeveer een kwart van de patiënten nog vrij van progressie na één jaar. Belangrijk is dat voordeel werd gezien over veel tumortypen heen en onafhankelijk van welk NTRK‑gen of fusiepartner betrokken was.
Bereiken van resistente en hersenziekte
Een belangrijke uitdaging voor TRK‑middelen zijn de zogenaamde solvent front‑mutaties, specifieke veranderingen in de drug‑bindingstas die eerdere middelen kunnen blokkeren. In deze trial droeg bijna de helft van de eerder behandelde patiënten dergelijke mutaties bij aanvang. Zelfs in deze moeilijk behandelbare subgroep had 53% een betekenisvolle tumorkrimp met repotrectinib, wat bevestigt dat het middel ten minste sommige vormen van resistentie kan overwinnen. De hersenen, een veelvoorkomende schuilplaats voor kanker, waren een andere focus. Onder patiënten met meetbare hersenmetastasen bij aanvang, hadden twee van de drie in de onbehandelde groep en vier van de zes in de eerder behandelde groep tumorafname in de hersenen, vaak vele maanden lang. Voor patiënten die zonder hersenbetrokkenheid begonnen, bleef de overgrote meerderheid vrij van nieuwe hersenlaesies tijdens follow‑up.
Bijwerkingen en wat het voor patiënten betekent
Over meer dan 500 mensen die met repotrectinib werden behandeld in deze en verwante cohorten, waren de meest voorkomende bijwerkingen duizeligheid, veranderde smaak en tintelingen, waarvan de meeste mild tot matig waren. Ernstiger behandelgerelateerde problemen, zoals bloedarmoede of verhoogde spier‑enzymwaarden, kwamen minder vaak voor, en slechts ongeveer 4% van de patiënten stopte met het middel vanwege bijwerkingen. Maatregelen van de algemene kwaliteit van leven bleven voor de meeste deelnemers stabiel of verbeterden gedurende vele behandelingscycli. Gezamenlijk tonen de resultaten aan dat repotrectinib duurzame controle kan bieden bij NTRK‑fusie–positieve kankers — inclusief die welke eerdere TRK‑middelen hebben weerstaan en die naar de hersenen zijn uitgezaaid — terwijl het over het algemeen verdraagbaar blijft. Voor patiënten met deze zeldzame maar agressieve tumoren ondersteunt de studie repotrectinib als een belangrijke nieuwe optie in het uitbreidende arsenaal van precisiekankertherapie.
Bronvermelding: Besse, B., Lin, J.J., Bazhenova, L. et al. Repotrectinib in NTRK fusion–positive advanced solid tumors: a phase 1/2 trial. Nat Med 32, 682–689 (2026). https://doi.org/10.1038/s41591-025-04079-7
Trefwoorden: gerichte kankertherapie, NTRK‑fusie, repotrectinib, weerstand tegen TRK‑remmers, hersenmetastasen