Clear Sky Science · nl
Gedeelde en specifieke bloedbiomarkers voor multimorbiditeit
Waarom veel aandoeningen tegelijk optreden
Naarmate mensen langer leven, komt het steeds vaker voor dat dezelfde persoon meerdere langdurige aandoeningen tegelijk heeft—zoals hartziekte, diabetes, longaandoeningen en geheugenverlies. Deze opeenstapeling van aandoeningen, multimorbiditeit genoemd, kan onafhankelijkheid en levenskwaliteit sterk aantasten. Toch weten artsen nog weinig over de onderliggende biologie die ervoor zorgt dat sommige oudere volwassenen veel ziekten opstapelen terwijl anderen relatief gezond blijven. Deze studie stelt een eenvoudige maar krachtige vraag: kunnen routinematige bloedtesten aangeven wie sneller meerdere ziekten ontwikkelt en welke biologische systemen dat proces aandrijven?
Een brede blik op verouderend bloed
Onderzoekers in Zweden bestudeerden 54 verschillende bloedmarkers bij meer dan 2.200 mensen van 60 jaar en ouder die tot 15 jaar werden gevolgd. De vrijwilligers maakten deel uit van de Swedish National Study on Aging and Care in Kungsholmen, waar deelnemers uitgebreide medische onderzoeken, geheugentests en bloedafnames ondergaan. De markers weerspiegelden een reeks processen die met veroudering samenhangen, waaronder ontsteking, stofwisseling, bloedvatengezondheid, orgaanschade en hersenafbraak. In plaats van zich op één ziekte te concentreren, telde het team alle langdurige aandoeningen per persoon, groepeerde mensen in veelvoorkomende “profielen” van gelijktijdige aandoeningen en mat hoe snel nieuwe aandoeningen in de loop van de tijd verschenen. 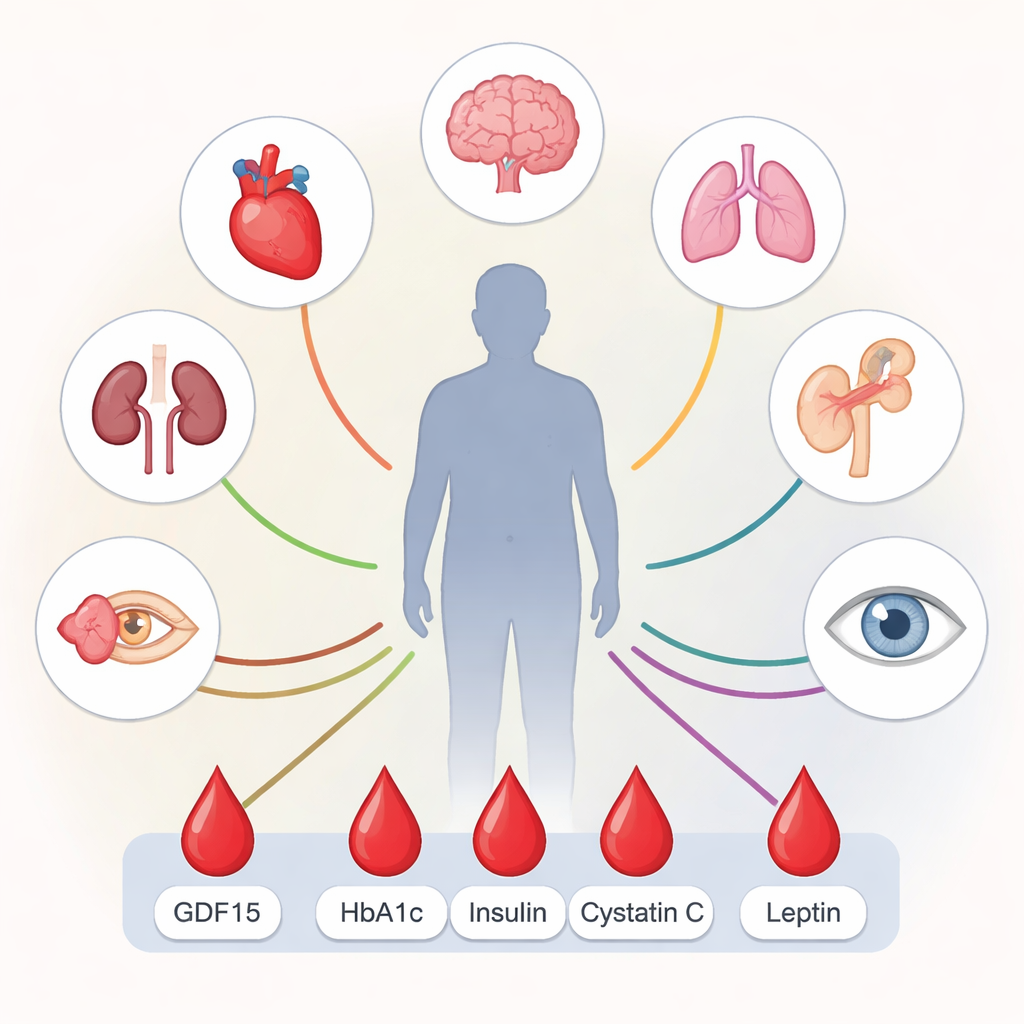
Vijf veelvoorkomende patronen van ziekte
Toen de onderzoekers keken naar hoe ziekten samenklonterden, vonden ze vijf hoofdpatronen onder mensen met minstens twee chronische aandoeningen. Een grote groep had geen bijzonder dominante combinatie van ziekten (“Unspecific”), terwijl andere groepen werden gedomineerd door hersen‑ en psychische aandoeningen (“Neuropsychiatric”), stemmings- en longproblemen (“Psychiatric and Respiratory”), gehoor‑ en gezichtsverlies plus bloedarmoede (“Sensory impairment and Anemia”), of hart‑ en metabole aandoeningen zoals diabetes en hoge bloeddruk (“Cardiometabolic”). Deze patronen verschilden in leeftijd, beperking, cognitieve functies en medicijngebruik, en ze voorspelden ook latere uitkomsten: het Neuropsychiatric‑patroon ging bijvoorbeeld gepaard met een hoger risico op dementie en overlijden, terwijl het Cardiometabolic‑patroon sterk toekomstige hartproblemen voorspelde.
Metabolisme blijkt de belangrijkste motor
Over alle manieren waarop het team multimorbiditeit mat—de eenvoudige ziektenaantalmethode, de vijf patronen en de lange termijnsnelheid van ziekteopbouw—bleef dezelfde kleine groep bloedmarkers opvallen. Hogere niveaus van growth differentiation factor 15 (GDF15), hemoglobine A1c (een maat voor langetermijnbloedglucose), cystatine C (gekoppeld aan nierfunctie), leptine (een hormoon uit vetweefsel) en insuline waren allemaal geassocieerd met meer ziekten bij aanvang en met het behoren tot elk van de multimorbiditeitspatronen. Verschillende van deze markers, samen met een leverenzym genaamd gamma‑glutamyltransferase, voorspelden ook een snellere toename van nieuwe aandoeningen over 15 jaar. Daarentegen was een hoger albumine—een eiwit dat goede voeding en algemene gezondheid weerspiegelt—geassocieerd met een langzamere ziekteopbouw. Samen wijzen deze resultaten op verstoorde stofwisseling en energiehuishouding, nauw verweven met laaggradige ontsteking, als een centrale motor van multimorbiditeit.
Gedeelde wortels en specifieke signaturen
Niet alle ziektepatronen waren biologisch identiek. Terwijl sommige markers bij alle patronen voorkwamen, waren andere specifieker. Neurofilament light chain—een marker voor schade aan zenuwvezels—was bijvoorbeeld sterk gekoppeld aan het Neuropsychiatric‑profiel, in lijn met zijn verband met hersenschade. Een structureel hartproteïne genaamd N‑cadherin was sterker verbonden met het Cardiometabolic‑patroon. Het Unspecific‑patroon liet daarentegen geen duidelijke unieke biomarker‑vingerafdruk zien, wat suggereert dat het kan voortkomen uit meer algemene verouderingsprocessen. De onderzoekers bevestigden ook hun belangrijkste bevinding—dat een kleine set metabole markers de snelheid van ziekteopbouw voorspelt—door hetzelfde model te testen in een tweede, onafhankelijke groep ouderen uit de langdurige Baltimore Longitudinal Study of Aging in de Verenigde Staten. 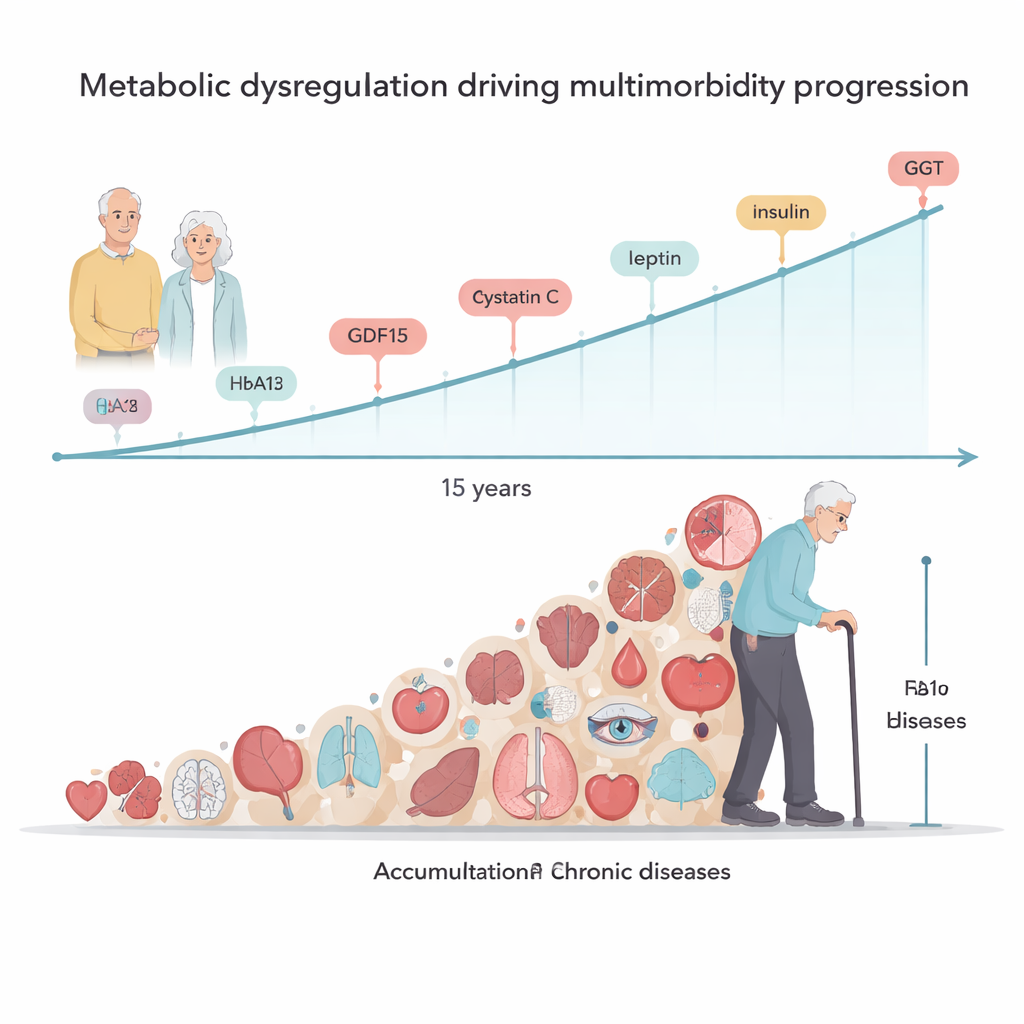
Wat dit betekent voor gezond ouder worden
Voor niet‑specialisten is de kernboodschap dat veel verschillende chronische aandoeningen op latere leeftijd gemeenschappelijke biologische wortels lijken te hebben, vooral in hoe het lichaam suiker en energie verwerkt en hoe organen reageren op langdurige, laaggradige ontsteking. De studie bewijst niet dat deze bloedmarkers ziekte veroorzaken, maar toont wel dat ze kunnen helpen mensen te signaleren wier lichaam onder grotere “metabole stress” staat en die waarschijnlijk in de loop van de tijd meer aandoeningen zullen opstapelen. Op de lange termijn kan deze onderzoekslijn nieuwe strategieën ondersteunen—variërend van leefstijlaanpassingen tot medicijnen die oorspronkelijk voor diabetes zijn ontwikkeld—die het verouderingsproces zelf aanpakken in plaats van elke ziekte afzonderlijk te behandelen, met als doel de algehele ophoping van gezondheidsproblemen op latere leeftijd te vertragen.
Bronvermelding: Ornago, A.M., Gregorio, C., Triolo, F. et al. Shared and specific blood biomarkers for multimorbidity. Nat Med 32, 736–745 (2026). https://doi.org/10.1038/s41591-025-04038-2
Trefwoorden: multimorbiditeit, veroudering, bloedbiomarkers, metabole gezondheid, preventie van chronische ziekten