Clear Sky Science · nl
Flt3L-gemedieerde uitbreiding van tumor cDC1 verbetert immunotherapie door priming van stamachtige CD8+-T-cellen in lymfeklieren
Helpen van het immuunsysteem herinneren hoe het kanker moet bestrijden
Waarom verdwijnen bij sommige mensen tumoren met moderne immunotherapie terwijl anderen weinig baat hebben? Deze studie kijkt onder de motorkap van het immuunsysteem om die vraag te beantwoorden. De onderzoekers tonen aan dat door een specifieke groep wachters in tumoren te versterken, ze een reservoir kunnen opbouwen van langlevende ‘‘stamachtige’’ cytotoxische T‑cellen in nabijgelegen lymfeklieren. Die cellen laten op hun beurt standaard checkpointmiddelen, vooral anti‑CTLA‑4‑therapie, harder en langer werken.
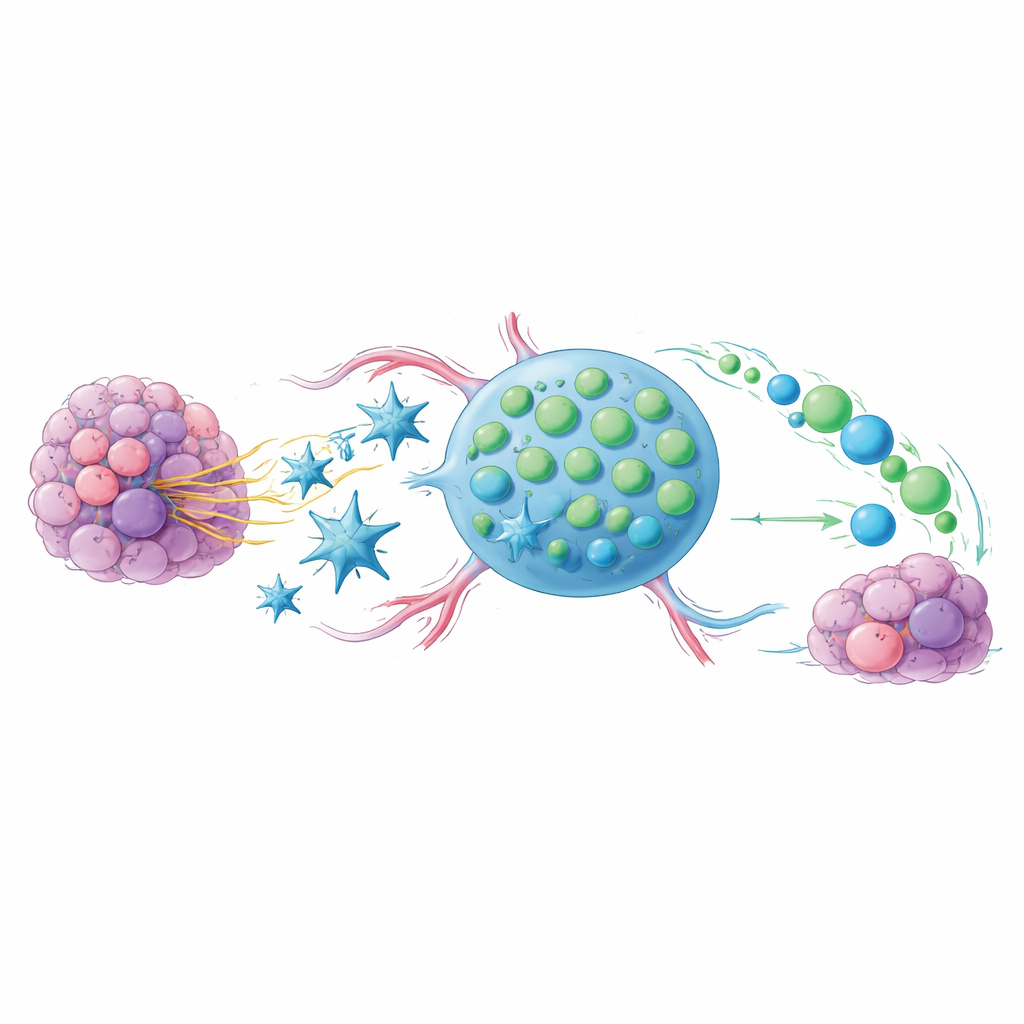
Het probleem van uitgeputte tumorbestrijdende cellen
Checkpointmiddelen zoals anti‑PD‑1 en anti‑CTLA‑4 zetten immuuncellen los tegen kanker, maar ze werken slechts goed bij een deel van de patiënten. Een aanwijzing ligt in de toestand van CD8‑T‑cellen, de belangrijkste moordenaars van geïnfecteerde of kankercellen. Wanneer deze T‑cellen te lang en te intensief geprikkeld worden, glijden ze in een versleten, ‘‘uitgeputte’’ toestand en stoppen ze met effectief vermenigvuldigen. Een kleinere subset behoudt echter een jeugdigere, stamachtige karakter: ze delen gemakkelijk, scheppen nieuwe strijders en hangen sterk samen met goede responsen bij mensen die checkpoint‑therapie ontvangen. De centrale vraag van dit werk is hoe men tumoren en hun omgeving kan sturen om deze stamachtige cellen te bevoordelen boven hun uitgebluste tegenhangers.
Het superchargen van de tumorwachters
Het team richtte zich op conventionele type 1 dendritische cellen, een zeldzame maar krachtige klasse van immuunwachters die uitblinken in het presenteren van tumorfragmenten aan T‑cellen. Ze gebruikten een groeisignaal genaamd Flt3‑ligand (Flt3L) om deze cellen in muizen tumoren uit te breiden, hetzij door de kankercellen zo te ontwerpen dat ze het afscheiden, hetzij door het als geneesmiddel toe te dienen. Single‑cell RNA‑sequencing toonde aan dat Flt3L‑rijke tumoren veel meer dendritische cellen en lymfocyten en minder tumorcellen bevatten. Binnen het dendritische compartiment namen drie verschillende groepen toe, waaronder één die zeer volgroeid was en klaar om naar lymfeklieren te migreren, waar T‑cellen voor het eerst worden getraind. Tegelijkertijd verschoven CD8‑T‑cellen in deze tumoren weg van een terminal uitgeput profiel naar een stam‑ of geheugenachtig stadium.
Een stamachtige T‑celreservoir opbouwen in lymfeklieren
Door tumor‑specifieke T‑cellen te volgen en genetische hulpmiddelen te gebruiken, lieten de onderzoekers zien dat Flt3L‑behandeling een populatie CD8‑T‑cellen versterkt die oppervlaktekenmerken dragen geassocieerd met stamachtige potentie en actieve deling. Deze cellen waren afhankelijk van XCR1‑positieve dendritische cellen en van CCR7‑geleid transport van dendritische cellen van de tumor naar de afvoerende lymfeklier. Wanneer dendritische cellen werden uitgeput of hun migratie geblokkeerd, kromp het stamachtige T‑celbestand. Het blokkeren van lymfocytuitgang uit lymfeklieren had een vergelijkbaar effect, waardoor de toevoer van vernieuwde T‑cellen naar de tumor werd afgesneden. Moleculaire profilering toonde aan dat dit proces afhankelijk was van de transcriptiefactor Myb en bevoordeelde T‑cellen met relatief zwakke herkenning van tumordoelen, een type dat steeds meer wordt erkend als belangrijk voor duurzaam kankergedragbeheer.
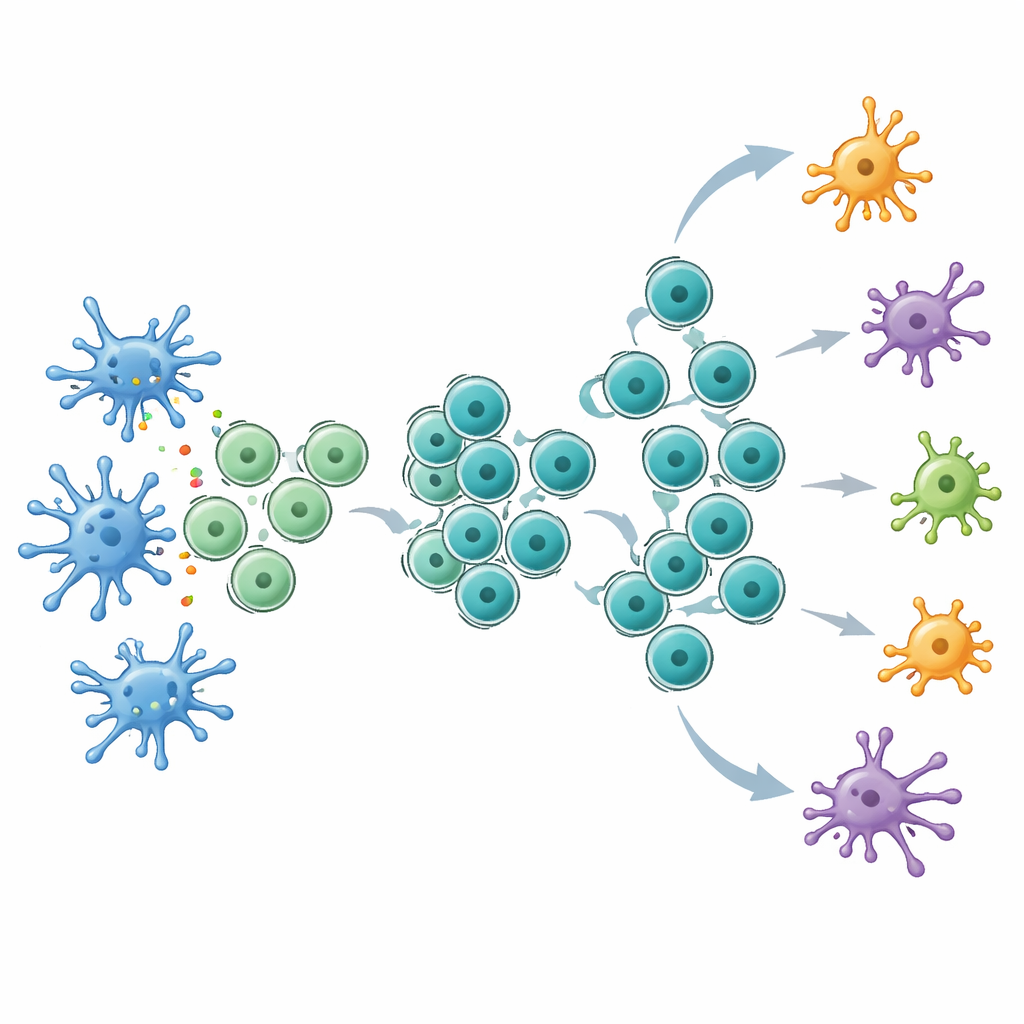
Checkpoint‑therapie zwaarder laten werken
Gewapend met dit uitgebreide reservoir van stamachtige T‑cellen reageerden de muizen veel beter op checkpoint‑blokkade, met name anti‑CTLA‑4‑behandeling. Tumoren bij Flt3L‑behandelde dieren krimpten sterker, de overleving verbeterde en het bloed en de lymfeklieren bevatten meer tumor‑specifieke T‑cellen. Binnen tumoren verhoogde Flt3L het aantal stamachtige CD8‑cellen, terwijl daaropvolgende CTLA‑4‑blokkade deze cellen leek te stimuleren om uit te rijpen tot krachtige effectoren die hoge niveaus van belangrijke anti‑tumormoleculen produceerden. Sequencing van T‑celreceptoren toonde aan dat de combinatietherapie het spectrum aan T‑celklonen vergrootte dat expandeerde, inclusief veel subdominante, wat wijst op een diversere aanval op de kanker. Gedetailleerde single‑cellanalyse ontdekte een unieke CD8‑T‑celcluster, gemarkeerd door expressie van de receptor voor de immuunboodschapper IL‑21, die zich bevond tussen stamachtige en uitgeputte toestanden en T‑celreceptoren deelde met zowel vroege als late populaties. Het blokkeren van IL‑21‑signaal verzwakte de voordelen van het combineren van Flt3L met anti‑CTLA‑4.
Wat dit betekent voor toekomstige kankerbehandelingen
Voor een niet‑specialistische lezer is de boodschap dat succesvolle immunotherapie niet alleen afhangt van het harder stimuleren van het immuunsysteem, maar van het hebben van het juiste type cellen om te stimuleren. Dit werk laat zien dat het voeden en sturen van dendritische cellen met Flt3L nabijgelegen lymfeklieren kan vullen met een hernieuwbare voorraad stamachtige cytotoxische T‑cellen. Wanneer vervolgens checkpointmiddelen zoals anti‑CTLA‑4 worden toegepast, kunnen ze op dit reservoir terugvallen om golven van nieuwe strijders te genereren die talrijker, diverser en beter in staat zijn tumoren onder controle te houden. Analyses van menselijke kankerdatasets suggereren dat de genhandtekeningen die aan deze route zijn gekoppeld ook betere uitkomsten bij patiënten voorspellen. Gezamenlijk wijzen deze bevindingen op combinatietherapieën die eerst de juiste immuuncel ‘‘zaadvoorraad’’ opbouwen met middelen zoals Flt3L, en deze vervolgens vrijlaten met checkpointmiddelen voor krachtigere en duurzamere kankercontrole.
Bronvermelding: Lai, J., Chan, C.W., Armitage, J.D. et al. Flt3L-mediated tumor cDC1 expansion enhances immunotherapy by priming stem-like CD8+ T cells in lymph nodes. Nat Immunol 27, 530–542 (2026). https://doi.org/10.1038/s41590-026-02419-4
Trefwoorden: kankerimmunotherapie, dendritische cellen, stamachtige CD8 T-cellen, checkpoint-blokkade, Flt3-ligand