Clear Sky Science · nl
CD38 geeft lokale antigeenspecifieke Treg-cellen stressbestendigheid voor beheersing van gecompartimenteerde ontsteking in het CZS
Waarom immuuncellen die de hersenen beschermen ertoe doen
Veel auto-immuunziekten van de hersenen, zoals multiple sclerose, gedragen zich als smeulende branden: een aanvankelijke uitbarsting van ontsteking neemt af, maar schade kan jaren later weer oplaaien. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote implicaties: na een aanval in het centraal zenuwstelsel (CZS), wat houdt de vrede — en wat kantelt het evenwicht weer richting ziekte? De auteurs richten zich op een kleine populatie immuuncellen, zogenaamde regulatorische T-cellen, die zich na ontsteking in de hersenen en het ruggenmerg vestigen, en onthullen hoe één oppervlakte-eiwit hen in staat stelt te overleven in een vijandige omgeving en terugvallen te voorkomen.
Immuunvredebewakers die achterblijven
Met een muismodel dat aspecten van multiple sclerose nabootst, volgden de onderzoekers verschillende typen T-cellen terwijl de ziekte een piek bereikte en vervolgens in een herstelfase kwam. Terwijl gewone helper-T-cellen die ontsteking aanjagen in aantal afnamen naarmate de symptomen verbeterden, bleven regulatorische T-cellen — gespecialiseerde cellen die normaal immuunreacties dempen — in het CZS aanwezig. Hun relatieve aandeel binnen de lokale T-celpopulatie nam zelfs toe, en ze groeperen zich in specifieke niches rond hersenvloeistofruimtes en de beschermende membranen rond de hersenen. Door te labelen waar binnenkomende T-cellen vandaan kwamen, toonde het team aan dat na herstel zeer weinig nieuwe regulatorische T-cellen uit lymfeklieren arriveerden. In plaats daarvan onderhield de CZS-populatie zich grotendeels lokaal, wat wijst op een langetermijn residentie-‘vredehandhavingsmacht’. 
Stressbestendige bewakers van een vijandige niche
Het post-inflammatoire CZS is allesbehalve comfortabel voor deze bewakers. Na de hoofdgolf van ziekte dalen de niveaus van het groeisignaal interleukine-2 (IL-2) — waarop regulatorische T-cellen sterk vertrouwen — omdat de meeste conventionele T-cellen zijn teruggetrokken. Tegelijk bevat het weefsel veel van het metabole molecuul NAD+, dat celdood kan uitlokken of belangrijke oppervlaktereceptoren kan verzwakken wanneer het door een specifiek enzym wordt aangepast. Door individuele regulatorische T-cellen genetisch te markeren en te volgen, onderscheidden de auteurs ‘stabiele’ cellen die hun identiteit behielden van ‘onstabiele’ cellen die hun kenmerkende Foxp3-programma verloren. Stabiele cellen vertoonden een veel sterker IL-2-signatuursignaal en hogere niveaus van IL-2-receptoren, wat suggereert dat het vermogen om schaarse IL-2 te detecteren cruciaal is voor overleven in deze gestreste omgeving.
Lokale controle van terugvallen vanuit binnenin de hersenen
Om te testen of deze residente regulatorische T-cellen werkelijk belangrijk zijn voor langdurige ziektecontrole, verwijderden de onderzoekers ze selectief uit het CZS met een toxine dat direct in de hersenvloeistof werd toegediend, terwijl de meeste systemische regulatorische T-cellen elders in het lichaam intact bleven. Binnen enkele dagen ontwikkelden muizen die herstelden ernstige terugvallen met hernieuwde verlamming. Ter vergelijking: het ruimten van regulatorische T-cellen alleen in het lichaam, met behoud van die in het CZS, veroorzaakte geen oplevingen. De terugval betrof snelle heractivering en expansie van effector-T-cellen die al in het CZS aanwezig waren, zelfs wanneer hun recrutering uit het bloed was geblokkeerd. Dit toont aan dat lokale regulatorische T-cellen, en niet circulerende, essentieel zijn om agressieve restcellen die na de acute aanval achterblijven te remmen.
Hoe één enzym regulatorische cellen beschermt
Verder gravend zochten de auteurs naar moleculen die stressbestendige CZS-regulatorische T-cellen onderscheiden. Een sleutelspeler dook op: CD38, een enzym op het celoppervlak dat extracellulair NAD+ afbreekt. In het ontstoken CZS verhoogden regulatorische T-cellen sterk hun CD38-expressie, terwijl conventionele T-cellen niet zo’n uitgesproken verschuiving lieten zien. Toen het team myeline-reactieve regulatorische T-cellen zonder CD38 in muizen transfereerde, bereikten deze cellen het CZS maar faalden ze in het controleren van de ziekte, in tegenstelling tot hun normale tegenhangers. In gemengde chimerische dieren, waarin alleen de residentiële regulatorische T-cellen CD38-deficiënt waren, was het verwijderen van de CD38-rijke fractie voldoende om terugvallen uit te lokken, wat laat zien dat CD38 cell-intrinsiek werkt om effectieve controle mogelijk te maken.
De levenslijnsignal beschermen
Mechanistische experimenten lichten toe hoe CD38 deze veerkracht verleent. Hoge NAD+-niveaus in het CZS kunnen chemische modificatie van oppervlakte-eiwitten door het enzym ARTC2.2 aanjagen. Eén gevoelige target is de hoge-affiniteitssubunit van de IL-2-receptor, die regulatorische T-cellen zeer sterk tot expressie brengen, vooral wanneer ze hersenantigenen herkennen. In CD38-deficiënte regulatorische T-cellen die aan NAD+ werden blootgesteld, raakten de meeste IL-2-receptoren gemodificeerd, wat leidde tot zwakkere activatie van de downstream boodschapper STAT5 en verminderde responsiviteit op IL-2. In contrast verlaagden CD38-expressieve cellen lokaal het NAD+ rond zichzelf, waardoor deze schadelijke modificatie werd beperkt en sterke IL-2-signalisatie behouden bleef. In levende muizen leidde het injecteren van NAD+ in de hersenen selectief tot het doden van de meeste regulatorische T-cellen via dit pad, terwijl conventionele T-cellen werden ontzien, wat onderstreept hoe precair de niche is zonder dit beschermende enzym. 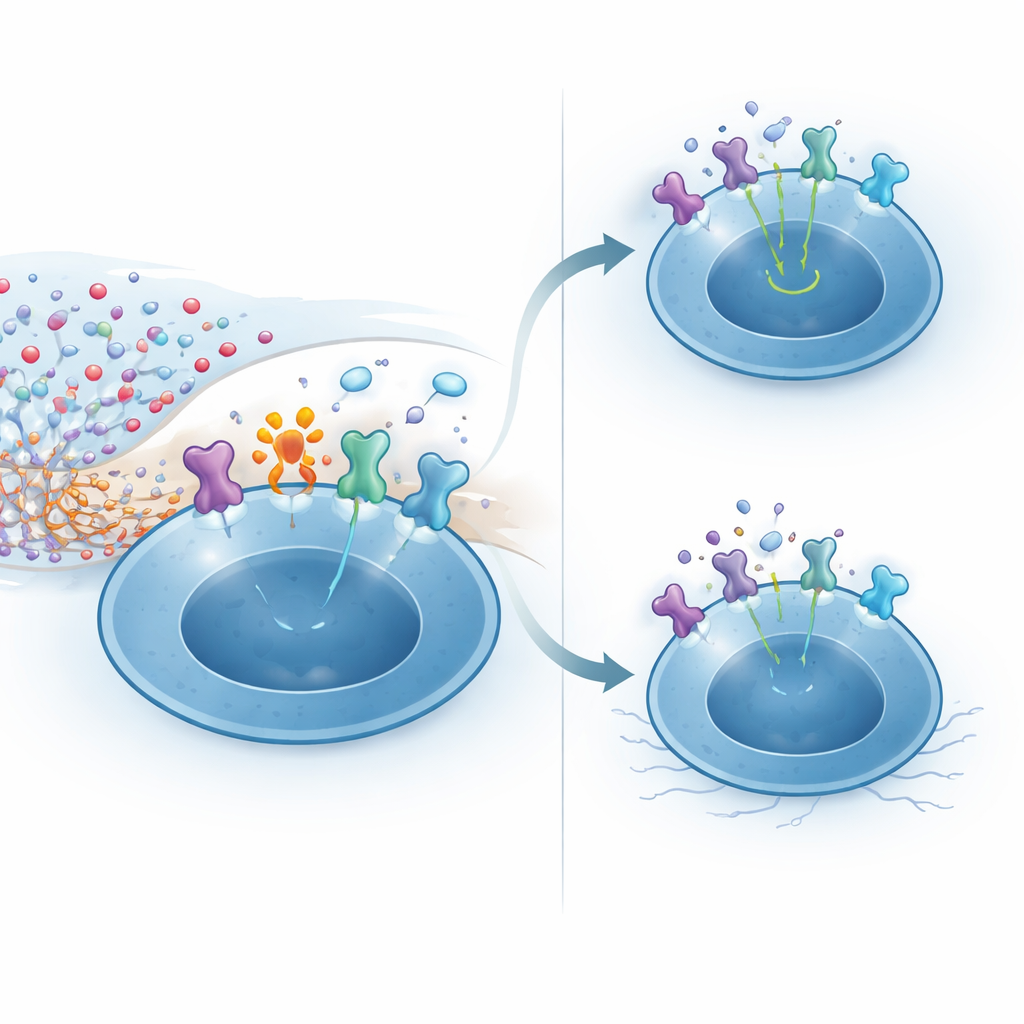
Wat dit betekent voor chronische auto-immuniteit van de hersenen
Dit werk schetst een beeld van chronische CZS-auto-immuniteit als een gecompartimenteerde strijd: kleine clusters van resterende agressieve T-cellen huizen in de hersenen en het ruggenmerg en worden in toom gehouden door even gespecialiseerde lokale regulatorische T-cellen. Deze bewakers zijn ‘stressbestendig’ omdat CD38 hen in staat stelt hoge NAD+-niveaus te weerstaan en geringe hoeveelheden IL-2 te blijven waarnemen, waardoor ze hun identiteit en onderdrukkende functie behouden. Voor niet-specialisten is de kernboodschap dat de langetermijncontrole van ziekten zoals multiple sclerose mogelijk minder afhangt van het circulerende immuunsysteem en meer van het koesteren en beschermen van deze residentiële vredehandhavers binnen de hersenen — bijvoorbeeld door routes te richten die CD38-functie of IL-2-gevoeligheid in regulatorische T-cellen versterken.
Bronvermelding: Chen, HH., Tyystjärvi, S., Ruiz Navarro, D. et al. CD38 endows local antigen-specific Treg cells with stress resilience for control of compartmentalized CNS inflammation. Nat Immunol 27, 516–529 (2026). https://doi.org/10.1038/s41590-025-02416-z
Trefwoorden: regulatorische T-cellen, multiple sclerose, ontsteking van het centraal zenuwstelsel, CD38-enzym, immuun tolerantie