Clear Sky Science · nl
Een GDF-15–GFRAL-as reguleert auto-immuun T-celresponses tijdens neuroinflammatie
Waarom zwangerschap een haperend immuunsysteem kan kalmeren
Artsen merkten al lange tijd een medisch raadsel op: veel vrouwen met multiple sclerose, een ziekte waarbij het immuunsysteem de hersenen en het ruggenmerg aanvalt, voelen zich tijdens de zwangerschap vaak beter. Hun opvlammingen nemen sterk af, om na de bevalling weer terug te keren. Deze studie onthult een belangrijke schakel in dat puzzelstuk: een signaal dat van het lichaam naar een klein hersengebied stroomt en terug naar het immuunsysteem, waardoor schadelijke immuunaanvallen worden afgezwakt zonder de afweer volledig uit te schakelen. 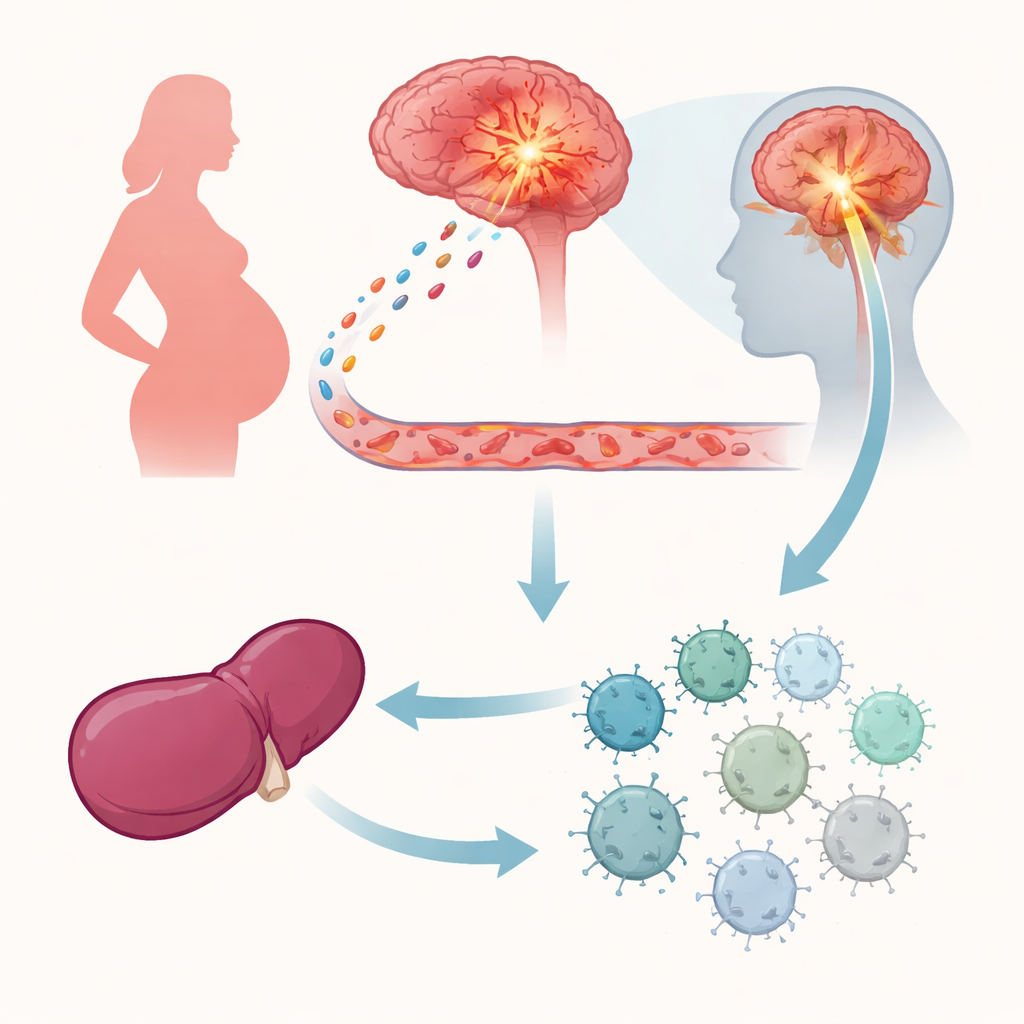
Een boodschapper die stijgt tijdens zwangerschap en hersenziekte
De onderzoekers richtten zich op een eiwit genaamd GDF-15, dat in het bloed circuleert. Ze bepaalden de GDF-15-spiegels bij zwangere vrouwen en bij muizen en ontdekten dat dit molecuul gedurende de zwangerschap gestaag toeneemt. Vrouwen met multiple sclerose die tijdens de zwangerschap vrij van terugvallen bleven, hadden hogere GDF-15-niveaus dan zij die opvlammingen ervoeren. Bij muizen met genetisch verschillende nakomelingen stegen de GDF-15-spiegels bijzonder sterk, en lagere niveaus waren gekoppeld aan kleinere nestgroottes, wat suggereert dat dit eiwit helpt het lichaam van de moeder te tolereren dat de foetus deels ‘vreemd’ is.
Wanneer de hersenen ontsteken, wordt het signaal sterker
Het team onderzocht vervolgens wat er gebeurt tijdens experimentele neuroinflammatie, een muismodel van multiple sclerose. In deze dieren begonnen cellen in de hersenen en het ruggenmerg grote hoeveelheden GDF-15 te produceren precies ter plaatse van de ontstekingen. Ook geïnvadeerde immuuncellen in het centrale zenuwstelsel droegen bij aan deze toename. Muizen die GDF-15 misten werden zieker, herstelden slechter en toonden agressievere hersenimmuuncellen, wat suggereert dat het molecuul normaal gesproken fungeert als een rem om ontsteking te helpen oplossen in plaats van deze te voorkomen.
Hersenenstam als ‘schakelbord’ stuurt kalmerende signalen naar de milt
GDF-15 kan alleen signalen activeren door te binden aan een specifieke sensor genaamd GFRAL, die vrijwel uitsluitend voorkomt op neuronen in een klein gebied van de hersenstam dat buiten de gebruikelijke bloed-hersenbarrière ligt. De wetenschappers gebruikten gentherapie en eiwitinjecties om GDF-15 bij muizen te verhogen en ontdekten dat dit krachtig beschermde tegen neuroinflammatie, zelfs nadat de ziekte al was begonnen, zonder afhankelijk te zijn van stresshormonen of eenvoudigweg gewichtsverlies. Wanneer GFRAL ontbrak, of wanneer een mutant van GDF-15 werd gebruikt dat niet langer aan die receptor kon binden, verdween de bescherming. Het direct activeren van GFRAL-positieve neuronen, met een chemogenetisch hulpmiddel waarmee onderzoekers cellen met een ontworpen medicijn kunnen aanzetten, was op zichzelf al voldoende om te voorkomen dat immuuncellen het ruggenmerg binnenstroomden. 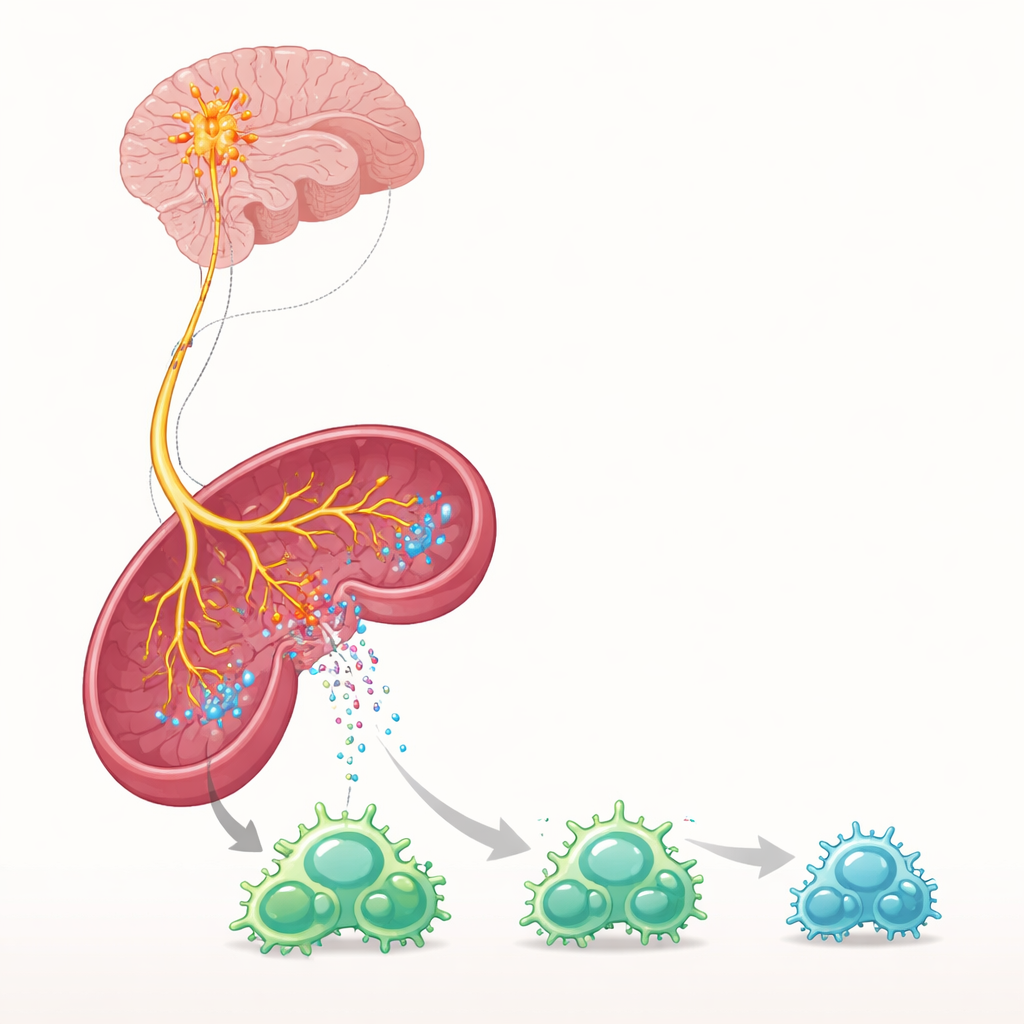
Hoe zenuwsignalen T-cellen hervormen
Om te begrijpen hoe een kleine groep neuronen een grote immuunrespons kon beheersen, volgde het team hun effecten tot in de milt, een belangrijk knooppunt voor immuuncellen. Het verhogen van GDF-15 of het stimuleren van GFRAL-positieve neuronen vergrootte de activiteit van sympathische zenuwvezels in de milt en verhoogde de niveaus van noradrenaline, een chemische boodschapper die bekender is door zijn rol in de ‘vecht-of-vlucht’-reactie. Toen milt-T-cellen werden blootgesteld aan noradrenaline of vergelijkbare middelen, deelden ze minder, toonden ze zwakkere activeringsmarkers en verminderde niveaus van belangrijke oppervlakte‑‘grip’-eiwitten die hen normaal helpen aan vaatwanden te hechten en het centrale zenuwstelsel binnen te dringen. In levende dieren vertaalde dit zich naar minder geactiveerde T-cellen in lymfoïde organen en aanzienlijk minder immuuncellen die de hersenen en het ruggenmerg bereikten.
Een nieuw brein‑immuuncircuit met therapeutisch potentieel
Samen genomen onthullen de bevindingen een fijn afgestemd circuit: zwangerschap of weefselstress verhoogt GDF-15, dit signaal bereikt GFRAL-expressieve neuronen in de hersenstam, die neuronen activeren sympathische zenuwen naar de milt, en noradrenaline temt vervolgens potentieel schadelijke T-cellen door hun activatie, groei en vermogen om de hersenen binnen te dringen te beperken. In plaats van de immuniteit breed te onderdrukken, koelt deze route selectief auto-immuunaanvallen af. Omdat medicijnachtige versies van GDF-15 en hulpmiddelen die de receptor richten al zijn getest voor andere aandoeningen, biedt deze nieuw in kaart gebrachte brein‑immuunas een veelbelovende weg naar toekomstige therapieën voor multiple sclerose en mogelijk andere auto-immuunziekten.
Bronvermelding: Sonner, J.K., Kahn, A., Binkle-Ladisch, L. et al. A GDF-15–GFRAL axis controls autoimmune T cell responses during neuroinflammation. Nat Immunol 27, 503–515 (2026). https://doi.org/10.1038/s41590-025-02406-1
Trefwoorden: multiple sclerose, neuro-inflammatie, immuuntolerantie, neuro-immuun circuit, GDF-15