Clear Sky Science · nl
Fijnafstelling van BACH2-dosering balanceert stamheid en effectorfunctie om antitumor T-celtherapie te verbeteren
Helpen dat kankebestrijdende cellen langer blijven bestaan
Veel van de meest veelbelovende kankerbehandelingen van vandaag vertrouwen op versnelde versies van de eigen immuuncellen van het lichaam. Toch raken deze geïnengineerde T-cellen vaak te snel vermoeid in tumoren, wat hun effectiviteit beperkt. Deze studie onderzoekt een manier om kankebestrijdende T-cellen langer te laten voortbestaan zonder hun dodelijke capaciteit te verminderen, door zorgvuldig de activiteit van één controlesignaal binnen de cellen af te stemmen.
Waarom immuuncellen zowel jeugd als kracht nodig hebben
Ons immuunsysteem berust op een taakverdeling. Sommige T-cellen fungeren als robuuste, stamachtige "zaad"cellen die lang leven en nieuwe strijders kunnen blijven voortbrengen. Andere worden kortlevende "soldaat"cellen die het grootste deel van de directe tumordoding uitvoeren maar snel uitgeput raken. Effectieve kankertherapie heeft beide nodig: een duurzaam reservoir van zaden en een constante aanvoer van soldaten. Bij chronische infecties en tumoren glijden veel T-cellen echter weg in een uitgeput, terminaal stadium waarin ze niet meer kunnen vermenigvuldigen of goed reageren op behandeling. Klinische resultaten met bestaande T-celtherapieën tonen aan dat patiënten beter af zijn wanneer de geïnfuseerde cellen meer van de stamachtige subset bevatten en langer in het lichaam blijven bestaan.
Een moleculaire knop voor T-celrust en activiteit
De onderzoekers richtten zich op een eiwit genaamd BACH2, dat helpt T-cellen in een rustende, geheugenachtige staat te houden. In natuurlijke immuunreacties zijn BACH2-niveaus hoog in naïeve en stamachtige T-cellen en dalen ze zodra cellen volledig bewapende moordenaars worden. Eerder werk toonde aan dat BACH2 beschermt tegen overactivatie en zelfs als tumoronderdrukker functioneert in geïnengineerde T-cellen, wat het een aantrekkelijk maar lastig hulpmiddel maakt: te veel rust kan cellen te slaperig maken om kanker te bestrijden. Toen het team T-cellen dwong grote hoeveelheden BACH2 te produceren, gebeurde precies dat. De cellen bleven in een quiescente, stamachtige toestand, toonden minder activeringsmarkers, produceerden weinig van de toxische moleculen die nodig zijn om tumorcellen te doden en controleerden tumoren slecht bij muizen.
Het vinden van de "precies-juiste" dosis
Om te onderzoeken of BACH2 kon helpen in plaats van hinderen wanneer op het juiste niveau ingesteld, bouwden de auteurs genetische constructen die slechts een klein deel van de gebruikelijke overexpressie produceren—ongeveer zoveel BACH2 als in gezonde geheugen-T-cellen wordt aangetroffen. Ze bevestigden deze doses door het eiwit te taggen en door massaspectrometrie te gebruiken om het aantal kopieën te tellen. Met dit laagdosesysteem in handen stimuleerden ze muis-T-cellen herhaaldelijk in cultuur om de chronische stress van een tumor na te bootsen. Zowel hoge als lage BACH2 verminderden de opkomst van terminaal uitgeputte cellen en behielden markers geassocieerd met stamachtig gedrag. Het cruciale verschil was dat laaggedoseerde BACH2 de cellen in staat stelde sterke productie van sleutelcytokinen en enzymen te behouden, terwijl hoge BACH2 deze effectorfuncties scherp onderdrukte en zelfs de celgrootte verminderde, een teken van slechte activatie.
Op moleculair niveau vonden de onderzoekers dat BACH2 werkt door te concurreren met een familie van activator-eiwitten die gezamenlijk bekendstaan als AP-1 op specifieke DNA-motieven. Genen die sterk afhankelijk zijn van AP-1 bevatten veel van deze motieven en waren bijzonder gevoelig voor BACH2. Hoge BACH2 verdrong AP-1 vrijwel volledig van deze sites, waardoor veel effectorgenen werden uitgeschakeld. Lage dosis BACH2 verminderde AP-1-binding slechts gedeeltelijk, waardoor selectief genen werden gedempt die terminale uitputting aandrijven terwijl een groot deel van het nuttige effectorprogramma gespaard bleef. In tumoren stapelden T-cellen die met lage dosis BACH2 waren geconstrueerd zich beter op, behielden zowel stamachtige als meer gedifferentieerde subsets en produceerden meer cytokine-producerende cellen per gram tumor, wat leidde tot duidelijk verbeterde controle van melanoom en colorectale kankers in muismodellen. 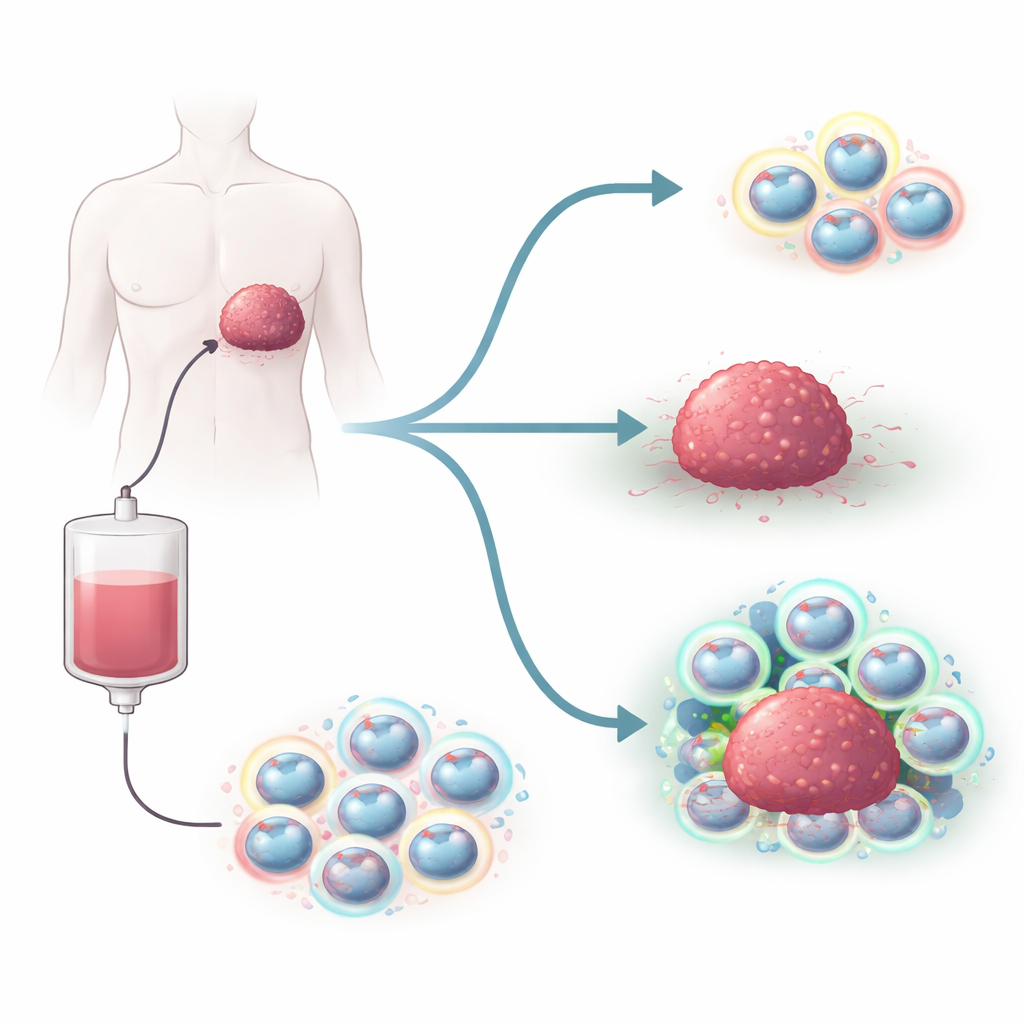
Het creëren van hybride T-cellen die volhouden en aanvallen
Door T-cellen te onderzoeken die wel of niet een oppervlaktemarker tot expressie brachten die aan stamachtig gedrag gekoppeld is, toonden de onderzoekers aan dat laaggedoseerde BACH2 de meest gedifferentieerde, uitgeputte cellen hervormde tot een hybride toestand. Deze cellen verworven geselecteerde kenmerken van stamachtige T-cellen—zoals genen geassocieerd met langdurigheid en homing—terwijl ze kernkenmerken van actieve effectors behielden, waaronder krachtige cytokineproductie en proliferatie. Met andere woorden, in plaats van alle cellen in een stille stamtoestand te dwingen, verhoogde dosisafgestelde BACH2 een ondergrens van zelfvernieuwing en terughoudendheid, vooral in cellen die anders zouden opbranden. 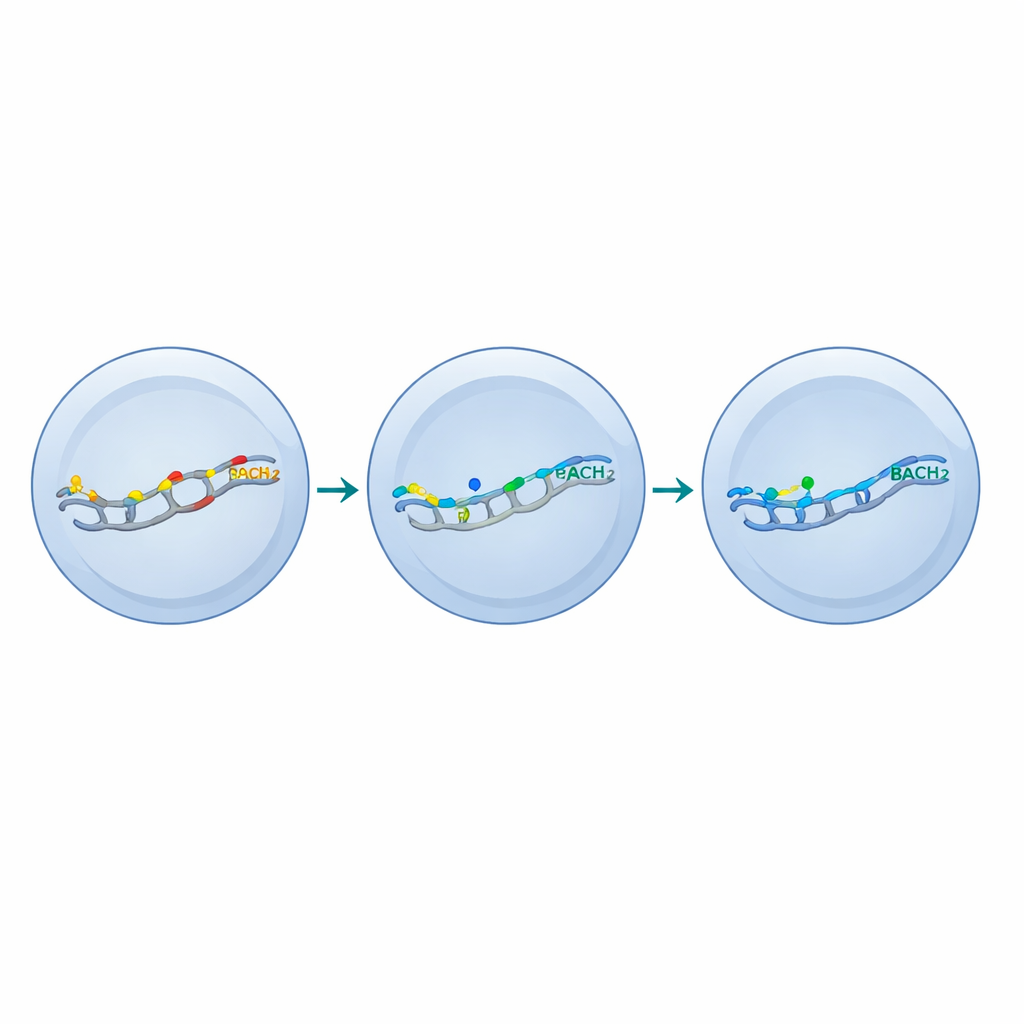
Een bredere strategie voor veiliger, sterkere celtherapieën
Om te testen of dit concept verder reikt dan BACH2, pasten de auteurs dezelfde dosisaanpak toe op een ander quiescentie-bevorderend eiwit, FOXO1. Opnieuw verhoogden hoge niveaus stamachtige markers maar verlamden effectorfuncties, terwijl lage, zorgvuldig ingestelde doses zowel duurzaamheid als dodelijke capaciteit behielden en de tumorcontrole bij muizen verbeterden. Samen laten deze bevindingen zien dat de hoeveelheid van een regulatorisch eiwit die tot expressie wordt gebracht het gedrag van geïnengineerde T-cellen volledig kan veranderen. In plaats van te vertrouwen op permanent hypergeactiveerde, potentieel kankerverwekkende circuits, kunnen clinici wellicht veiligere therapieën ontwerpen door natuurlijke "rust- en herstel"-factoren fijn af te stemmen zodat T-cellen langer in de strijd blijven zonder hun slagkracht te verliezen.
Bronvermelding: Conti, A.G., Evans, A.C., von Linde, T. et al. Fine-tuning BACH2 dosage balances stemness and effector function to enhance antitumor T cell therapy. Nat Immunol 27, 436–451 (2026). https://doi.org/10.1038/s41590-025-02389-z
Trefwoorden: T-celtherapie, kankerimmunotherapie, BACH2, cellulaire quiescentie, gen-dosering