Clear Sky Science · nl
Ruimtelijke patroonvorming van TGFβ-signalerende fibroblasten ligt ten grondslag aan behandelresistentie bij reumatoïde artritis
Waarom aanhoudende gewrichtspijn ertoe doet
Veel mensen met reumatoïde artritis gebruiken moderne medicijnen die het immuunsysteem onderdrukken, maar hun gewrichten blijven pijnlijk en stijf. Deze studie onderzoekt waarom sommige patiënten niet verbeteren, zelfs wanneer de ontsteking in het gewricht lijkt af te nemen. Door nauwkeurig te kijken waar en hoe bepaalde ondersteunende cellen in het gewricht littekenprogramma’s inschakelen, onthullen de onderzoekers een verborgen vorm van schade die aanhoudende pijn kan verklaren en aanwijzingen geeft voor nieuwe behandelstrategieën.
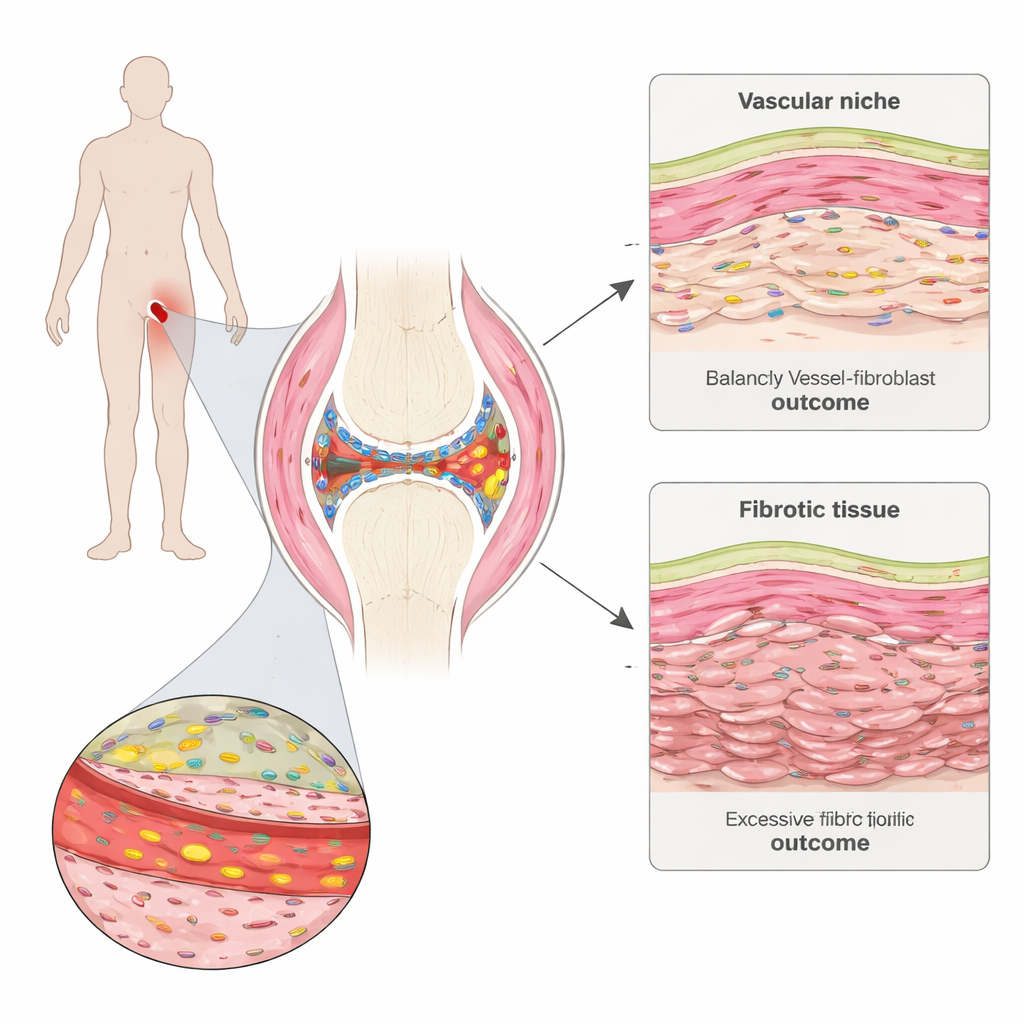
Een nadere blik in het pijnlijke gewricht
Reumatoïde artritis valt het synovium aan, een dun weefsel dat gewrichten bekleedt en smeert. Het team nam kleine synoviale biopsieën van mensen met vroege ziekte vóór aanvang van de behandeling en opnieuw zes maanden later. Met geavanceerde ruimtelijke genmapping konden ze zien welke genen actief waren in duizenden afzonderlijke cellen, terwijl de locatie van die cellen in het weefsel behouden bleef. Ze identificeerden verschillende “buurten” in het synovium, waaronder clusters van immuuncellen, vetrijke gebieden, de dunne binnenbekleding en regio’s vol met bloedvaten en structurele cellen die fibroblasten worden genoemd.
Littekenvormende cellen en behandelresistentie
In vergelijking met patiënten die later remissie bereikten, vonden de onderzoekers bij degenen die niet in remissie raakten een opvallend patroon: vóór de behandeling hadden de non-remitters al sterkere signalen voor weefselfibrose. Een specifiek fibroblastprogramma, gekenmerkt door hoge productie van het extracellulaire matrixeiwit COMP, was bij deze patiënten uitgebreid aanwezig. Deze COMP-rijke fibroblasten deelden kenmerken met littekenvormende cellen die worden gezien bij long- en huidfibrose en waren het sterkst geassocieerd met een slechte behandelrespons. In de loop van de tijd raakten regio’s die door deze cellen gedomineerd werden, vaak dicht opgevuld met bindweefsel maar relatief arm aan cellen, wat suggereert dat ze een stijve matrix afzetten die kan blijven bestaan zelfs nadat de ontsteking is afgenomen.
Bloedvaten als verborgen regisseurs
De fibrogene fibroblasten lagen niet willekeurig verspreid. Ze groepeerden rond bloedvaten en vormden gelaagde perivasculaire zones. De binnenste laag, grenzend aan de vaatwand, bracht andere genen tot expressie dan de buitenste laag. Het team toonde aan dat cellen die bloedvaten bekleden Notch-signalen naar nabijgelegen fibroblasten sturen, die op hun beurt bepalen hoe deze fibroblasten reageren op een familie van pro-fibrotische prikkels bekend als TGF-bèta. Dicht bij het vat stimuleert Notch-signalerng fibroblasten tot het maken van TGF-bèta maar verlaagt tegelijkertijd het aantal TGF-bèta-receptoren aan hun oppervlak, waardoor hun gevoeligheid wordt geremd. Verder weg, waar de invloed van Notch afneemt, dragen fibroblasten meer receptoren en worden ze zeer responsief, waardoor ze veranderen in COMP-rijke cellen die fibrose aanjagen.
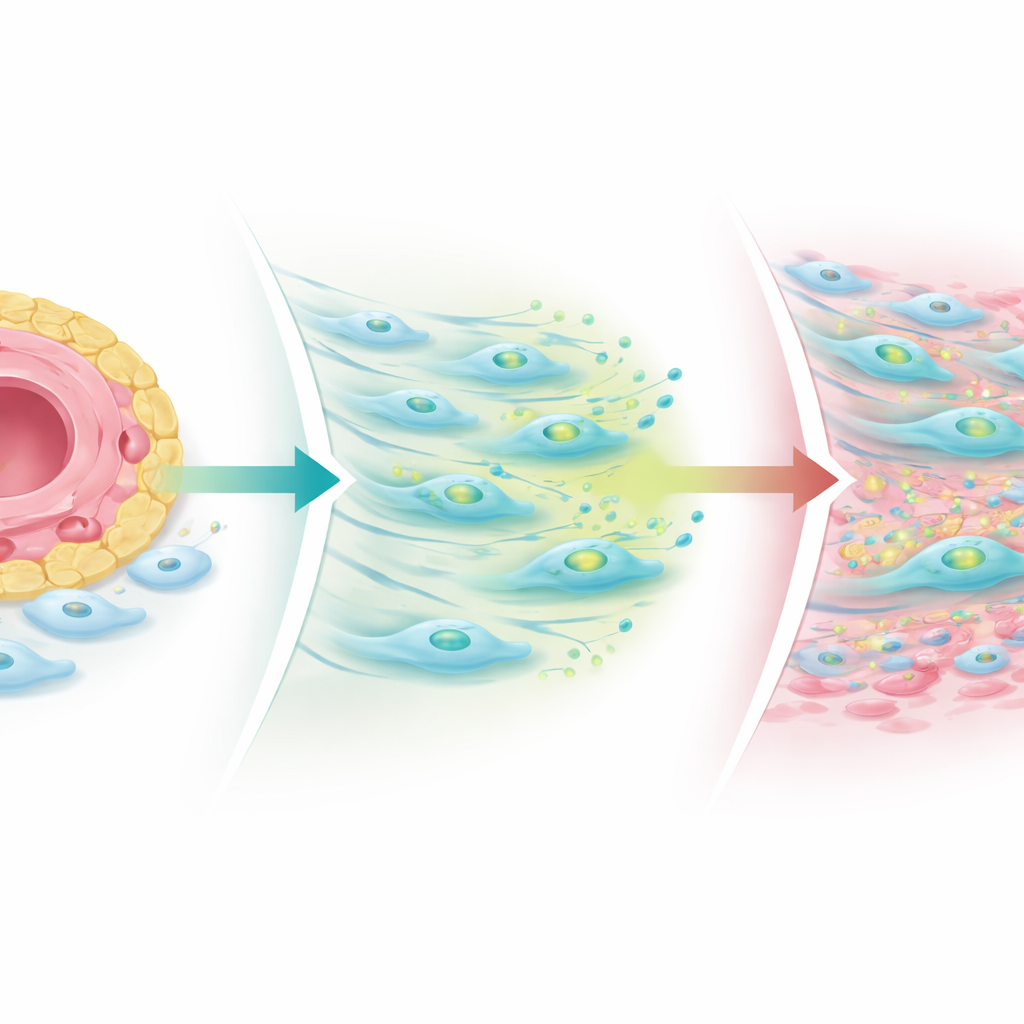
Wat er gebeurt als het evenwicht verstoord raakt
De onderzoekers bouwden vereenvoudigde gewrichtsmodellen in laboratoriumschotels en driedimensionale organoïden gemaakt van patiëntweefsel om dit mechanisme te onderzoeken. Wanneer ze Notch-signalen van endotheelcellen versterkten, namen fibroblasten de productie van TGF-bèta toe maar daalde het aantal receptoren, wat littekenvorming beperkte. Wanneer ze Notch blokkeerden of het vaste patroon verstoorden, herwonnen fibroblasten TGF-bèta-receptoren—vooral een co-receptor genaamd TGF-bèta receptor III—en breidden COMP-positieve fibrogene cellen zich uit weg van de vaten. In patiëntbiopten genomen na behandeling krimpten immuuncelclusters bij bijna iedereen, maar fibrogene niches, met name COMP-rijke regio’s, groeiden vaak, vooral bij degenen wier gewrichtspijn aanhield. Dit suggereert dat standaard anti-inflammatoire geneesmiddelen het immuungevaar kunnen blussen terwijl ze een littekenproces achterlaten of zelfs onthullen dat de gewrichten stijf en pijnlijk houdt.
Nieuwe manieren om hardnekkige gewrichten te kalmeren
Tot slot testte het team of het verstoren van dit fibrogene circuit therapeutisch nuttig zou kunnen zijn. In patiënt-afgeleide organoïden verminderden geneesmiddelen die Notch remmen of TGF-bèta-signalerng blokkeren de productie van COMP, andere litteken-gerelateerde eiwitten en belangrijke collagens, en herschikten ze genactiviteit in perivasculaire zones. Voor de leek is de boodschap dat niet alle schade bij reumatoïde artritis voortkomt uit zichtbare ontsteking: een deel is “hardgeprogrammeerd” in de ondersteunende cellen en bloedvaten van het gewricht. Door de Notch–TGF-bèta-communicatie te richten die bepaalt hoe fibroblasten littekenweefsel aanleggen, zouden toekomstige behandelingen een hardnekkige, fibrotische vorm van de ziekte die zich aan de huidige immuungerichte medicijnen onttrekt, kunnen voorkomen of omkeren.
Bronvermelding: Bhamidipati, K., McIntyre, A.B.R., Kazerounian, S. et al. Spatial patterning of fibroblast TGFβ signaling underlies treatment resistance in rheumatoid arthritis. Nat Immunol 27, 556–571 (2026). https://doi.org/10.1038/s41590-025-02386-2
Trefwoorden: reumatoïde artritis, fibrose, fibroblasten, TGF-bèta signalering, Notch-pad