Clear Sky Science · nl
Engineering van xylosyltransferase om proteoglycanen in zoogdiercellen te manipuleren
Waarom celomhulsels ertoe doen
Elke cel in ons lichaam draagt een moleculair “omhulsel” dat helpt te communiceren met buren en de omgeving waar te nemen. Een belangrijk deel van dit omhulsel bestaat uit proteoglycanen—eiwitten versierd met lange suikerketens die fungeren als kleine antennes voor groeifactoren, immuunsignalen en structurele aanwijzingen. Wanneer deze suikerdecoratie misgaat, kan de ontwikkeling stagneren en kunnen weefsels zoals bot en spier ernstig worden aangetast. Toch hebben wetenschappers het moeilijk gevonden om precies in kaart te brengen welke eiwitten deze ketens dragen en hoe individuele componenten van het omhulsel het celgedrag beïnvloeden. Deze studie introduceert een nauwkeurige chemische strategie om deze suikerketens op levende zoogdiercellen te labelen en opnieuw op te bouwen, wat een manier opent om de informatie op hun oppervlak te lezen en te herschrijven. 
De eerste stap van suiker‑aanhechting herbedraden
De bouw van proteoglycanen begint wanneer een speciale enzymfamilie, xylosyltransferasen XT1 en XT2, de eerste suiker op een eiwit aanbrengt, waarmee de plek wordt gemarkeerd waar een lange keten zal groeien. Omdat beide enzymen dezezelfde eerste stap kunnen uitvoeren, was het moeilijk te bepalen op welke eiwitten ieder van hen binnen cellen werkt. De auteurs gebruikten een “bump‑and‑hole” ontwerp—gebruikelijk in de moderne chemische biologie—om dit op te lossen. Ze hervormden de actieve plaats van XT1 lichtelijk en creëerden extra ruimte (het “gat”), en introduceerden een bijpassend, iets groter suikerbouwblok, 6AzGlc (de “bult”). De gemodificeerde XT1 kan nu dit aangepaste suiker gebruiken, terwijl het natuurlijke enzym dat niet kan, waardoor onderzoekers alleen die eiwitten kunnen labelen die door het herontworpen enzym worden aangeraakt.
Een ontworpen suiker de cel binnensmokkelen
Om deze aanpak in levende cellen te laten werken, moest het team het verhoogde suiker aanleveren in een vorm die door de cellulaire stofwisseling herkend wordt. In plaats van te vertrouwen op normale suikeropnamepaden—die xylose‑analogen slecht verwerken—bouwden ze een gecageerde versie van 6AzGlc met een verborgen fosfaatgroep. Eenmaal in het cytosol maken cellulaire enzymen deze groep vrij en zetten het molecuul om in UDP‑6AzGlc, de geactiveerde vorm die door de gemodificeerde xylosyltransferasen nodig is. Zorgvuldige chromatografie bevestigde dat cellen behandeld met de correct geconfigureerde gecageerde verbinding aanzienlijke hoeveelheden van de geactiveerde ontworpen suiker produceerden, terwijl een spiegelbeeld‑controle bijna niets produceerde. 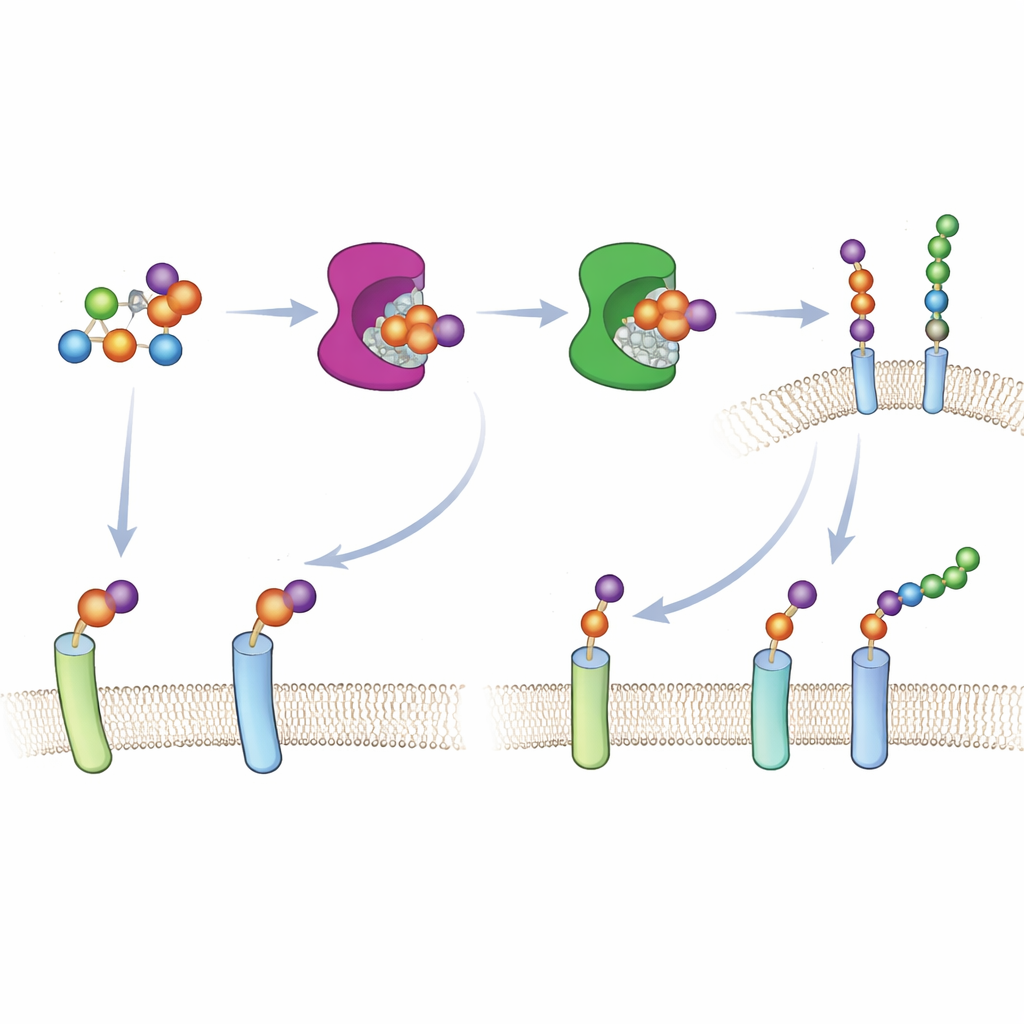
Verborgen spelers labelen en identificeren
Met zowel het gewijzigde enzym als de geactiveerde suiker aanwezig, toonden de onderzoekers aan dat alleen cellen die het gemodificeerde XT1 of XT2 tot expressie brachten het 6AzGlc‑label in hun oppervlakte‑proteoglycanen opnamen. De azidegroep op 6AzGlc fungeert als een klein chemisch handvat dat kan worden “geklikt” aan fluorescerende kleurstoffen of biotine, waarmee gelabelde eiwitten zichtbaar en verrijkbaar worden. Massaspectrometrie van verrijkte monsters toonde een rijke verzameling bekende proteoglycanen—waaronder decorine, meerdere glypicanen, syndecan‑4, CD44 en versican—wat bevestigt dat het systeem echte suikerdragende eiwitten markeert. Belangrijk is dat de gemodificeerde enzymen dezelfde sequentievoorkeuren behielden als hun natuurlijke tegenhangers, wat betekent dat het chemische label op authentieke aanhechtingsplaatsen wordt geïnstalleerd en niet op nieuwe, kunstmatige posities.
Designer‑proteoglycanen bouwen
Een onverwacht voordeel van het 6AzGlc‑label is dat dit, in tegenstelling tot de natuurlijke aanvangssuiker, niet door downstreamenzymen kan worden verlengd tot een volledige keten. Dit verhindert effectief verdere groei van de keten en vereenvoudigt de moleculaire structuur die met massaspectrometrie geanalyseerd moet worden. De auteurs maakten van deze eigenschap een instrument: nadat XT1 6AzGlc op een natuurlijke aanhechtingsplaats heeft geplaatst, gebruiken ze klikchemie om synthetische heparinefragmenten aan te monteren, waardoor “designer‑proteoglycanen” met precies gedefinieerde suikerketens ontstaan. In borstkankercellen die hun eigen syndecan‑1 misten, herstelde het terugplaatsen van zulke designer‑versies normaal uitspreiden op een eiwitbedekt oppervlak, wat aantoont dat het chemisch herbouwde proteoglycaan functioneel kan vervangen wat het natuurlijke eiwit doet.
Betekenis voor biologie en geneeskunde
Dit werk levert een krachtig instrumentarium om selectief de suikerketens te labelen en te manipuleren die bepalen hoe cellen communiceren. Door de rollen van XT1 en XT2 uiteen te halen en alleen hun directe doelen te labelen, kunnen onderzoekers nu in kaart brengen welke proteoglycanen in specifieke weefsels en ziektebeelden actief zijn. De mogelijkheid om natuurlijke ketengroei te stoppen en te vervangen door op maat gemaakte suikers stelt wetenschappers ook in staat te onderzoeken hoeveel van de functie van een proteoglycaan wordt bepaald door de eiwitruggegraat versus de suikerlaag. Op de lange termijn kan zulke precieze engineering helpen complexe signaalprocessen aan het celoppervlak te ontcijferen en therapieën inspireren die defecte celomhulsels herstellen of herprogrammeren bij ontwikkelingsstoornissen, kanker en andere ziekten.
Bronvermelding: Li, Z., Chawla, H., Di Vagno, L. et al. Xylosyltransferase engineering to manipulate proteoglycans in mammalian cells. Nat Chem Biol 22, 612–621 (2026). https://doi.org/10.1038/s41589-025-02113-w
Trefwoorden: proteoglycanen, glycosaminoglycanen, xylosyltransferase, chemische biologie, celoppervlakte‑signalering