Clear Sky Science · nl
Een enkele allosterische plek verenigt activatie, modulatie en remming in TRPM5
Hoe één kleine poortwachter smaak en stofwisseling vormt
De voedingsmiddelen die we lekker vinden en de manier waarop ons lichaam suiker verwerkt, hangen af van microscopische "poortwachter"-eiwitten in onze cellen. Eén van die poortwachters, een kanaal genaamd TRPM5, helpt ons zoete, bittere en hartige smaken te waarnemen en helpt de alvleesklier insuline vrij te geven. Deze studie onthult hoe een enkele kleine holte op TRPM5 fungeert als een hoofdregelaar: het kanaal aanzetten, de gevoeligheid afstemmen en het zelfs uitschakelen — inzichten die toekomstige behandelingen voor diabetes, obesitas en darmstoornissen kunnen sturen.
Een kanaal op het kruispunt van smaak en bloedsuiker
TRPM5 bevindt zich in de membranen van smaakcellen op de tong, hormoonproducerende cellen in de darm en insuline‑afgevende cellen in de alvleesklier. Wanneer het calciumniveau binnen deze cellen stijgt, opent TRPM5 en laat positieve ionen stromen, waardoor de celspanning kort verandert. In smaakpapillen vertelt dit elektrische signaal de hersenen dat er iets zoets, bitters of umami op de tong zit. In de alvleesklier helpt het de pieken van insuline na een maaltijd fijn af te stemmen. Mensen en dieren met verminderde TRPM5‑functie vertonen problemen met insulineafgifte en bloedsuikerregulatie, wat suggereert dat geneesmiddelen die TRPM5 targeten mogelijk ooit metabolische aandoeningen kunnen behandelen. Tot voor kort ontbraken onderzoekers echter precieze middelen om dit kanaal aan of uit te zetten.
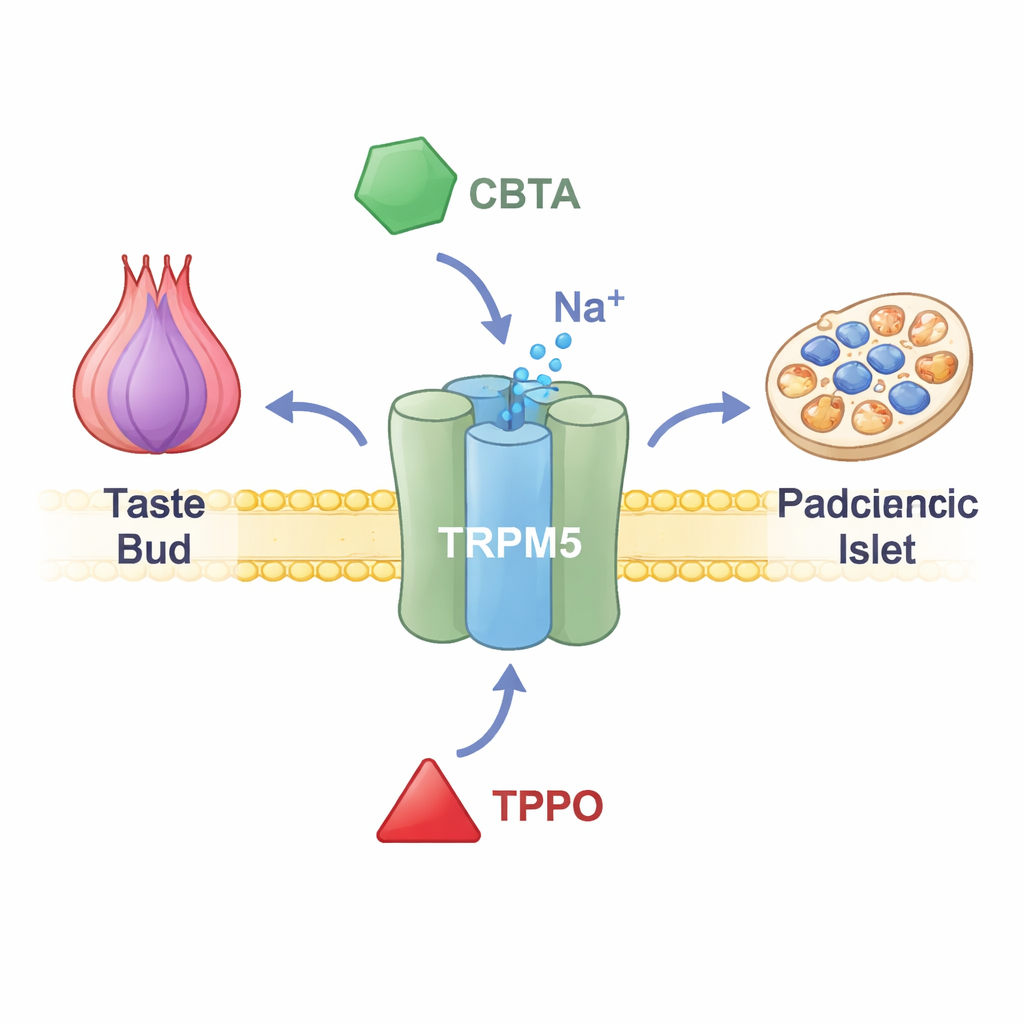
Een nieuwe chemische schakelaar die het kanaal superlaadt
De onderzoekers concentreerden zich op een synthetische verbinding genaamd CBTA, eerder bekend als een stimulator van TRPM5, maar weinig begrepen. Met elektrische opnames van cellen die waren gemodificeerd om TRPM5 te produceren, toonden ze aan dat CBTA het kanaal kan openen zelfs wanneer calcium vrijwel afwezig is, wat bewijst dat het als een echte activator werkt en niet slechts de effecten van calcium versterkt. Bij zeer kleine hoeveelheden calcium — niveaus die TRPM5 normaal stil laten — werken CBTA en calcium samen en genereren veel grotere stromen dan elk afzonderlijk. Dit betekent dat CBTA TRPM5 buitengewoon gevoelig maakt, zodat bijna‑rustende calciumniveaus plotseling sterk genoeg zijn om het kanaal wijd open te zetten.
Een verborgen controleholte onthuld met cryo‑EM
Om te zien hoe dit op atomair niveau werkt, gebruikte het team cryo‑elektronenmicroscopie om driedimensionale momentopnamen van TRPM5 onder verschillende condities vast te leggen. Ze ontdekten dat CBTA zich nestelt in een tot dan toe over het hoofd gezien holte in het bovenste deel van een spanningsgevoelig gebied van het kanaal, net boven waar calcium gewoonlijk bindt. Deze holte, gevormd door een cluster van aminozuren, fungeert als een precies aanlegplaats. Toen de wetenschappers sleutelbouwstenen die deze pocket bekleden veranderden, kon CBTA TRPM5 niet meer activeren, ook al werkte calcium nog steeds, wat bevestigt dat deze kleine nis essentieel is voor de werking van de verbinding. Opvallend is dat CBTA‑binding nabijgelegen delen van het eiwit subtiel herschikt op een manier die het veel gemakkelijker maakt voor calcium om zijn gebruikelijke plaats te grijpen, wat de dramatische synergie in de elektrische metingen verklaart.
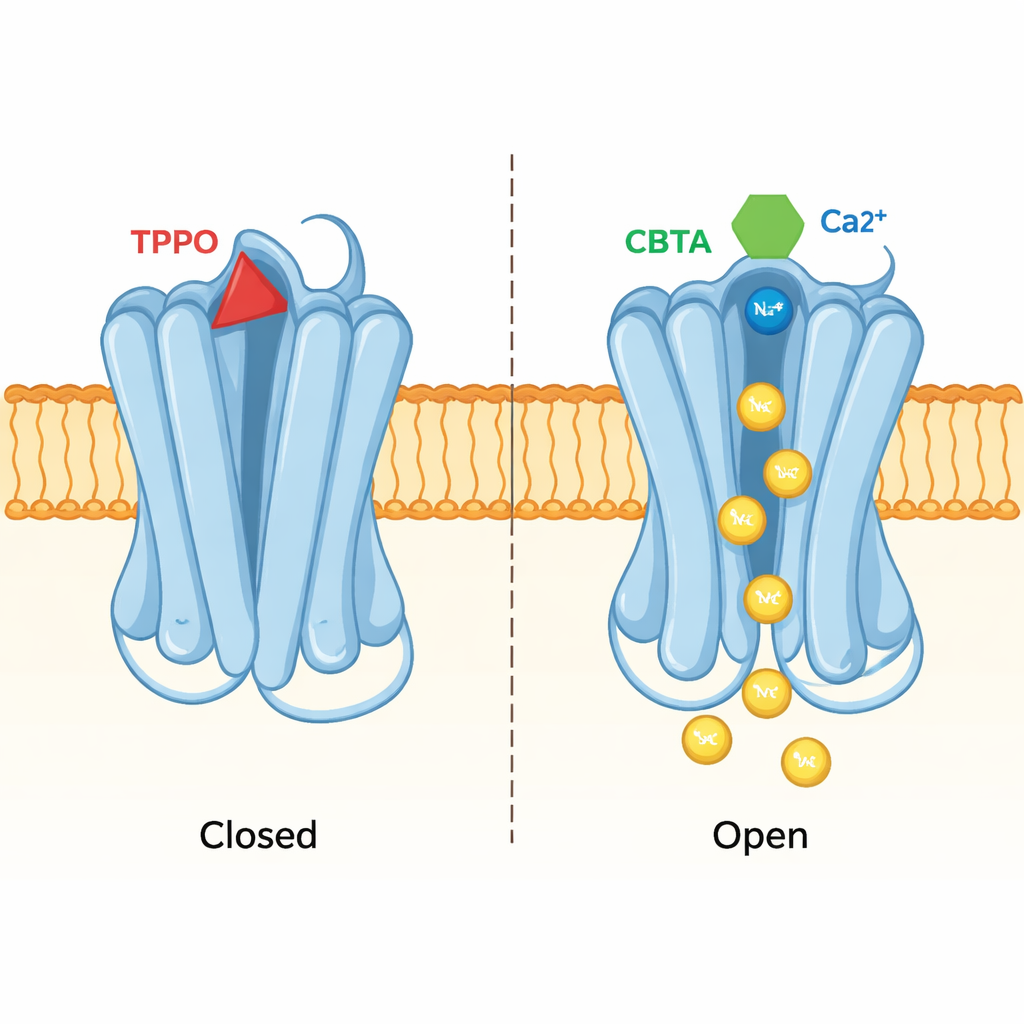
Één pocket, twee tegengestelde uitkomsten
Met dezelfde structurele benadering werd onthuld hoe een remmer genaamd TPPO exact dezelfde pocket gebruikt om het tegengestelde effect te produceren. Wanneer TPPO bindt, blijven beide calciumsites op TRPM5 gevuld, maar blijft de centrale porie van het kanaal samengetrokken en passeren er geen ionen. Vergelijking van TPPO‑gebonden en CBTA‑gebonden structuren toonde aan dat hun verschillende vormen nabijgelegen eiwitsegmenten in tegengestelde richtingen duwen. CBTA bevordert bewegingen die zich naar de porie verspreiden en deze openen; TPPO verstoort juist de communicatie tussen de pocket en de porie, waardoor de poort gesloten blijft. In wezen kan deze ene pocket fungeren als zowel gaspedaal als rem, afhankelijk van welk molecuul erin zit.
De interne bedrading van het kanaal omleiden
De studie laat ook zien dat deze controleholte taken kan overnemen die normaal door een aparte calciumbindende regio binnen de cel worden uitgevoerd. In gemuteerde kanalen waar de gebruikelijke interne calciumsite is uitgeschakeld, kon calcium alleen TRPM5 niet openen. Toch schakelde CBTA deze mutanten nog steeds in en herschikte het een essentieel structureel element dat de binnenste en buitenste delen van het kanaal verbindt. In andere mutanten die de koppeling tussen calciumbinding en porie‑opening verbreken, herstelde toevoeging van CBTA het normale gedrag. Deze resultaten tonen aan dat de nieuw geïdentificeerde site de communicatie tussen verschillende kanaaldomeinen kan omleiden of repareren en fungeert als een flexibel knooppunt voor langafstandssignaaloverdracht binnen het eiwit.
Waarom dit belangrijk is voor toekomstige medicijnen
Voor leken is de kernboodschap dat de onderzoekers een enkele, geneesmiddelgevoelige pocket op TRPM5 hebben gevonden die activatie, fijnafstelling en uitschakeling kan integreren. Een kleine activator zoals CBTA kan zowel calcium imiteren als de gevoeligheid van het kanaal sterk verhogen, terwijl een andere verbinding, TPPO, hetzelfde kanaal kan vastzetten door het te sluiten — allemaal door aan dezelfde plek te binden. Dit eenduidige beeld van hoe TRPM5 wordt gereguleerd, opent de deur naar het ontwerpen van op maat gemaakte moleculen die de activiteit ervan in specifieke weefsels kunnen versterken of dempen, met mogelijke toepassingen variërend van verbeterde smaakgerichte therapieën en geneesmiddelen voor darmmotiliteit tot nieuwe strategieën voor het beheersen van bloedsuiker en metabole ziekten.
Bronvermelding: Ruan, Z., Lee, J., Li, Y. et al. A single allosteric site merges activation, modulation and inhibition in TRPM5. Nat Chem Biol 22, 402–410 (2026). https://doi.org/10.1038/s41589-025-02097-7
Trefwoorden: TRPM5-kanaal, smaakwaarneming, insulineafgifte, ionkanaal‑gating, allosterische modulatie