Clear Sky Science · nl
Genoomwijde associatieanalyses van auto-immuun hypothyreoïdie onthullen auto-immuun- en schildklier-specifieke bijdragen en een omgekeerde relatie met kankerrisico
Waarom dit van belang is voor de dagelijkse gezondheid
Veel mensen voelen zich moe, koud of geestelijk mistig zonder te beseffen dat hun schildklier de oorzaak kan zijn. Auto-immuun hypothyreoïdie, waarbij het eigen afweersysteem de schildklier geleidelijk aan aanvalt, treft meer dan één op de twintig mensen. Deze studie gebruikt genetische gegevens van honderden duizenden vrijwilligers om twee grote vragen te beantwoorden: welke erfelijke veranderingen in ons DNA vergroten de kans op deze aandoening, en hoe hangen diezelfde veranderingen samen met het risico om kanker te ontwikkelen? De antwoorden tonen een verrassende afruil tussen een immuunsysteem dat soms schade aan de schildklier veroorzaakt maar ook extra bescherming tegen tumoren kan bieden.
Over het hele genoom kijken
De onderzoekers combineerden medische dossiers en genetische informatie uit twee grote populatieprojecten, FinnGen in Finland en de UK Biobank in het Verenigd Koninkrijk. Ze richtten zich op mensen die langdurige vervanging van schildklierhormoon nodig hadden en sloten zorgvuldig degenen uit waarvan de schildklierproblemen veroorzaakt waren door chirurgie, kanker of andere niet-auto-immuun oorzaken. Dit leverde meer dan 81.000 gevallen van auto-immuun hypothyreoïdie en meer dan 700.000 controles op, waarmee het de grootste studie naar deze aandoening tot nu toe is. Door miljoenen DNA-markers over het genoom te scannen, ontdekten ze 418 onafhankelijke genetische signalen buiten het grote immuungenecluster, verspreid over minstens 280 regio’s van het genoom. Veel van deze signalen betroffen zeldzame of laagfrequente DNA-veranderingen die de eiwitstructuur wijzigen en daarmee directe aanwijzingen geven voor de onderliggende biologie.
Algemene immuuneffecten scheiden van schildklier-specifieke effecten
Auto-immuun hypothyreoïdie bevindt zich op het kruispunt van algemene auto-immuniteit en de specifieke biologie van de schildklier. Om deze componenten uit elkaar te halen, vergeleek het team hun resultaten met genetische studies van andere auto-immuunziekten en met bloedwaarden van schildklierstimulerend hormoon (TSH), de belangrijkste klinische marker die gebruikt wordt om een traag werkende schildklier op te sporen. Met behulp van een Bayesiaanse classificatiemethode groepeerden ze genetische signalen in die gedeeld worden met brede auto-immuunziekten en die meer specifiek zijn voor de regulatie van schildklierhormoon. Ze schatten dat ongeveer 38% van de signalen werkt via algemene immuunroutes die veel auto-immuun aandoeningen beïnvloeden, terwijl ongeveer 20% voornamelijk via schildklierfunctie werkt. De schildkliergerichte varianten beïnvloedden eerder hormoonspiegels en genen die actief zijn in schildklierweefsel, terwijl de algemene immuunvarianten actiever waren in T-cellen, de witte bloedcellen die immuunreacties coördineren.
Inzoomen op een sleutelschakelaar in het immuunsysteem
Een bijzonder opvallende bevinding betrof een zeldzame DNA-verandering in het gen ZAP70, dat een belangrijke signaalstof in T-cellen codeert. Ernstige defecten in dit eiwit staan bekend om het veroorzaken van ernstige immuundeficiëntie, maar de hier geïdentificeerde variant veroorzaakt slechts een gedeeltelijk functieverlies. Laboratoriumexperimenten in geconstrueerde T-cellen lieten zien dat dit gewijzigde ZAP70 de keten van signalen die normaal volgt op herkenning van een doelwit verzwakt, maar niet volledig blokkeert. Cellen met de variant konden activatiemerkers en downstream signaalstappen minder goed inschakelen. Deze afgezwakte respons lijkt het delicate evenwicht te verstoren dat normaal zelfreactieve T-cellen opruimt, waardoor dragers vatbaarder worden voor auto-immuunziekten maar ook hun risico op bepaalde immuundeficiënties licht verhoogd is.
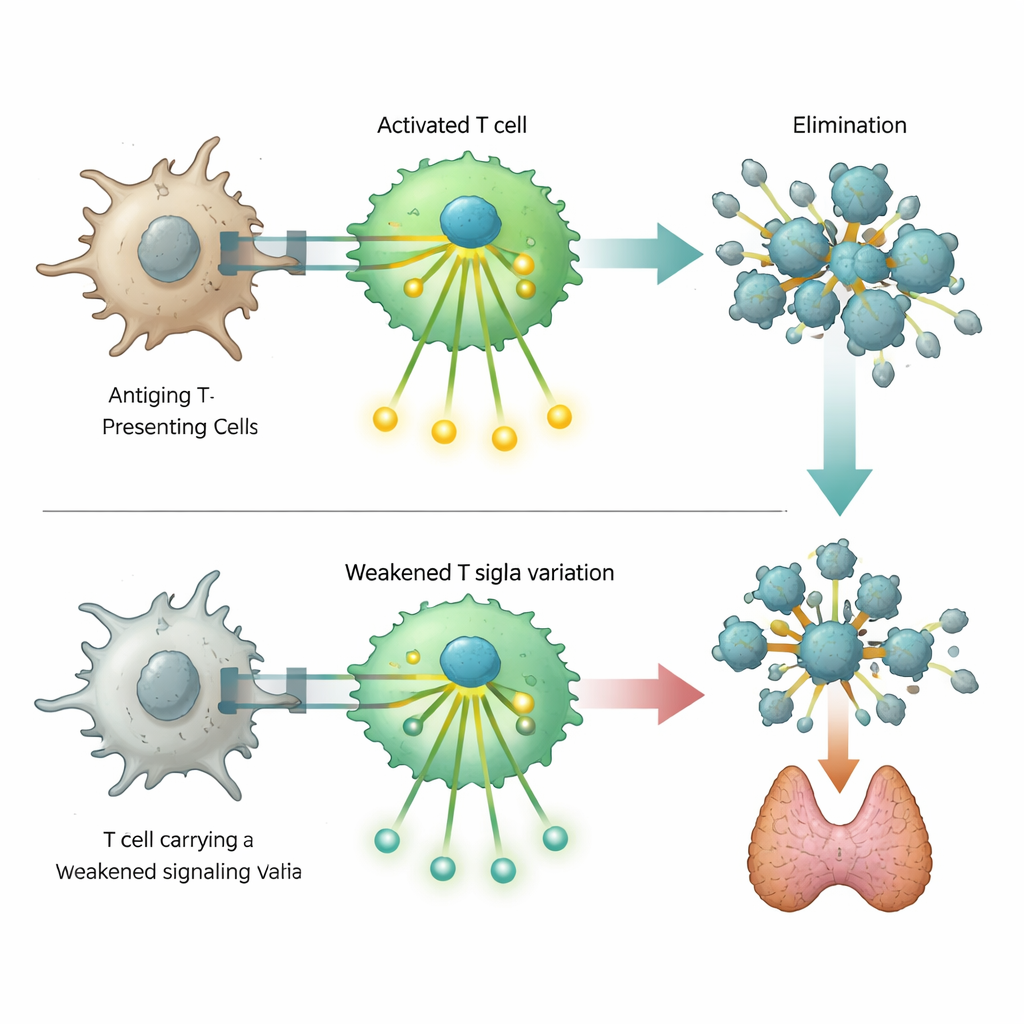
Een onverwachte link met kankerbescherming
Aangezien dezelfde immuunroutes die auto-immuniteit aandrijven ook tumoren kunnen aanvallen, onderzochten de auteurs vervolgens hoe de genetica van auto-immuun hypothyreoïdie samenhangt met kankerrisico. Ze berekenden een polygeen risicoscore die iemands erfelijke aanleg voor hypothyreoïdie samenvat en testten de associatie daarvan met vele ziekten in de Finse gegevens. Zoals verwacht correleerde een hogere score met een hoger risico op diverse auto-immuunziekten. Verrassender was een consistent patroon van lager risico op verschillende vormen van kanker, vooral basaalcelcarcinoom en andere huidkankers, maar ook borstkanker en prostaatkanker en een algemene categorie “alle kankers”. Toen het team rechtstreeks keek naar kanker-genoomonderzoeken, beïnvloedde ongeveer 10% van de hypothyreoïdie-gerelateerde loci ook huidkanker, waarbij dezelfde genetische variant doorgaans de schildklierauto-immuniteit verhoogde en het risico op huidkanker verlaagde. Deze gedeelde varianten waren geconcentreerd in immuun-gerelateerde genen, inclusief bekende geneesmiddeldoelen die worden gebruikt bij checkpoint-immunotherapie.
Wat dit betekent voor patiënten en de geneeskunde
In gewoon Nederlands laat dit onderzoek zien dat sommige mensen worden geboren met immuunsystemen die iets “vuuriger” zijn ingesteld, waardoor ze gevoeliger zijn voor langzame, vaak stille schade aan de schildklier, maar tegelijk beter uitgerust zijn om opkomende kankercellen te herkennen en te verwijderen. De studie maakt duidelijk welke genetische veranderingen via algemene immuunoveractiviteit werken en welke specifiek de productie van schildklierhormoon beïnvloeden, en verklaart daarmee waarom aandoeningen zoals de ziekte van Hashimoto en de ziekte van Graves sommige risicogenen kunnen delen maar de schildklierfunctie in tegengestelde richtingen duwen. Het helpt ook verklaren waarom patiënten die schildklierproblemen ontwikkelen tijdens immuunversterkende kankertherapieën vaak beter op die behandelingen reageren. Over het geheel genomen suggereren de bevindingen dat veelvoorkomende, natuurlijke variatie in immuuncheckpoint- en signaalgenen zowel auto-immuun schildklieraandoeningen als het levenslange kankerrisico vormgeeft, en bieden ze nieuwe aanknopingspunten voor preventie en meer gepersonaliseerd gebruik van immunotherapieën.
Bronvermelding: Reeve, M.P., Kanai, M., Graham, D.B. et al. Genome-wide association analyses of autoimmune hypothyroidism reveal autoimmune and thyroid-specific contributions and an inverse relationship with cancer risk. Nat Genet 58, 550–559 (2026). https://doi.org/10.1038/s41588-026-02521-1
Trefwoorden: auto-immuun hypothyreoïdie, schildklieraandoening, genetisch risico, immuunsysteem, kankerbescherming