Clear Sky Science · nl
Genome-wide association analyses highlight the role of the intestinal molecular environment in human gut microbiota variation
Waarom uw DNA en darmbacteriën bij hetzelfde verhaal horen
Biljoenen microben leven in onze darmen en beïnvloeden alles, van vertering en stofwisseling tot het immuunsysteem. Maar waarom dragen sommige mensen van nature andere mengsels van darmbacteriën dan anderen, zelfs wanneer ze op dezelfde plek wonen en vergelijkbaar eten? Deze studie, gebaseerd op gedetailleerde genetische en darmmicrobioomgegevens van bijna 30.000 volwassenen in Zweden en Noorwegen, laat zien dat ons eigen DNA stilletjes meehelpt het netwerk van microben in ons lichaam te schrijven.
Een omvangrijke blik in Noordse darmen
Om te achterhalen hoe menselijke genen het microbioom vormen, combineerden onderzoekers gegevens uit vier grote Zweedse bevolkingsonderzoeken met 16.017 volwassenen en controleerden hun bevindingen in 12.652 Noren. Alle deelnemers gaven bloed voor analyse van hun DNA en brachten fecale monsters in voor diepe sequentiebepaling van microbieel DNA. In plaats van zich alleen te richten op brede bacteriegroepen, gebruikten de onderzoekers methoden met hoge resolutie die honderden individuele soorten kunnen onderscheiden. Vervolgens doorzochten ze het menselijk genoom, variant voor variant, om te zien welke DNA-regio’s samenhingen met de algemene microbiele rijkdom (hoeveel verschillende soorten aanwezig zijn) en met de aanwezigheid of abundantie van specifieke bacteriesoorten.
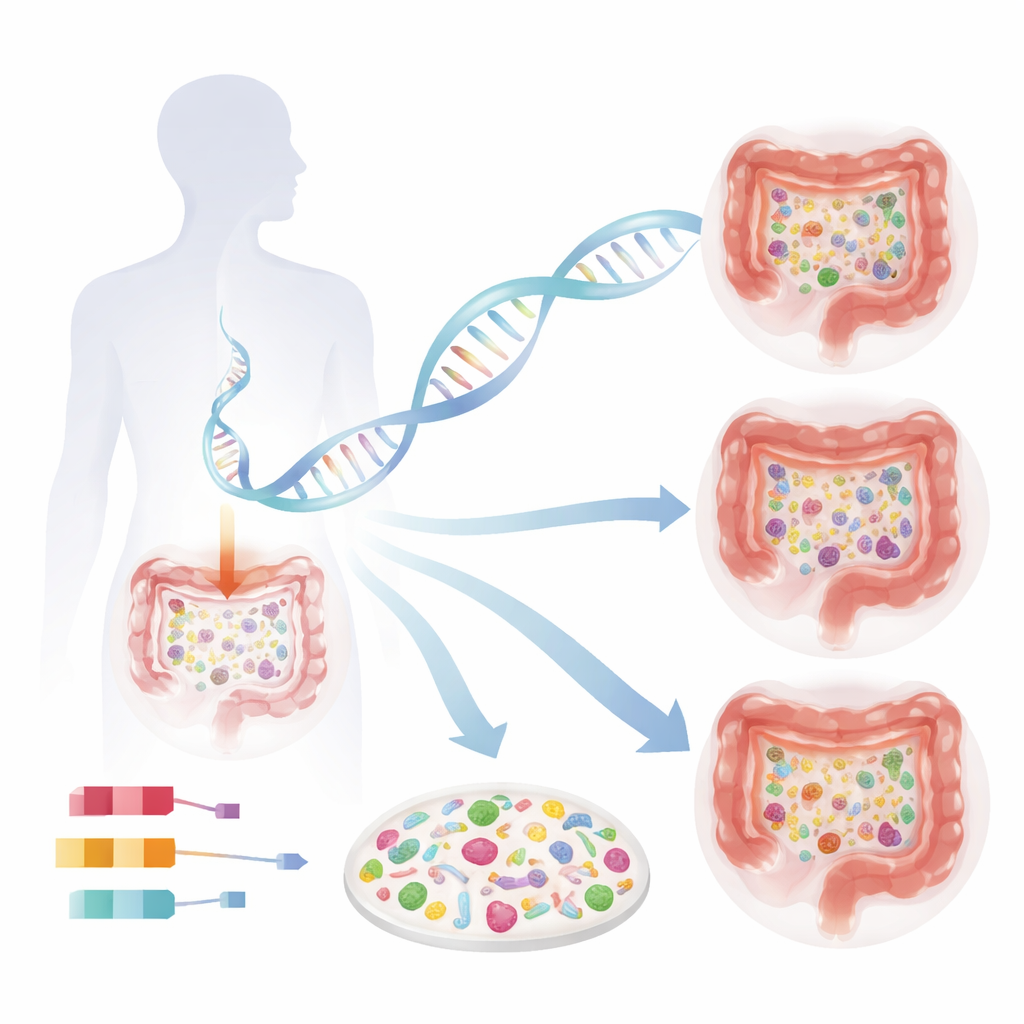
Genetische schakelaars die microbiele rijkdom afstemmen
Een van de meest opvallende ontdekkingen was een regio in het menselijk genoom met twee genen, OR51E1 en OR51E2, die eerder bekendstonden als reukreceptoren. Deze receptoren zitten ook op speciale hormoonproducerende cellen in het darmslijmvlies en detecteren vetzuren die door microben worden gemaakt. Mensen met een bepaalde versie van deze DNA-regio hadden doorgaans minder bacteriesoorten in hun darmen, en dit patroon werd onafhankelijk bevestigd in de Noorse groep. De bevinding suggereert dat de manier waarop darmcellen microbe-afgeleide vetzuren waarnemen terugkoppelt op de diversiteit van het microbioom zelf, mogelijk door veranderingen in darmahormonen die motiliteit, eetlust of lokale immuunreacties beïnvloeden.
Oppervlakte suikers, mucus en de microbiele buurt
De studie wees ook meerdere genetische regio’s aan die de suikerachtige en slijmerige omgeving aan het darmsoppervlak bepalen—prime vastgoed voor bacteriën. Varianten in het welbekende lactasegen (LCT), dat bepaalt of volwassenen melksuiker kunnen verteren, hielden verband met verschuivingen in meerdere soorten, waaronder Bifidobacterium die goed gedijen op lactose. Genen die bloedgroepen en de bijbehorende “secretor”-status bepalen—ABO, FUT2 en FUT3–FUT6—wijzigen fucose-bevattende suikers die op darmslijm en in afscheidingen voorkomen. Verschillende genetische combinaties hierin waren gekoppeld aan onderscheiden sets bacteriën die zich daaraan kunnen hechten of ervan kunnen leven. Een andere sleutelregio lag in een mucinegen, MUC12, dat deel uitmaakt van het geraamte van de mucuslaag zelf. Veranderingen in deze regio correleerden met de abundantie van een soort genaamd Coprobacillus cateniformis en deelden zelfs een genetisch signaal met hoe vaak mensen hun darmen legen, wat wijst op verweven effecten op darmfunctie en microbieel samenstel.
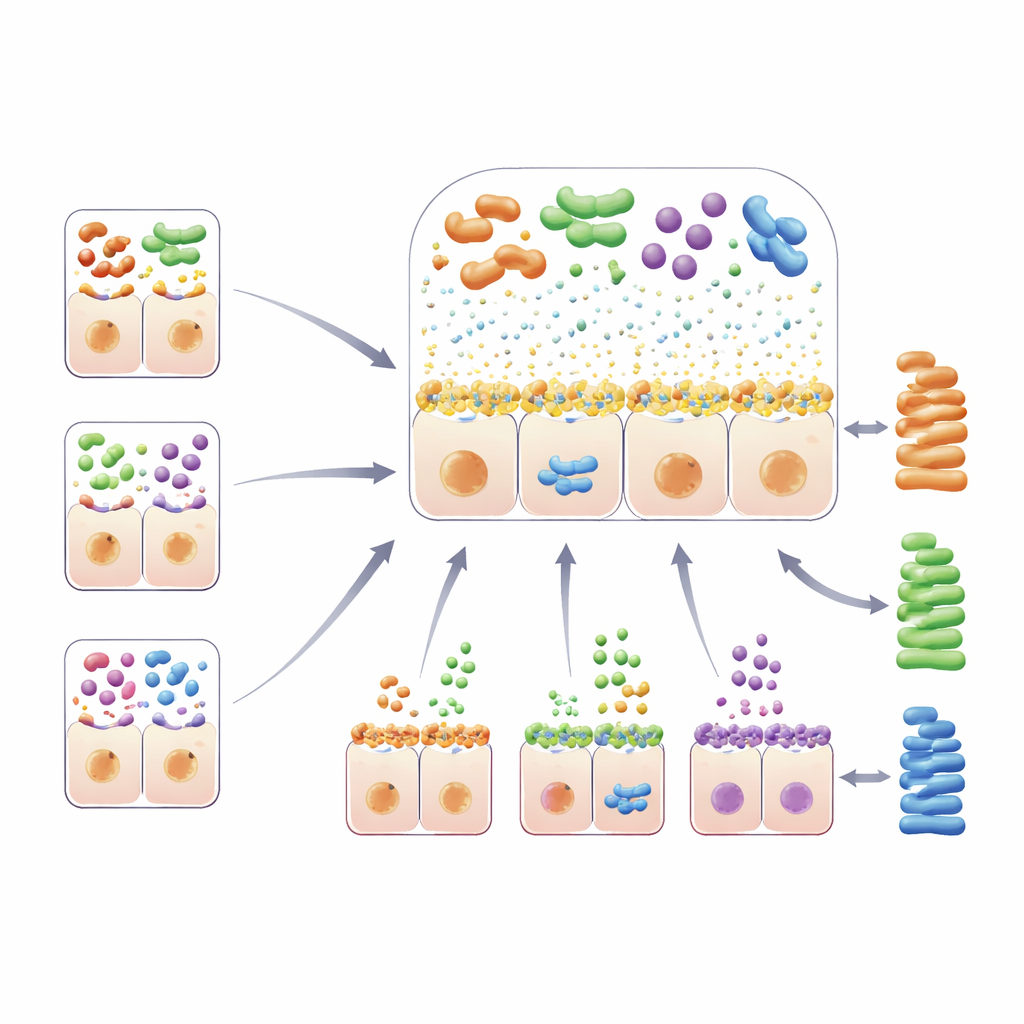
Van microben naar stofwisseling en lichaamsvorm
Buiten het in kaart brengen van “wie er woont” vroegen de onderzoekers of DNA-regio’s die aan bepaalde bacteriën gekoppeld zijn, ook overlappen met menselijke kenmerken zoals bloedcholesterol, galzuren en vetverdeling. In meerdere gevallen betroffen dezelfde genoomdelen beide. Varianten nabij de genen CORO7–HMOX2 en FOXP1 beïnvloedden een cluster bacteriën waaronder Turicibacter en Clostridium saudiense, en vielen ook samen met verschillen in taille-heupverhouding, galzuren en LDL-cholesterol. Met genetische instrumenten die causaal verband suggereren, vonden de auteurs aanwijzingen dat één microbe, een Intestinibacter-soort, mogelijk het LDL-cholesterol verhoogt, en dat Turicibacter de opslagplaats van lichaamsvet kan beïnvloeden. Een andere regio, SLC5A11, was gekoppeld aan een butyraat-producerende bacterie, Agathobaculum butyriciproducens, die in diermodellen van hersenziekte beschermende effecten heeft laten zien. Hier leek de menselijke DNA-variant de bloedspiegels van een klein molecuul, myo-inositol, te verlagen terwijl hij de groei van deze mogelijk gunstige microbe bevorderde.
Wat dit betekent voor gezondheid en toekomstige behandelingen
Samen tonen deze resultaten dat menselijke genen die betrokken zijn bij darmwaarneming, mucus-samenstelling en oppervlakte-suikers mede bepalen welke microbiele soorten zich met succes in onze darmen kunnen vestigen. De effecten zijn bescheiden voor elk afzonderlijk gen, en het beeld is tot nu toe het duidelijkst voor relatief veelvoorkomende bacteriën bij mensen met Europese afkomst. Toch breidt het werk de lijst van menselijke DNA-regio’s die betrouwbaar aan specifieke darmmicroben gekoppeld zijn uit van slechts een paar naar minstens acht, en koppelt meerdere hiervan aan metabole kenmerken zoals cholesterol en vetpatronering. Voor leken is de kernboodschap dat het darmmicrobioom niet alleen door voeding en omgeving wordt gevormd: ons genetische bouwplan bouwt het leefgebied dat microben aantreffen, en duwt de gemeenschap naar bepaalde bewoners en weg van anderen. Naarmate grotere en meer diverse studies beschikbaar komen, kan begrip van deze tweerichtingsrelatie tussen genen en microben helpen bij het afstemmen van voedingsadviezen, het voorspellen van ziekte-risico’s en mogelijk het sturen van therapieën die medicijnen, dieet en gerichte manipulatie van het microbioom combineren.
Bronvermelding: Dekkers, K.F., Pertiwi, K., Baldanzi, G. et al. Genome-wide association analyses highlight the role of the intestinal molecular environment in human gut microbiota variation. Nat Genet 58, 540–549 (2026). https://doi.org/10.1038/s41588-026-02512-2
Trefwoorden: gut microbiome, human genetics, intestinal mucus, bile acids, metabolism