Clear Sky Science · nl
GlycoRNA in complex met heparan sulfaat reguleert VEGF-A-signaal
Hoe cellen de bloedvatuitsignalen van het lichaam verfijnen
Bloedvaten verschijnen niet zomaar overal waar groeisignalen optreden — ze moeten nauwkeurig worden geregeld om weefsels van voeding te voorzien zonder tumoren te voeden of blindheid te veroorzaken. Dit artikel onthult een onverwachte "rem" op een belangrijk vaatgroeisignaal genaamd VEGF-A. De auteurs tonen aan dat kleine RNA-fragmenten die samen met suikers en eiwitten het celoppervlak decoreren, het bericht van VEGF-A kunnen dempen en daarmee onze kijk op de taal die cellen aan hun oppervlak gebruiken veranderen.
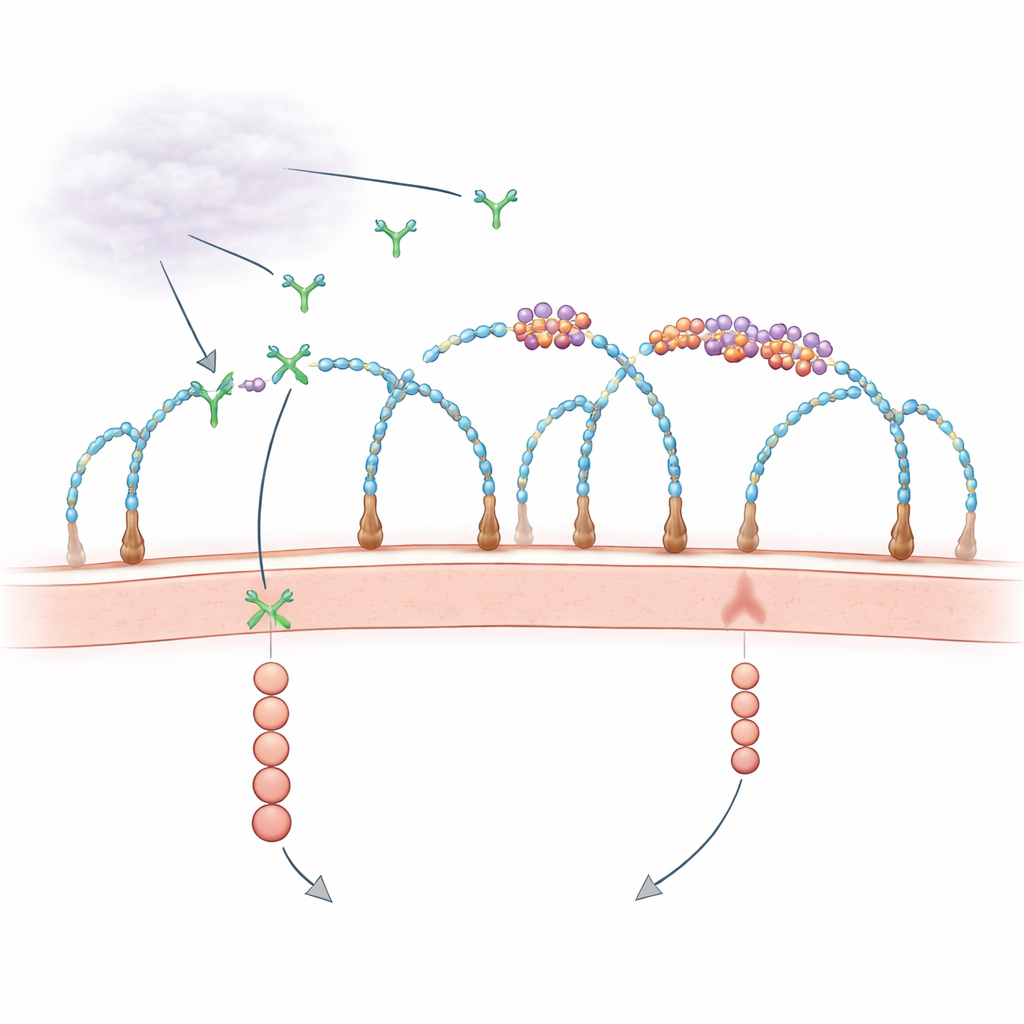
Een verrassende rol voor RNA op het celoppervlak
Decennialang wisten biologen dat de buitenste laag van de cel, rijk aan suikerdecoratie op eiwitten die heparan sulfaat proteoglycanen worden genoemd, helpt groeifactoren vast te houden en aan hun receptoren voor te schotelen. Tegelijkertijd wezen verspreide observaties erop dat RNA-fragmenten buiten cellen de bloedvatgroei konden beïnvloeden, maar de spelers en mechanismen waren onduidelijk. Recente studies lieten zien dat sommige kleine RNA’s chemisch aan complexe suikers zijn gekoppeld om "glycoRNA’s" te vormen, en dat bepaalde RNA-bindende eiwitten ook op het celoppervlak verschijnen en samen met deze RNA’s clusteren. De nieuwe studie stelt een gerichte vraag: regelen deze kleine RNA–eiwit eilandjes in het membraan daadwerkelijk hoe groeisignalen zoals VEGF-A worden waargenomen?
Gecentraliseerde RNA–eiwit-eilandjes bouwen met suikerketens
Middels genoomwijde CRISPR-knockoutscreens en hogeresolutiemicroscopie ontdekten de onderzoekers dat specifieke suikerketens — heparan sulfaat met bepaalde sulfaatgroepen — essentiële scaffolds vormen voor het samenstellen van deze RNA–eiwitclusters, die zij celoppervlakte-ribonucleoproteïnen (csRNP’s) noemen. Wanneer sleutelenzymen die heparan sulfaat bouwen of sulfateren werden verwijderd, verdwenen de clusters van glycoRNA en hun partner-eiwitten van het celoppervlak, hoewel de RNA’s en eiwitten nog wel in de cellen aanwezig waren. Enzymen die heparan sulfaatketens van het oppervlak knippen of chemische blokkering van sulfatering hadden hetzelfde effect. Deze resultaten tonen aan dat intacte, correct gesulfateerde heparan sulfaatketens csRNP’s organiseren in nanoschaal-eilandjes in het membraan.
RNA-clusters werken als remmen op een krachtig vaatgroeisignaal
Het team richtte zich vervolgens op humane endotheelcellen, die bloedvaten bekleden en op VEGF-A reageren. Zij vonden dat deze cellen ook heparan sulfaat-gebonden csRNP-clusters tonen. Behandeling van levende cellen met RNasen, enzymen die RNA afbreken, verwijderde de RNA-component zonder de onderliggende suikerketens te verstoren. Onder die omstandigheden veroorzaakte VEGF-A’s meest voorkomende, heparan-bindende vorm (VEGF-A165) veel sterkere activatie van de downstream ERK-signaalroute, terwijl een kortere vorm zonder de heparan-bindende staart (VEGF-A121) onaangetast bleef. Na verwijdering van RNA binden meer VEGF-A165-moleculen aan het celoppervlak, terwijl de receptorhoeveelheden gelijk bleven. In 3D-microfluïdische apparaten groeiden endotheelcellen die aan RNase waren blootgesteld verder in collageengel en vormden ze robuuster buisachtige structuren, wat aangeeft dat het vernietigen van oppervlak-RNA pro-angiogene activiteit ontketent.
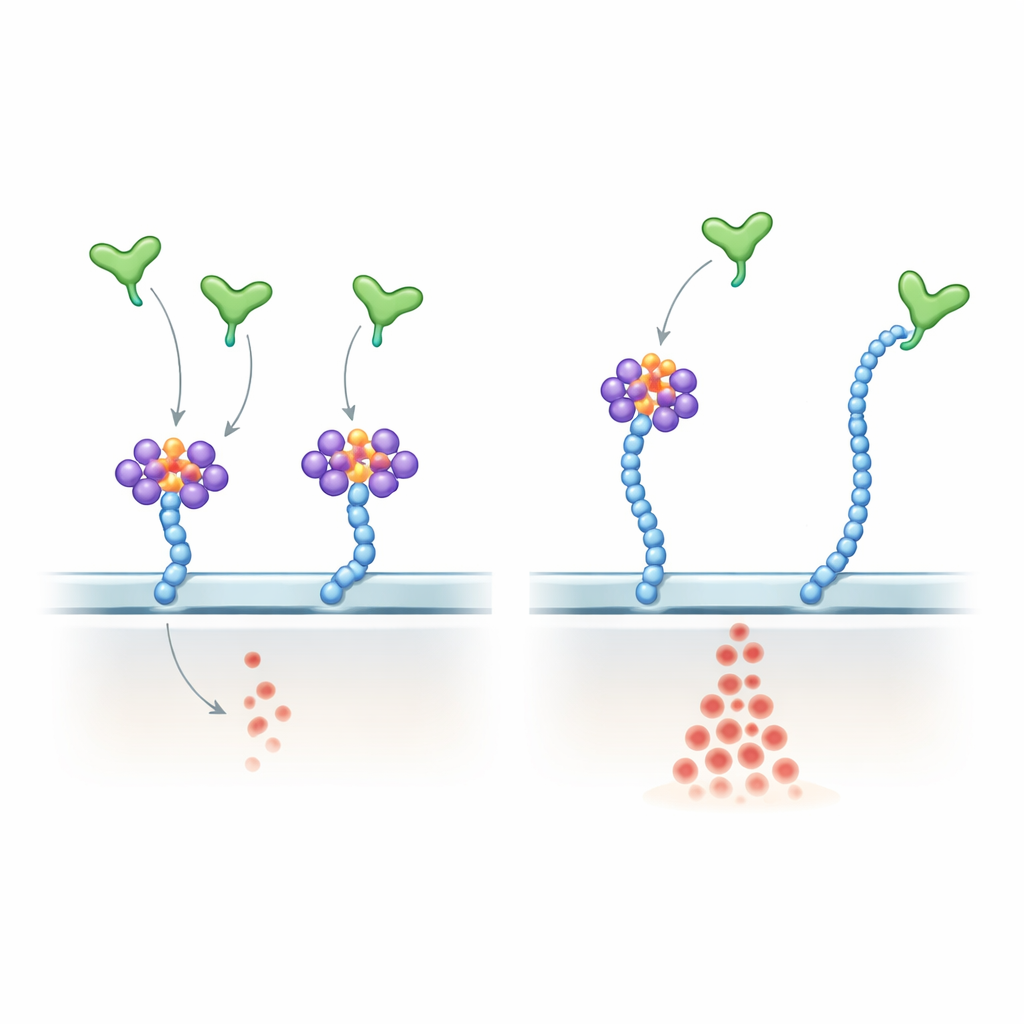
Ontleden hoe VEGF-A RNA versus suiker waarneemt
Om het mechanisme te onderzoeken toonden de auteurs aan dat VEGF-A165 direct bindt aan geselecteerde kleine RNA’s, waaronder veel bekende glycoRNA’s, via zijn positief geladen C-terminaal — dezelfde regio die heparan sulfaat bindt. Ze maakten een subtiele versie van VEGF-A165 waarbij kritieke arginine-residuen in deze staart werden vervangen door lysines. Deze mutant behield zijn algemene positieve lading en greep nog steeds heparan sulfaatketens, maar bond slecht aan glycoRNA en werd grotendeels ongevoelig voor RNase-behandeling. In endotheelcellen veroorzaakte de mutant sterkere en meer RNase-resistente ERK-activatie dan de normale VEGF-A165, wat nauw het effect nabootste van het verwijderen van RNA van het celoppervlak. Bij levende muizen veroorzaakte injectie van de mutant in het oog uitbundigere retinale vaatgroei dan het normale eiwit. In zebravisembryo’s verstoorde overexpressie van de mutant-Vegfa de normale vatpatronen en nam het aantal endotheelcellen toe.
Van basaal mechanisme naar bredere implicaties
Tenslotte lieten de auteurs zien dat het fuseren van VEGF-A’s heparan-bindende staart aan een ongeassocieerd signaaleiwit, Wnt3a, de Wnt-activiteit kon herleiden: het vastzetten van de normale staart verminderde Wnt-gestuurde ontwikkelingseffecten, terwijl het vastzetten van de RNA-ongevoelige staart deze versterkte. Gezamenlijk ondersteunen deze experimenten een model waarin csRNP-clusters, verankerd door specifiek gesulfateerde heparan sulfaat, VEGF-A en verwante factoren binden om hun activiteit te temperen. Wanneer de RNA-component wordt verwijderd of wanneer groeifactoren hun vermogen om RNA waar te nemen verliezen, kantelt de balans naar sterkere signalering en veranderde vasculaire ontwikkeling in meerdere soorten.
Waarom dit belangrijk is voor gezondheid en toekomstige therapieën
Voor niet-specialisten is de kernboodschap dat cellen niet alleen eiwitten en suikers gebruiken, maar ook kleine RNA’s die op hun oppervlak worden getoond om krachtige groeisignalen zoals VEGF-A fijn af te stemmen. Deze aan suikers vastgemaakte RNA–eiwitclusters fungeren als verstelbare remmen op bloedvatvorming en helpen ervoor te zorgen dat nieuwe vaten ontstaan waar en wanneer dat nodig is. Het verstoren van deze balans — door oppervlak-RNA af te breken of door de RNA-bindende eigenschappen van groeifactoren te wijzigen — kan vaatgroei versterken of misleiden. Inzicht in deze nieuw ontdekte controlelaag kan de deur openen naar therapieën die angiogenese preciezer omhoog of omlaag kunnen bijstellen bij kanker, oogziekten, wondgenezing en regeneratieve geneeskunde door zich te richten op oppervlak-RNA’s, hun suiker-scaffolds of de RNA-gevoelige regio’s van groeifactoren.
Bronvermelding: Chai, P., Kheiri, S., Kuo, A. et al. GlycoRNA complexed with heparan sulfate regulates VEGF-A signalling. Nature 651, 808–818 (2026). https://doi.org/10.1038/s41586-025-10052-8
Trefwoorden: angiogenese, vasculair endotheliale groeifactor, heparan sulfaat, celoppervlakte-RNA, glycoRNA