Clear Sky Science · nl
Ontwikkelingsconvergentie en -divergentie in humane stamcelmodellen van autisme
Waarom dit onderzoek belangrijk is voor gezinnen en de samenleving
Autismespectrumstoornis is berucht complex: honderden verschillende genen zijn in verband gebracht met een verhoogd risico, maar veel autistische mensen delen vergelijkbare uitdagingen in communicatie, sociale interactie en gedrag. Deze studie stelt een bedrieglijk eenvoudige vraag met grote implicaties: wanneer zeer verschillende genetische veranderingen de kans op autisme vergroten, verstoren ze dan uiteindelijk de zich ontwikkelende menselijke hersenen op vergelijkbare manieren? Met behulp van kleine in het laboratorium gekweekte modellen van de menselijke cortex, gemaakt van de eigen cellen van patiënten, traceren de onderzoekers hoe vroege storingen in genactiviteit kunnen samenkomen in gemeenschappelijke paden die beïnvloeden hoe hersencellen ontstaan, rijpen en verbindingen vormen.
Miniatuur menselijk hersenweefsel kweken in het laboratorium
Om deze vraag te onderzoeken verzamelde het team huid- of bloedcellen van 55 personen: sommigen hadden goed gekarakteriseerde zeldzame mutaties die sterk aan autisme zijn gekoppeld, anderen hadden autisme zonder een bekende grote mutatie, en weer anderen waren onbeïnvloede controles. Deze cellen werden omgeprogrammeerd tot geïnduceerde pluripotente stamcellen, die vrijwel elk celtype kunnen worden. De wetenschappers leidden ze vervolgens naar de vorming van driedimensionale “corticale organoïden” – kleine weefselbolletjes die de vroege ontwikkeling van de menselijke cerebrale cortex nabootsen. Gedurende 100 dagen ontwikkelden deze organoïden zich van grotendeels stamcelachtige voorlopercellen naar netwerken rijk aan jonge neuronen. Op vier momenten langs deze tijdlijn (dagen 25, 50, 75 en 100) mat het team welke genen aan- of uitgezet waren in honderden organoïden, waarmee ze een gedetailleerde film van moleculaire veranderingen tijdens vroege hersenontwikkeling creëerden.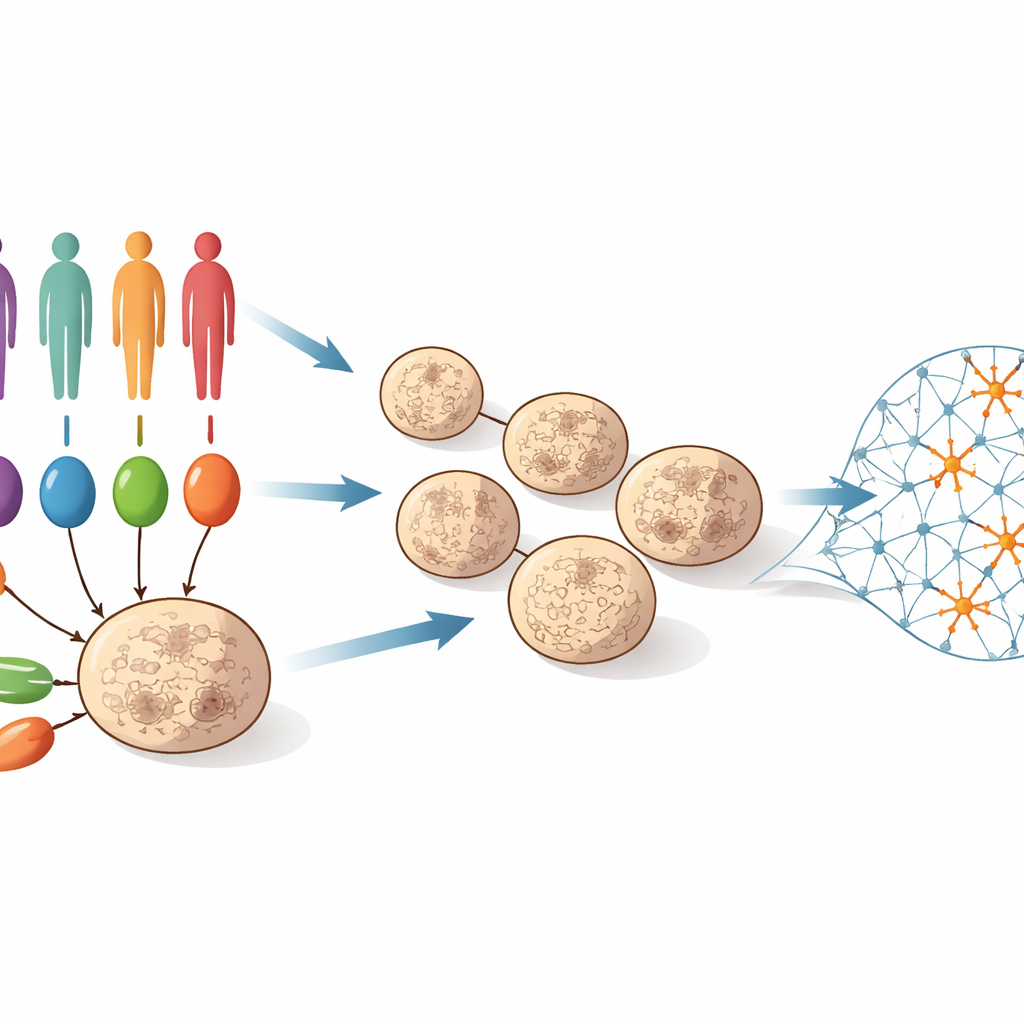
Veel genetische wegen, gedeelde vroege omwegen
Hoewel de aan autisme gekoppelde mutaties zeer verschillend waren – waaronder grote ontbrekende of gedupliceerde DNA-segmenten en specifieke genveranderingen – vertoonden organoïden met dezelfde mutatie zeer reproduceerbare genactiviteitsprofielen. Vroeg in de ontwikkeling, vooral rond dag 25, gaf elke mutatie een eigen sterke handtekening: honderden tot meer dan duizend genen waren verkeerd gereguleerd vergeleken met controles. Toch veranderden zelfs in dit vroege stadium meerdere mutaties overlappende genensets die betrokken zijn bij de manier waarop DNA in cellen wordt verpakt en afgelezen. Deze gedeelde veranderingen troffen bekende hoogrisico-autismegenen en andere genen verbonden aan neuro-ontwikkelingsstoornissen, wat suggereert dat verschillende mutaties al zeer vroeg in de hersenvorming vergelijkbare cellulaire mechanismen verstoren.
Convergentie naarmate het hersenmodel rijpt
Terwijl de organoïden zich ontwikkelden richting meer volwassen neuronen (rond dag 75 en 100), wijzigde het beeld. De mutatie-specifieke verschillen werden minder onderscheidend, terwijl de overeenkomsten sterker werden. Bij bijna alle bestudeerde genetische vormen van autisme zagen de onderzoekers verminderde activiteit van genen die belangrijk zijn voor elektrische signalering bij synapsen – de communicatiepunten tussen neuronen – en verhoogde activiteit van genen die zijn gekoppeld aan celgroei en eiwitproductie. Fijne verschuivingen in de verhoudingen en rijpingsstadia van verschillende celtypen deden zich voor, wat wijst op veranderingen in de timing van neuronaal ontstaan en rijping in plaats van het grootschalig verlies van bepaalde cellen. Tegen het laatste tijdpunt toonden duizenden genen een gedeeld patroon van dysregulatie over de verschillende zeldzame mutaties, hoewel de mutaties zelf verschillende oorspronkelijke genen betroffen.
Een centraal regelingsknooppunt dat veel autismegenen verbindt
Dieper gravend gebruikten de onderzoekers netwerkanalyses om genen die de neiging hebben samen aan- en uitgezet te worden in “modules” te groeperen. Eén module in het bijzonder, genoemd M5, viel op. De genen daarin zijn het meest actief vroeg in de ontwikkeling en zijn sterk verrijkt voor autisme-risicogenen, met name diegenen die regelen hoe andere genen worden aan- of uitgezet en hoe DNA wordt verpakt. In organoïden van meerdere autisme-mutatiegroepen werd deze module consequent naar beneden bijgesteld. De onderzoekers toonden aan dat veel van de eiwitten in M5 fysiek met elkaar interageren en zo een regulatoir knooppunt vormen. Met CRISPR-gebaseerde hulpmiddelen om selectief 26 van deze M5-regelaars in menselijke neurale voorlopercellen te onderdrukken, bevestigden ze dat dit knooppunt rechtstreeks grote sets downstream-genen aanstuurt, waaronder veel extra autisme- en neuro-ontwikkelingsrisicogenen, en dat verstoring ervan paden kan veranderen die betrokken zijn bij neuronvorming en synapsfunctie.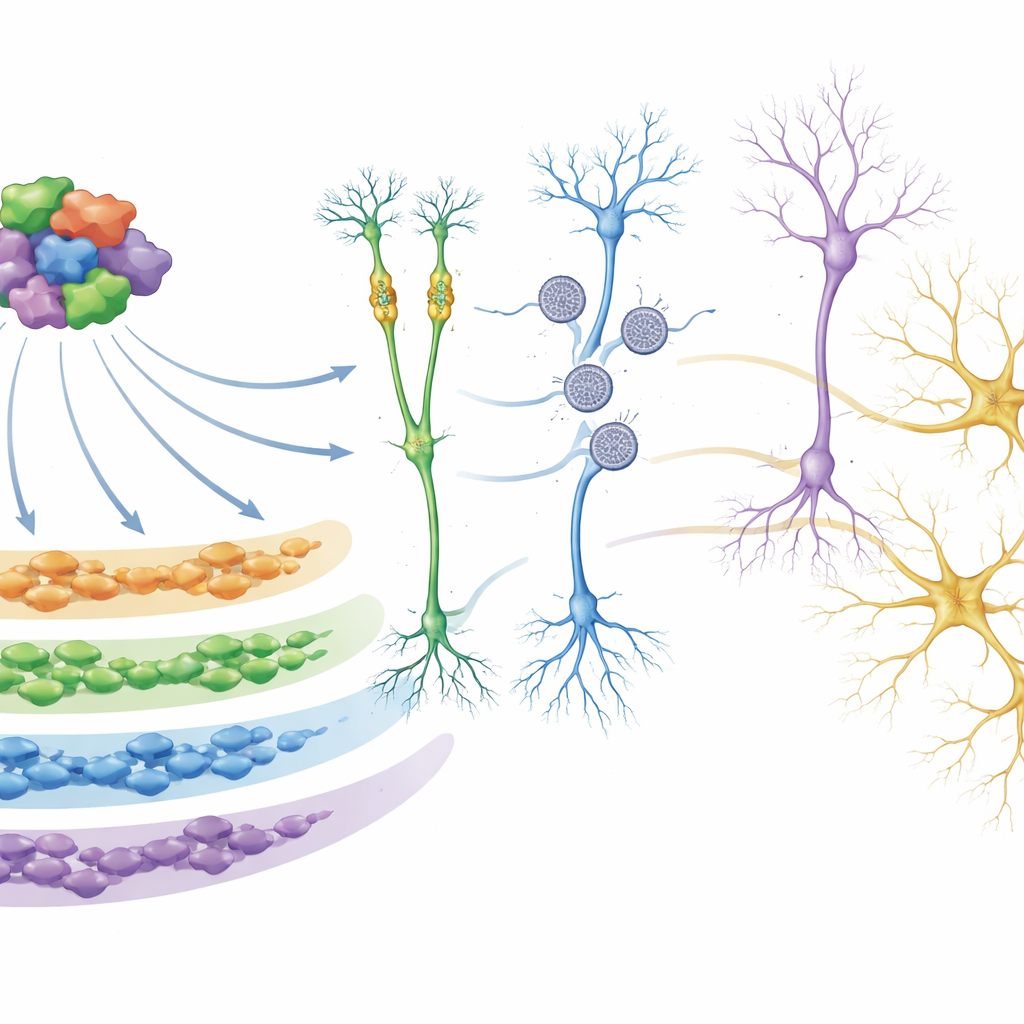
Wat dit betekent voor het begrip van autisme
Dit werk suggereert een verenigend beeld: zeldzame, krachtige aan autisme gekoppelde mutaties verstoren aanvankelijk verschillende delen van het genoom, maar hun effecten slaan door naar een gedeeld vroeg regelsysteem dat bepaalt hoe corticale neuronen worden gegenereerd en bekabeld. In de loop van de tijd convergeren die effecten naar gemeenschappelijke uitkomsten – vertraagde of veranderde neuronrijping en verstoorde synaptische programma’s – zelfs als de aanvankelijke genetische oorzaken verschillen. Voor gezinnen betekent dit dat zeer verschillende diagnoses op DNA-niveau toch overlappende biologische paden in de zich ontwikkelende hersenen kunnen beïnvloeden. Voor onderzoekers en clinici biedt het geïdentificeerde regulerende netwerk een gefocuste set moleculaire doelen voor toekomstige therapieën die gericht zijn op het herstellen van meer typische patronen van hersenontwikkeling bij een breed scala aan genetische aandoeningen gerelateerd aan autisme.
Bronvermelding: Gordon, A., Yoon, SJ., Bicks, L.K. et al. Developmental convergence and divergence in human stem cell models of autism. Nature 651, 707–719 (2026). https://doi.org/10.1038/s41586-025-10047-5
Trefwoorden: autismespectrumstoornis, hersenorganoïden, stamcelmodellen, genregulatie, neuroontwikkeling