Clear Sky Science · nl
Systeemanalyses van lipidemobilisatie door menselijke lipidoverdrachtseiwitten
Hoe cellen hun vet op orde houden
Elke cel in uw lichaam is omsloten door vetrijke membranen, en duizenden verschillende vetten helpen die membranen met alles, van het doorgeven van signalen tot het leveren van energie. Die vetten liggen echter niet willekeurig verspreid: elk intern compartiment van een cel heeft zijn eigen speciale samenstelling. Deze studie stelt een eenvoudige maar verstrekkende vraag: hoe verplaatsen cellen de juiste vetten naar de juiste plek op het juiste moment, en wat gebeurt er als dat systeem niet goed werkt?
Eiwitten die vetten vervoeren
Cellen vertrouwen op een grote familie van moleculen die lipidoverdrachtseiwitten (LTP's) worden genoemd; die kunnen een vetmolecuul uit het ene membraan plukken, het olieachtige deel in een beschermend zakje verbergen en het afleveren bij een ander membraan. Veel menselijke LTP's zijn gekoppeld aan aandoeningen zoals kanker en neurologische ziekten, maar voor de meesten wisten we niet welke vetten ze daadwerkelijk vervoeren. De auteurs gingen aan de slag om een systematische kaart te maken van welke menselijke LTP's aan welke lipiden binden, en hoe het verhogen van de activiteit van deze LTP's de volledige verzameling vetten in een cel herschikt.
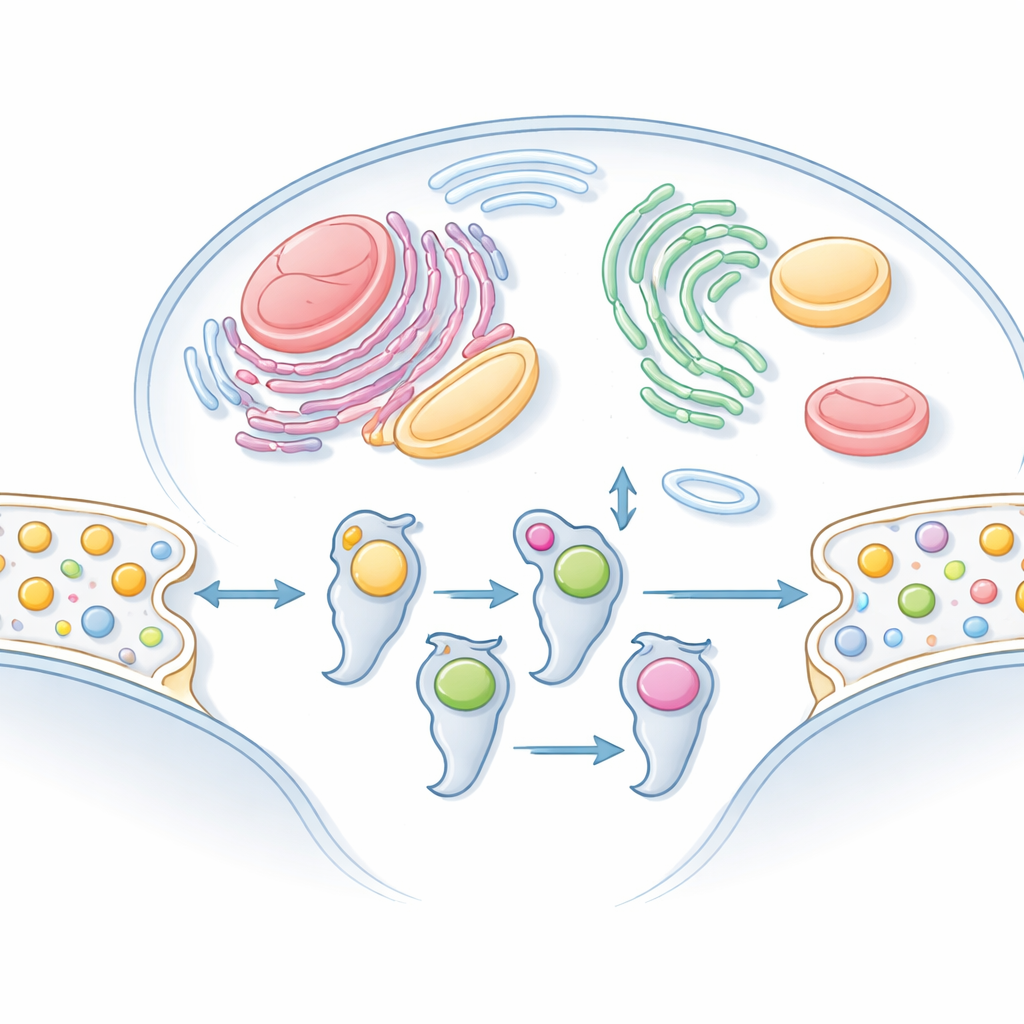
Een grootschalige kaart van vettransport opbouwen
Daartoe kloonden de onderzoekers 101 menselijke LTP's en brachten ze tot expressie in twee verschillende omstandigheden. In menselijk-afgeleide cellen lieten ze elke LTP zich samenvoegen met de vetten die er van nature aanwezig waren. In een reageerbuisopstelling mengden ze gezuiverde LTP's met kunstmatige membranen gemaakt van dierlijke weefselextracten. Vervolgens puurderen ze meer dan 100 LTP–lipidecomplexen en identificeerden de gebonden vetten met gevoelige massaspectrometrie. Door eiwit- en lipidesignalen te matchen over veel scheidingsstappen filterden ze toevallige meereizigers eruit en behielden alleen lipiden die betrouwbaar met elke LTP meereisden. Het resultaat was een catalogus van LTP-partners die negen grote LTP-families beslaat.
Nieuwe ladingen en nieuwe regels
Deze kaart bevestigde bekende partners — zoals vitamine A voor zijn draagereiwitten — maar bracht ook nieuwe en soms verrassende ladingen aan het licht. Een LTP genaamd HSDL2, gekoppeld aan stoornissen in vetopslag, bleek triacylglycerolen te mobiliseren, dezelfde neutrale vetten die onze vetcellen vullen. Andere LTP's bonden signaalvetten zoals diacylglycerol, of een speciale groep "ether"-lipiden die via een aparte route worden gemaakt. Veel LTP's bleken meer dan één klasse lipiden te hanteren, wat suggereert dat ze dubbel werk doen: ze kunnen hun hoofdlading verplaatsen terwijl ze ook hulpende lipiden behandelen die de uitwisseling aandrijven of de stofwisseling bijsturen. Toen de onderzoekers cellen dwongen om individuele LTP's te overproduceren, veranderden de niveaus van zowel bekende als nieuw ontdekte lipidepartners op voorspelbare manieren, wat aantoont dat de nieuw in kaart gebrachte ladingen geen laboratoriumartefacten zijn maar functioneren in levende cellen.
Waarom slechts sommige vetten mobiel zijn
Kijkend naar het gehele datapakket merkten de auteurs op dat LTP's niet alle varianten van een gegeven lipid gelijk behandelen. Ze tonen duidelijke voorkeuren voor vetten met kortere staarten en met één of twee dubbele bindingen in die staarten. Zulke vetten creëren kleine defecten in membranen waardoor ze gemakkelijker uit te trekken zijn, terwijl zeer stijve of sterk geknikte staarten moeilijker te extraheren zijn. Sommige LTP's gingen verder en gaven de voorkeur aan extreem specifieke staartpatronen. Bijvoorbeeld, de ceramidetransporter CERT prefereerde ceramiden met bepaalde ketenlengtes, waaronder zeldzame zeer lange soorten die helpen bij het vormen van dicht gepakte membraanpatches. Een andere groep, de fosfatidylinositol-overdrachtsproteïnen, gaf de voorkeur aan een soort die een arachidonzuurstaart draagt, een bouwsteen voor veel hormoonachtige signalen. Computersimulaties van LTP-structuren onthulden hoe clusters van specifieke aminozuren in de bindingszakjes nauwe passing voor deze gekozen staarten creëren.
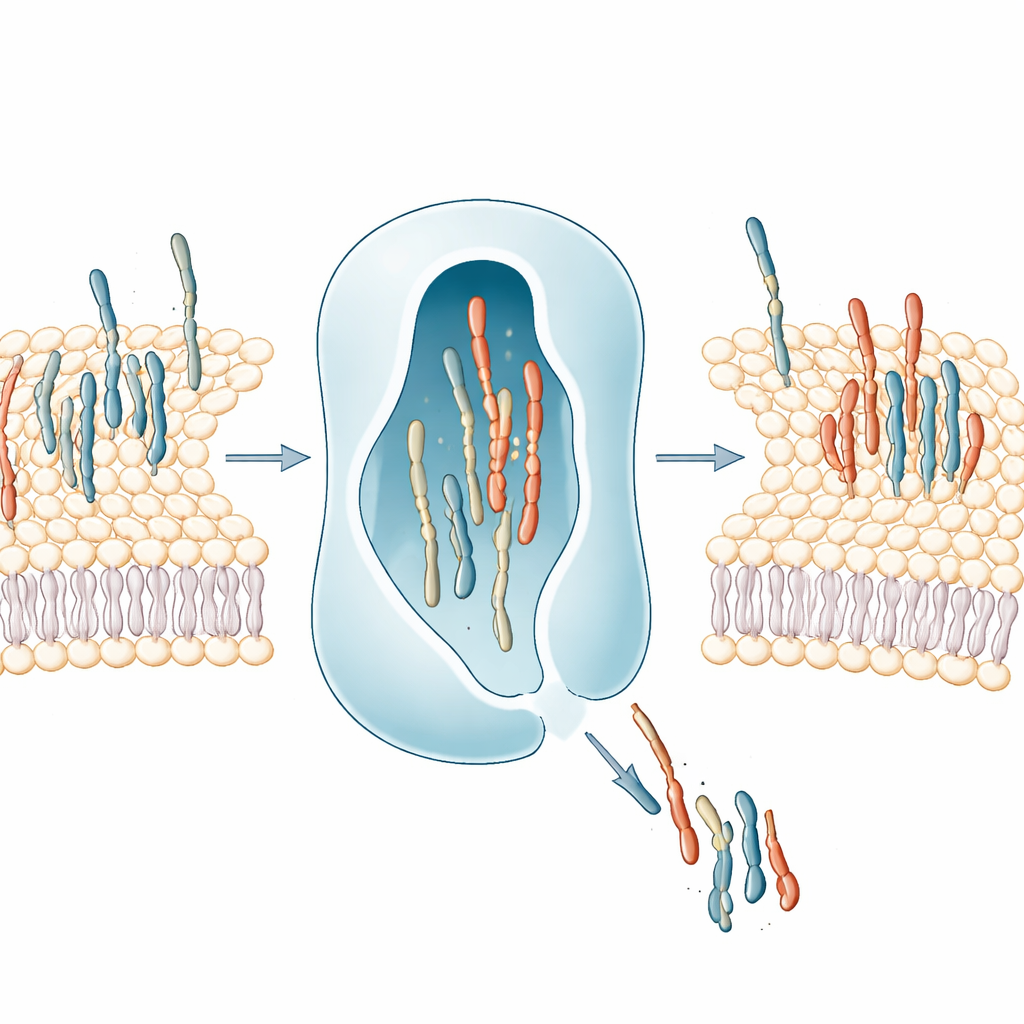
Verbonden lipiden en gecoördineerd celgedrag
De studie onderzocht ook of verschillende lipiden die door dezelfde LTP worden gedragen, onderling verband houden in het leven van een cel. Door hun kaart te vergelijken met grote bestaande datasets vonden de auteurs dat lipiden die door dezelfde LTP worden behandeld de neiging hebben gezamenlijk te stijgen en te dalen wanneer de stofwisseling verstoord is en de neiging hebben op dezelfde plaatsen in cellen en weefsels voor te komen. Dit suggereert dat LTP's groepen lipiden coördineren die samen werken, in plaats van geïsoleerde moleculen te verplaatsen. Met andere woorden, elke LTP kan een klein "netwerk" van vetten definiëren dat als eenheid reist en functioneert.
Waarom dit belangrijk is voor gezondheid en ziekte
Voor niet-specialisten is de kernboodschap dat cellen niet alleen de juiste vetten maken; ze moeten ook zorgvuldig geselecteerde vetsoorten naar de juiste membranen verplaatsen, en dat doen ze met een verrassend veelzijdige gereedschapskist van overdrachtseiwitten. Dit werk levert de eerste brede, experimenteel onderbouwde kaart van welke menselijke LTP's welke lipiden dragen, en onthult eenvoudige regels — zoals een voorkeur voor bepaalde staartlengtes en graden van onverzadigdheid — die bepalen welke leden van het enorme lipidebestand daadwerkelijk mobiel zijn. Omdat veel LTP's en hun lipidepartners gekoppeld zijn aan kanker, immuunresponsen en hersenfunctie, biedt deze bron een uitgangspunt om te begrijpen hoe subtiele veranderingen in vetverkeer zich kunnen verergeren tot ziekte, en om toekomstige therapieën te ontwerpen die deze microscopische shuttles naar gezondere routes sturen.
Bronvermelding: Titeca, K., Chiapparino, A., Hennrich, M.L. et al. Systematic analyses of lipid mobilization by human lipid transfer proteins. Nature 651, 511–520 (2026). https://doi.org/10.1038/s41586-025-10040-y
Trefwoorden: lipidoverdrachtseiwitten, celmembranen, lipidomics, membraanstofwisseling, ceramidetransport