Clear Sky Science · nl
Tumor–hersenen-communicatie remt kankerimmuniteit via een sensorisch–sympathische as
Hoe zenuwen tumoren kunnen helpen zich te verbergen
Kanker wordt meestal voorgesteld als een strijd tussen ontspoorde cellen en het immuunsysteem, maar deze studie onthult een verrassende derde speler: het zenuwstelsel. Onderzoekers tonen aan dat longtumoren kunnen inpluggen op een sensorisch–sympathische zenuwkring die longen en hersenen verbindt, en dat ze die kring vervolgens gebruiken om de natuurlijke antikankerverdediging van het lichaam te verzwakken. Inzicht in deze verborgen “draad” tussen tumoren en de hersenen kan nieuwe behandelroutes openen voor longkanker door zenuwen en hun signalen te richten, en niet alleen de kankercellen zelf. 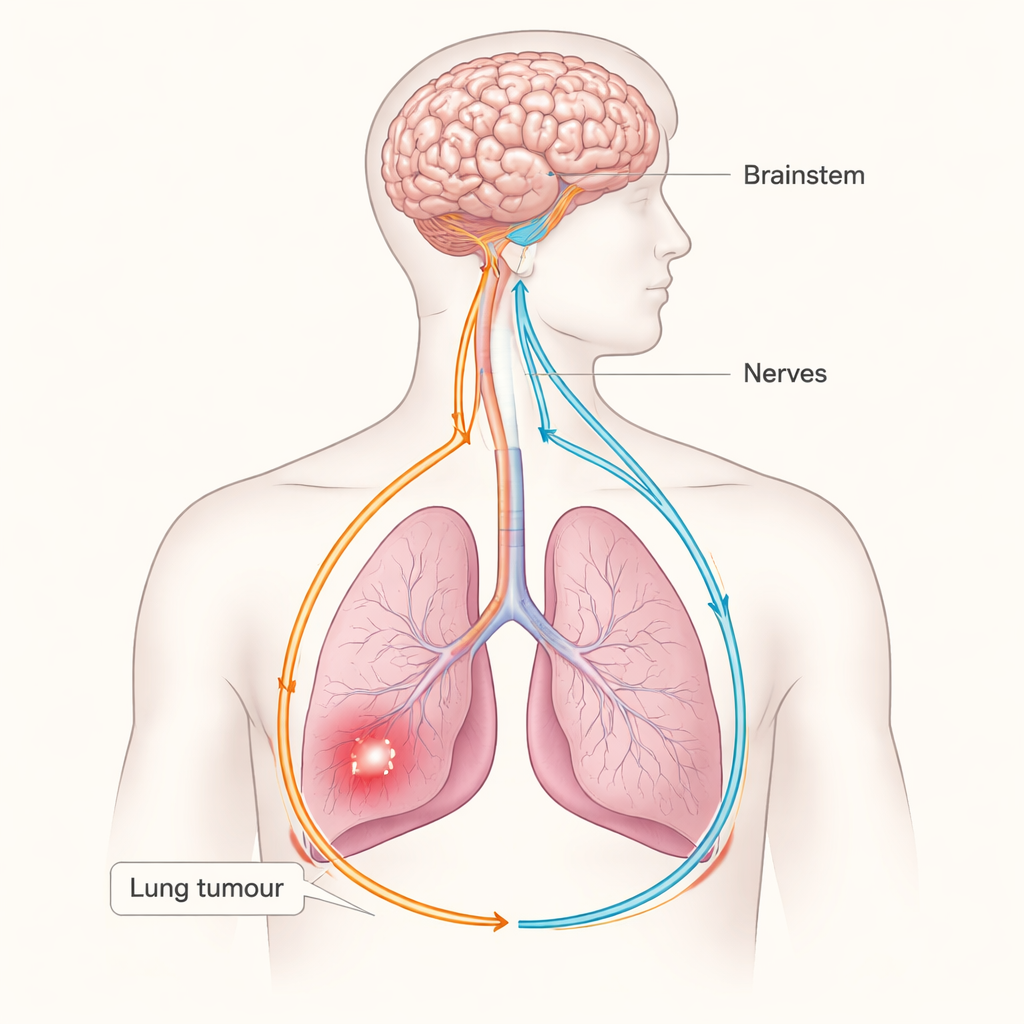
Zenuwen groeien het tumorweefsel in
Het team bestudeerde longadenocarcinoom, een veelvoorkomende vorm van longkanker, in geavanceerde muismodellen die sterk lijken op de menselijke ziekte. Met volledige orgaan-3D-beeldvorming en genetische labels ontdekten ze dat tumoren in de longen sterk vernet zijn met zenuwvezels. Deze zenuwen zijn niet willekeurig: veel afkomstig van een specifieke groep sensorische cellen in de nervus vagus, die normaal informatie over de toestand van de organen naar de hersenen leidt. Tumorcellen scheidden groeibevorderende eiwitten uit, zoals nerve growth factor, die deze vagale sensorische vezels aanmoedigen om uit te lopen en de tumor binnen te dringen. Tegelijkertijd veranderden de sensorische neuronen zelf hun genactiviteit, wat suggereert dat de tumor ze herprogrammeerde zodat ze anders reageren dan in gezond longweefsel.
Een eenrichtingsboost voor tumoraanwezige signalen
Niet alle vagus-gekoppelde sensorische neuronen waren betrokken. De onderzoekers konden een subtype aanwijzen gemarkeerd door twee moleculen, NPY2R en TRPV1, als de belangrijkste spelers. Deze neuronen waren overvloedig in tumorgebieden maar grotendeels afwezig in nabijgelegen normaal longweefsel. Toen de wetenschappers deze NPY2R/TRPV1-groep selectief verwijderden of stillegden—met genetische trucs, gerichte toxines of designerreceptoren die ze met een geneesmiddel konden uitschakelen—krimpten longtumoren drastisch en leefden muizen langer, met beter behoud van gewicht en gedrag. Ter vergelijking: het verwijderen van een ander sensorisch subgroep dat andere longstructuren innerveert vertraagde de tumorgroei niet, wat benadrukt dat slechts een specifiek sensorisch “kanaal” is doorverbonden met controle over kanker. 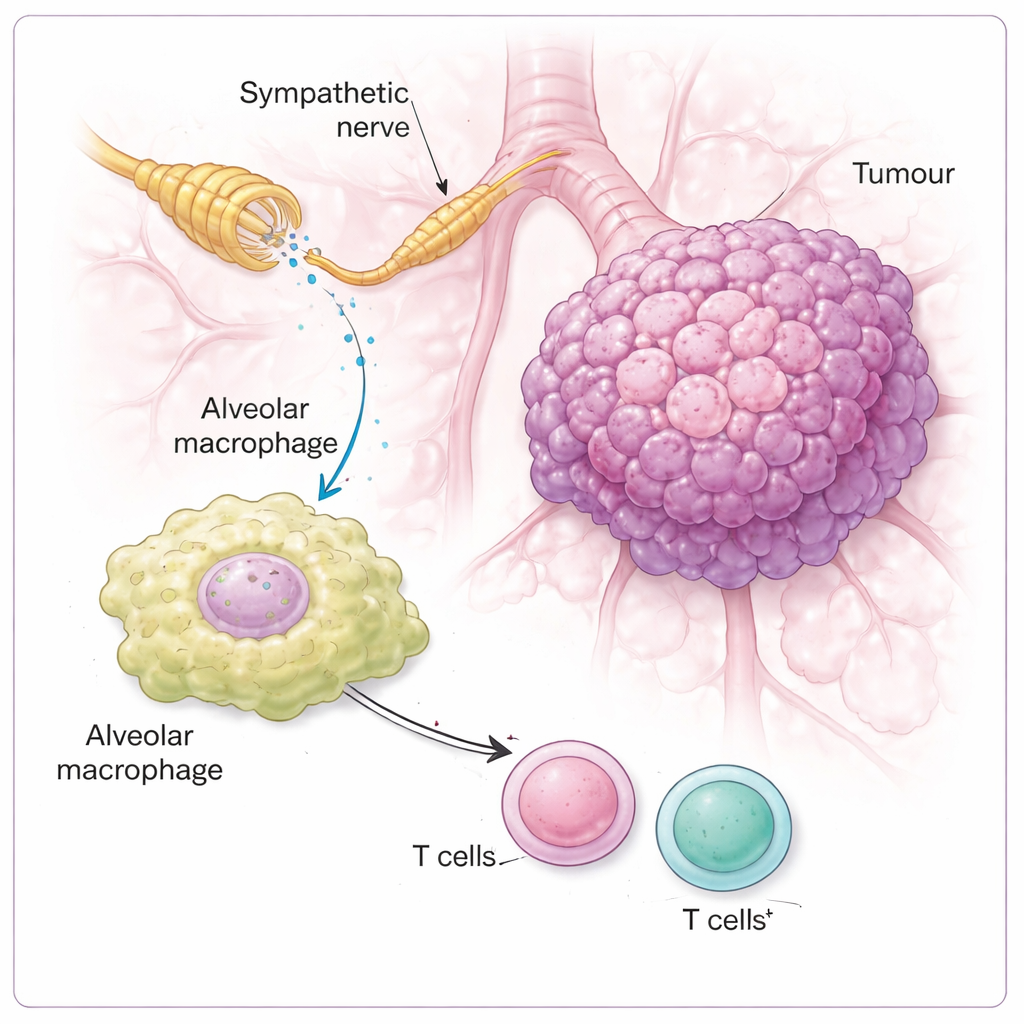
Van hersenstam naar stressachtige signalen in de long
Om te zien hoe deze sensorische signalen door de hersenen worden verwerkt, volgde het team het circuit stroomopwaarts. Activiteitsmarkers toonden aan dat wanneer longtumoren aanwezig waren, hersenstamgebieden die vagale input ontvangen oplichtten, vooral een gebied dat de rostrale ventrolaterale medulla wordt genoemd, een knooppunt dat de sympathische “vecht-of-vlucht”-uitstroom versterkt. Het uitschakelen van de NPY2R/TRPV1-sensorische neuronen bracht deze hersenstamactiviteit tot rust en verminderde het aantal sympathische zenuwvezels en de niveaus van de stressboodschapper noradrenaline in het tumorgebied. Het stilleggen van het hersenstamknooppunt zelf vertraagde ook de tumorgroei. Samen schetsen deze resultaten een gesloten lus: de tumor stimuleert vagale sensorische zenuwen, de hersenstam reageert door sympathische uitgaande activiteit te verhogen, en sympathische zenuwen beïnvloeden de longomgeving op een manier die de kanker bevordert.
Immuuncellen uitschakelen via lokale tussenpersonen
De studie vroeg vervolgens welke cellen in de tumoromgeving daadwerkelijk “luisteren” naar de sympathische signalen. Verrassend genoeg had noradrenaline weinig direct effect op tumorgroei in kweek. In plaats daarvan waren de sleutelverwerkers immuuncellen, vooral alveolaire macrophagen—sentinelcellen die in de longblaasjes zitten. Deze macrophagen droegen hoge niveaus van een receptor genaamd β2-adrenerge receptor, die noradrenaline detecteert. Wanneer deze receptor ontbrak, of wanneer noradrenalinesignaal werd geblokkeerd, groeiden tumoren minder en werd de immuunaanval door T-cellen sterker. Bij muizen met een intact zenuwcircuit duwde noradrenaline macrophagen in een meer onderdrukkende staat, gekenmerkt door hogere niveaus van een enzym genaamd ARG1, dat bekend staat T-cellen te dempen. Zodra macrophagen op deze manier waren hergeprogrammeerd, waren nabijgelegen CD4- en CD8-T-cellen—normaal gesproken de frontlinie van kankerbestrijding—minder goed in staat een sterke respons op te bouwen.
Waarom dit belangrijk is voor de behandeling van kanker
Kort gezegd tonen de auteurs aan dat longtumoren via de nervus vagus met de hersenen kunnen “praten” en een schadelijk antwoord kunnen terugkrijgen via sympathische zenuwen die lokale macrophagen instrueren T-cellen te temmen. Het verbreken van eender welke belangrijke schakel in deze lus—sensorische input, relais in de hersenstam, sympathische output, of β2-adrenerge signalering in macrophagen—was voldoende om sterkere antitumorimmuniteit te herstellen en kanker bij muizen te vertragen. Humane longkankergegevens suggereerden bovendien dat patiënten van wie de tumoren hogere signaturen van deze zenuwbanen vertonen doorgaans slechtere uitkomsten hebben en minder killer-T-cellen in hun tumoren. Het werk werpt de mogelijkheid op dat geneesmiddelen die al worden gebruikt voor hartziekten en angst, zoals bètablokkers, of toekomstige therapieën gericht op specifieke zenuwcircuitries, kunnen worden hergebruikt of verfijnd om de “draden” door te snijden die tumoren gebruiken om aan immuunaanvallen te ontsnappen.
Bronvermelding: Wei, H.K., Yu, C.D., Hu, B. et al. Tumour–brain crosstalk restrains cancer immunity via a sensory–sympathetic axis. Nature 650, 1007–1016 (2026). https://doi.org/10.1038/s41586-025-10028-8
Trefwoorden: kankerneurowetenschap, longkankerimmuniteit, nervus vagus, sympathisch zenuwstelsel, tumormicro-omgeving