Clear Sky Science · nl
Populatie-brede sequencing verklaart bepalende factoren van persistent EBV-DNA
Waarom een veelvoorkomend virus nog steeds van belang is
De meeste volwassenen dragen het Epstein–Barr-virus (EBV), vaak zonder het ooit te weten. Voor sommigen is deze stille metgezel echter gekoppeld aan aandoeningen variërend van klierkoorts tot bepaalde kankers en auto-immuunziekten. Deze studie stelt een eenvoudige maar verstrekkende vraag: kunnen we de enorme verzameling DNA-data die al publiekelijk beschikbaar is gebruiken om te bepalen wie meer EBV in hun bloed draagt, en of hun genen meehelpen te bepalen wie het virus onder controle houdt en wie niet?
Een verborgen viraal spoor in ons DNA lezen
Moderne biobanken, zoals de UK Biobank en het Amerikaanse All of Us-programma, hebben het volledige DNA van honderdduizenden vrijwilligers gesequenced. Deze projecten richtten zich op menselijke genen, maar de ruwe gegevens bevatten ook losse stukjes DNA van virussen. De onderzoekers realiseerden zich dat het referentiegenoom dat voor uitlijning wordt gebruikt een extra "chromosoom" voor EBV bevat. Door opnieuw te kijken naar reads die op dit EBV-segment waren gemapt, konden ze schatten hoeveel kopieën van het EBV-genoom op het moment van monstername in iemands bloed aanwezig waren. Na zorgvuldig een paar misleidende repetitieve regio’s te maskeren, definieerden ze mensen met duidelijk detecteerbare niveaus als dragers van "EBV-DNAëmie"—een meetbare hoeveelheid EBV-DNA circulerend in het bloed.
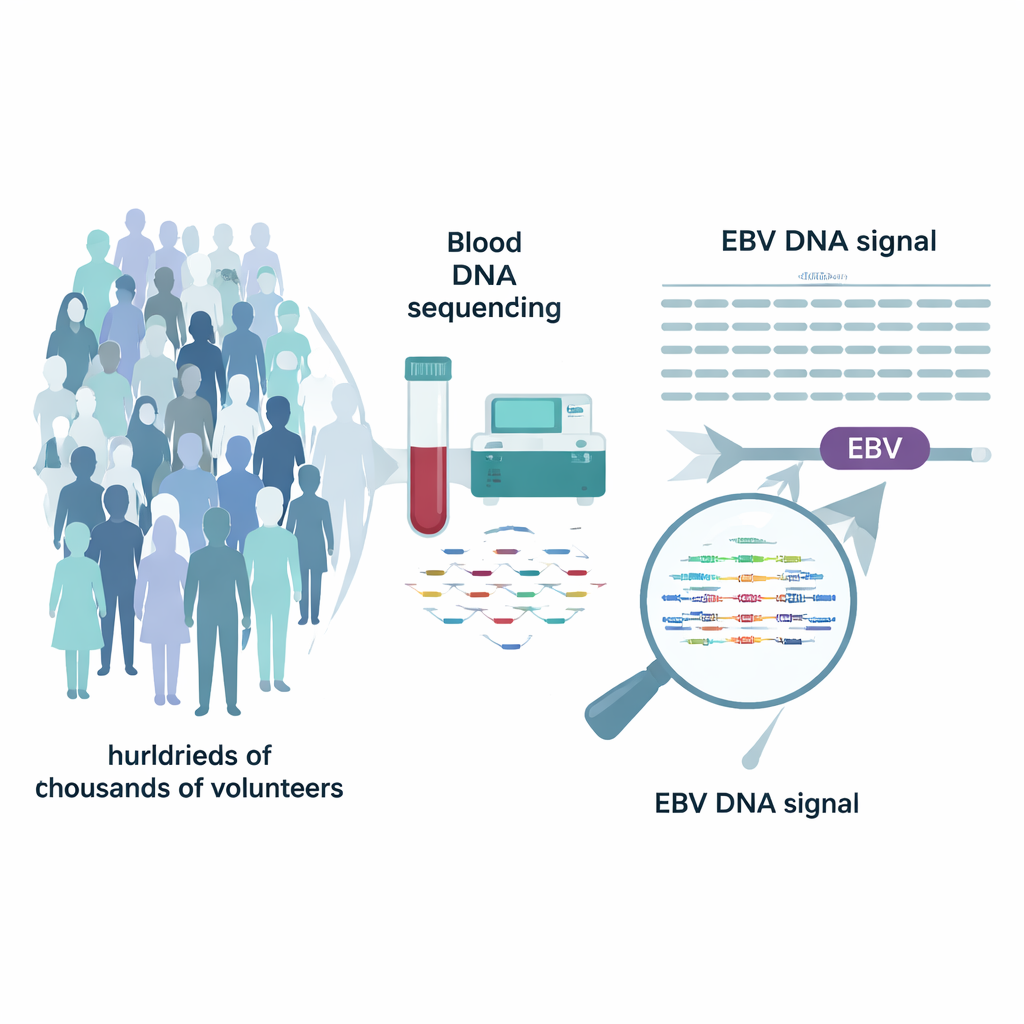
Een kleine minderheid draagt een hoge virale lading
Bij bijna een half miljoen mensen in de UK Biobank en een kwart miljoen in All of Us vond het team dat de meeste volwassenen geen detecteerbaar EBV-DNA in bloed hadden, ook al toonden antistoffentests bij meer dan 90% bewijs van eerdere infectie. Ongeveer 10% van de deelnemers viel echter in een staart van de verdeling met duidelijk verhoogd EBV-DNA. Deze personen waren gemiddeld ouder, vaker man, en iets vaker medicatiegebruikers die het immuunsysteem onderdrukken. Vergelijkbare patronen verschenen in beide cohorten, en in een aparte set speekselmonsters was het virus veel gebruikelijker, wat benadrukt dat EBV in verschillende reservoirs in het lichaam zit en dat bloedmetingen slechts één daarvan weergeven.
Verbanden tussen viraal persisteren en ziekte
Met deze nieuwe biomarker in handen vroegen de auteurs hoe persistent EBV-DNA in bloed samenhangt met gezondheid. Ze doorzochten duizenden diagnoses en laboratoriummetingen om te zien welke vaker voorkwamen bij mensen met EBV-DNAëmie. Sterke associaties verschenen met aandoeningen die al werden vermoed verband te houden met EBV, waaronder Hodgkin-lymfoom, reumatoïde artritis, lupus, chronische obstructieve longziekte en bepaalde longkankers. Er waren ook signalen voor cardiovasculaire problemen, nierfalen, depressie en vermoeidheid, en suggestieve verbanden met zeldzame neurologische aandoeningen zoals neuromyelitis optica. Veel van deze patronen werden gereproduceerd in de onafhankelijke All of Us-cohort. De studie kan niet bewijzen dat EBV deze problemen veroorzaakt, maar toont aan dat hoog EBV-DNA in bloed een merker is van bredere gezondheidsrisico’s en immuondisbalans.
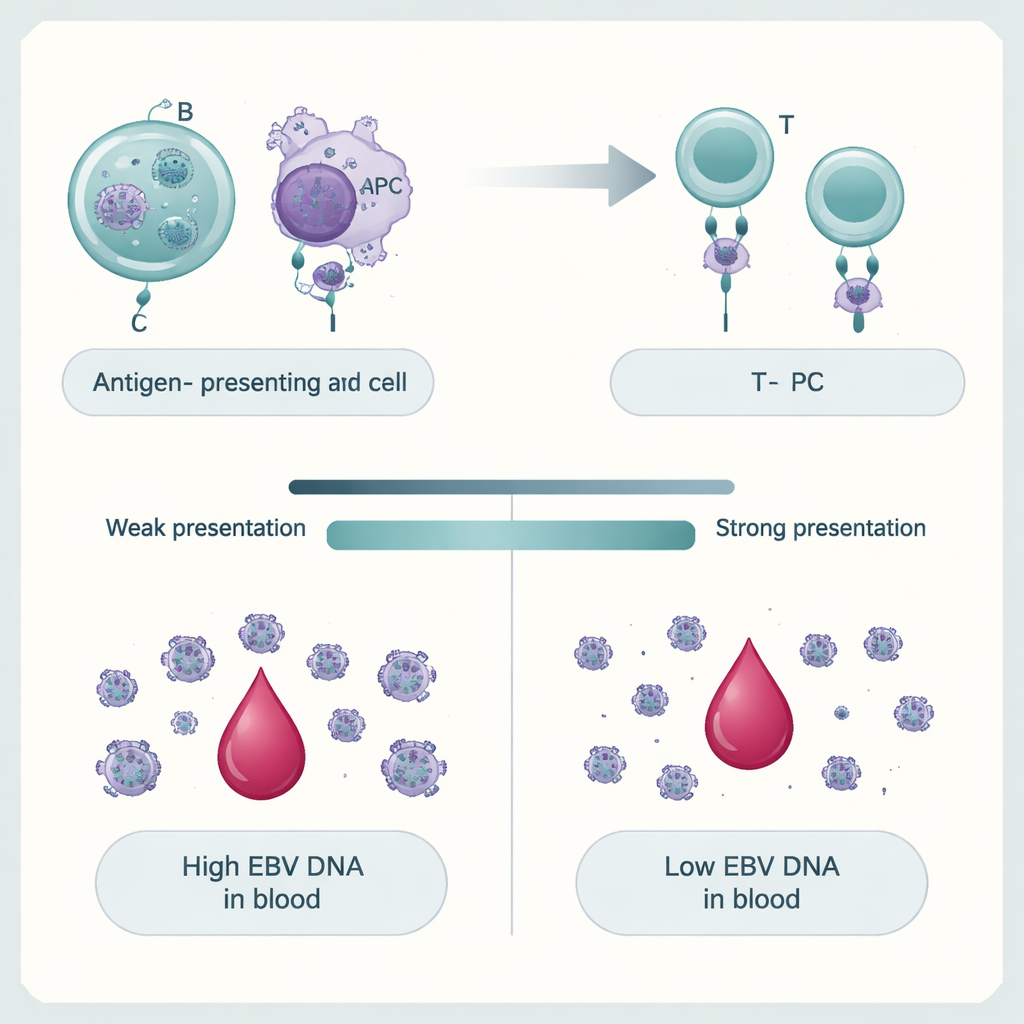
Hoe onze genen de controle over het virus vormen
Het team vroeg vervolgens waarom slechts sommige mensen hoge EBV-DNA-niveaus hebben. Door miljoenen genetische varianten over het genoom te scannen, lieten ze zien dat EBV-DNAëmie een polygeen kenmerk is: veel kleine DNA-verschillen samen sturen virale niveaus omhoog of omlaag. De sterkste signalen clusterden in en rond genen van het major histocompatibility complex (MHC), die immuuncellen helpen virale fragmenten aan T-cellen te tonen. Varianten die deze eiwitten veranderen, met name MHC klasse II-moleculen, waren sterk gekoppeld aan het aanhouden van EBV-DNA. Genen die actief zijn in B-cellen—de belangrijkste langetermijnresidentie van EBV—en andere antigeen-presenterende cellen waren bijzonder verrijkt. Met behulp van computermodellen van hoe verschillende menselijke MHC-varianten stukjes van het EBV-proteoom binden, vonden de auteurs dat versies die voorspeld worden EBV-fragmenten sterker te presenteren, vaak beschermen tegen hoog EBV-DNA, terwijl zwakker presenterende varianten met persisteren geassocieerd waren.
Wat dit betekent voor begrip van infectie
Voor niet-specialisten is de kernboodschap dat onze langdurige balans met EBV niet willekeurig is. Door bestaande populatie-brede DNA-gegevens te ontginnen laat de studie zien dat iemands genetische samenstelling—vooral in immuungenen die virale deeltjes aan T-cellen tonen—helpt bepalen hoeveel EBV in hun bloed aanhoudt. Hoge niveaus markeren een subset van mensen met een verhoogd risico op een reeks immuun-, respiratoire en mogelijk neurologische aandoeningen. Het werk biedt een blauwdruk om oude sequencinggegevens om te zetten in nieuwe inzichten over de vele virussen die in ons lichaam leven, en suggereert dat gerichte strategieën om effectieve antigeenpresentatie te versterken of te imiteren ooit kunnen helpen om levenslange infecties zoals EBV beter onder controle te houden.
Bronvermelding: Nyeo, S.S., Cumming, E.M., Burren, O.S. et al. Population-scale sequencing resolves determinants of persistent EBV DNA. Nature 650, 664–672 (2026). https://doi.org/10.1038/s41586-025-10020-2
Trefwoorden: Epstein–Barr-virus, viraal persisteren, menselijke genetica, auto-immuunziekte, biobank-sequencing