Clear Sky Science · nl
Gepersonaliseerde mRNA‑vaccins wekken duurzame T‑celimmuniteit op bij adjuvante TNBC
Nieuwe hoop na borstkankerbehandeling
Voor veel vrouwen met een agressieve vorm van borstkanker, genaamd triple‑negatieve borstkanker, houdt de angst niet op wanneer chemotherapie en operatie voorbij zijn. Deze kanker heeft een hoog risico op terugkeer en uitzaaiing, vaak binnen slechts enkele jaren. De hier beschreven studie onderzoekt een sterk gepersonaliseerd vaccin, gemaakt van de mutaties in het eigen tumorweefsel van elke patiënt, om te bepalen of het het immuunsysteem jarenlang in staat kan stellen waakzaam te blijven en de kans op terugval na de standaardbehandeling kan verlagen.
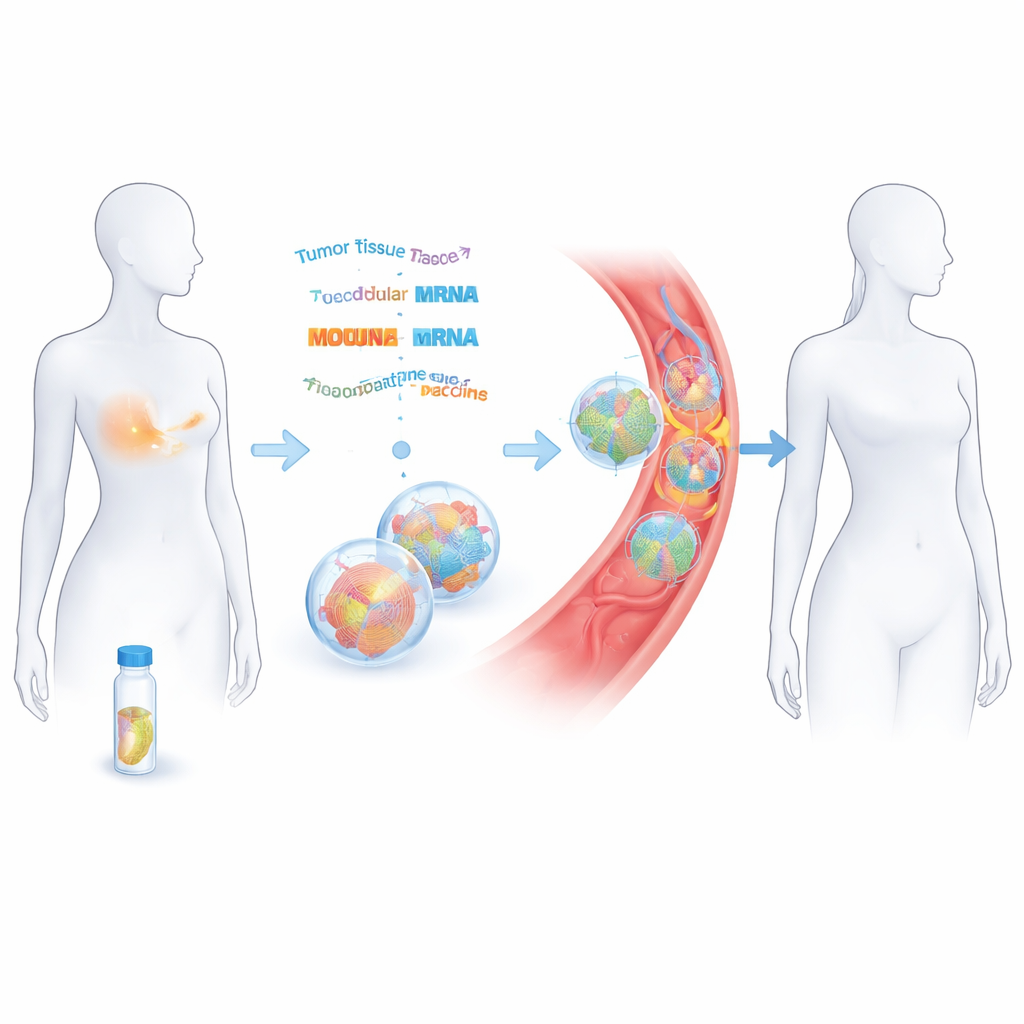
Een verwijderde tumor omzetten in een op maat gemaakt vaccin
De onderzoekers werkten met 14 vrouwen met vroeg‑stadium triple‑negatieve borstkanker die al chirurgie en chemotherapie met curatief doel hadden ondergaan. Uit het verwijderde tumorweefsel bepaalden ze DNA en RNA om de unieke mutaties van de kanker in kaart te brengen. Met computertools voorspellen ze welke van deze veranderingen door immuuncellen als vreemd zouden kunnen worden herkend. Tot 20 van deze "neoantigenen" werden vervolgens aaneengeschakeld en gecodeerd in twee strengen boodschapper‑RNA (mRNA), in principe vergelijkbaar met COVID‑19‑vaccins maar afgestemd op elke patiënt. Deze mRNA‑strengen werden verpakt in kleine vetbellen en via de ader toegediend in acht doses over ongeveer twee maanden.
Hoe het vaccin immuunverdedigers wekt
Eens in het lichaam instrueren de mRNA‑moleculen immuunwachters genaamd dendritische cellen om tijdelijk de neoantigeen‑eiwitten te maken en fragmenten daarvan aan hun oppervlak te tonen. Dit werkt als een gezochte‑poster voor T‑cellen, de belangrijkste kankerdodende kracht van het immuunsysteem. Het team nam bloed af vóór vaccinatie en op meerdere tijdstippen daarna om te testen of neoantigeenspecifieke T‑cellen verschenen en hoe sterk die waren. Met gevoelige laboratoriumtesten vonden ze dat elke patiënt nieuwe of versterkte T‑celreacties ontwikkelde tegen ten minste één van de geselecteerde mutaties, en de meeste reageerden op meerdere. In veel gevallen waren grote fracties van circulerende T‑cellen — niveaus die gewoonlijk alleen bij krachtige celtherapieën worden gezien — nu afgestemd om tumorspecifieke doelen te herkennen.
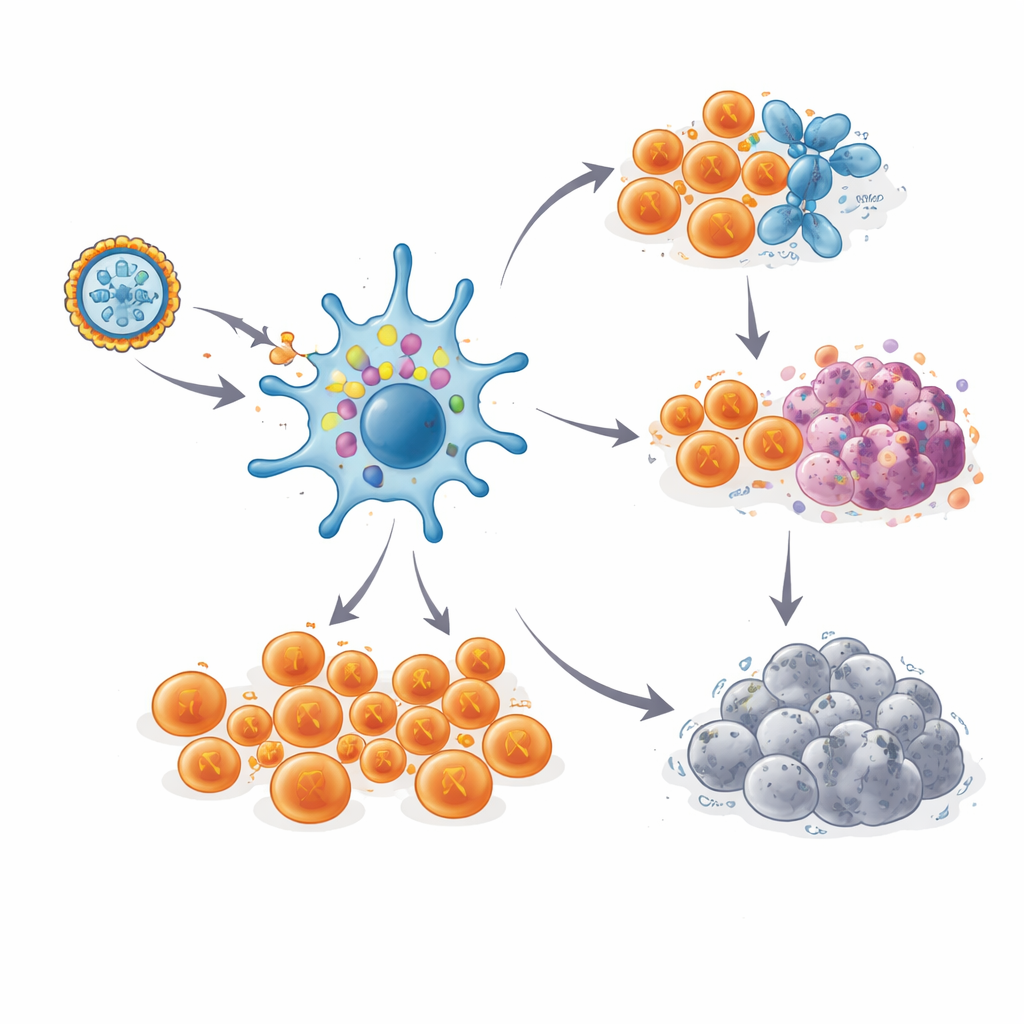
Duurend immuun‑geheugen
Belangrijk is dat deze T‑celreacties niet snel verdwenen. Bij de meeste patiënten piekten sterke responsen tijdens de vaccinatieperiode, zakten iets en bleven daarna op hoge niveaus gedurende één tot drieënhalf jaar, zelfs zonder boosterdoses. Door de unieke receptor‑"barcodes" van individuele T‑celclonen te volgen, konden de wetenschappers specifieke neoantigeen‑reactieve cellen tot zes jaar volgen bij één patiënt die kankervrij bleef. Gedetailleerde single‑cell‑analyses toonden twee belangrijke bestemmingen voor deze cellen. Velen werden hooggeëquipeerde doder‑T‑cellen, klaar om elke cel met het juiste neoantigeen te vernietigen. Anderen ontwikkelden zich tot een zeldzamere, stam‑achtige geheugengroep met merkers van zelfvernieuwing, wat wijst op een reservoir dat nieuwe golven strijders kan regenereren als kankercellen terugkeren.
Wat er met de patiënten gebeurde
Na een mediaan van iets meer dan vijf jaar follow‑up vanaf de eerste vaccindosis hadden elf van de veertien vrouwen geen terugkeer van hun kanker ervaren; één van hen overleed aan niet‑gerelateerde oorzaken terwijl ze nog in remissie was. Drie vrouwen kregen wel een recidief, en hun gevallen geven aanwijzingen waarom een gepersonaliseerd vaccin soms kan falen. Eén patiënt ontwikkelde slechts een zwakke T‑celrespons en profiteerde later van een andere immunotherapie, een anti‑PD‑1‑antilichaam, maar overleed uiteindelijk aan wijdverspreide ziekte. Een tweede patiënt had een erfelijk risico en tumoren in beide borsten; alleen één tumor werd gebruikt voor het ontwerp van het vaccin, en later toonde bewijs dat het recidief afkomstig was van de genetisch verschillende, niet‑gevaccineerde tumor. De derde patiënt had sterke door het vaccin geïnduceerde T‑cellen die de teruggekeerde tumor infiltreerden, maar de kankercellen waren grotendeels sleutel‑moleculen kwijtgeraakt die nodig zijn om neoantigenen op hun oppervlak te tonen, en ontweken zo de immuunaanval.
Waarom dit werk ertoe doet voor de toekomst
Deze vroeg‑fase studie was klein en had geen controlegroep, dus ze kan niet bewijzen dat het vaccin op zichzelf terugval heeft voorkomen. Desondanks toont ze dat het bouwen van een complex, op maat gemaakt mRNA‑vaccin uit het eigen tumorweefsel van een patiënt uitvoerbaar is in reguliere ziekenhuissituaties, over het algemeen goed wordt verdragen en krachtige, langlevende T‑cellegers tegen meerdere kankerspecifieke doelen kan opwekken. De bevindingen benadrukken ook ontsnappingsroutes die tumoren kunnen gebruiken, zoals het verliezen van hun antigenpresentatiemachinerie of ontstaan uit niet‑getargete letsels, wat wijst op combinaties met andere immuuntherapieën en uitgebreider tumorsequencen. Voor patiënten met triple‑negatieve borstkanker suggereert dit werk dat een op maat gemaakt vaccin, gegeven na de standaardbehandeling, de ziekte mogelijk in de toekomst kan helpen tegenhouden door hun eigen immuunsysteem om te vormen tot een duurzame, zeer specifieke verdedigingslinie.
Bronvermelding: Sahin, U., Schmidt, M., Derhovanessian, E. et al. Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC. Nature 651, 1088–1096 (2026). https://doi.org/10.1038/s41586-025-10004-2
Trefwoorden: triple‑negatieve borstkanker, mRNA kanker‑vaccins, neoantigeen‑immunotherapie, T‑celimmuniteit, tumorrecidief