Clear Sky Science · nl
Polyamine-afhankelijke metabolische bescherming reguleert alternatieve splicing
Hoe kleine moleculen cellen helpen hun genen te lezen
In elke cel kan hetzelfde DNA-script op veel manieren gelezen worden, waardoor een beperkt aantal genen een enorme verscheidenheid aan eiwitten kan voortbrengen. Deze flexibiliteit berust op een proces dat alternatieve splicing heet, waarbij RNA-boodschappen worden bewerkt voordat ze in eiwitten worden omgezet. Dit artikel onthult dat kleine, positief geladen moleculen—polyaminen—stille invloed uitoefenen op deze bewerkingsstap en fungeren als een soort beschermend schild dat cellen helpt beslissen welke RNA-versies gemaakt worden. Omdat alternatieve splicing cruciaal is bij kanker, hersenfunctie en stamcellen, heeft het blootleggen van deze verborgen regulatielaag verstrekkende gevolgen voor gezondheid en ziekte.
Kleine geladen helpers in elke cel
Polyaminen zijn kleine, flexibele moleculen met meerdere positieve ladingen. Cellen maken ze uit eenvoudige voedingsstoffen en ze zijn lang bekend als hulpjes voor groei en overleving, vooral in snel delende cellen zoals tumoren. De auteurs vroegen zich af of polyaminen ook als signalen fungeren, en niet alleen als brandstof. Door de polyamineproductie gedeeltelijk te blokkeren in prostaatkankercellen en in muizen, volgden ze hoe eiwitten en RNA in de loop van de tijd veranderden. Ze vonden dat lang voordat de totale polyaminespiegels drastisch daalden, er een sterke golf van veranderingen in eiwitfosforylering optrad—chemische labels die eiwitschakelaars aan- of uitzetten—vooral op componenten van het cellulaire RNA-bewerkingsapparaat, het spliceosoom.
Het herschakelen van de RNA-editor van de cel
Specifiek kijkend naar RNA gebruikte het team diepe sequencing om alternatieve splicing te volgen wanneer de polyaminesynthese werd geremd. Honderden RNA-segmenten werden anders overgeslagen of opgenomen, in kankercellijnen, normale celtypen en muisweefsels. Deze veranderingen waren niet louter bijproducten van vertraagde celdeling of van een ander bekend polyamine-afhankelijk proces, hypusinering. In plaats daarvan herstelden veel splicing-veranderingen zich toen de onderzoekers cellen van buitenaf weer polyaminen voorzagen. Zowel geneesmiddelen als genetische hulpmiddelen die polyaminen verlaagden, resulteerden in vergelijkbare splicingpatronen, en het verder verlagen van polyaminen met een combinatiedosering versterkte de veranderingen, wat bevestigt dat het effect nauw verbonden is met de beschikbaarheid van polyaminen.
Een verborgen doelwit: de SF3-spliceermodule
Om uit te zoeken waar in het splicingmachinerie polyaminen werkzaam zijn, vergeleken de auteurs het splicinghandtekening veroorzaakt door polyamineverlaging met een uitgebreide referentiemap die werd gemaakt door meer dan 300 bekende splicingfactoren één voor één uit te schakelen. De dichtstbijzijnde overeenkomst wees op een specifiek deel van het spliceosoom, het SF3-subcomplex, dat helpt sleutel-signalen in RNA te herkennen. Computationele analyse van publieke eiwit–RNA-bindingsgegevens ondersteunde deze koppeling: RNA-moleculen waarvan de splicing werd veranderd door polyaminetekort, werden bijzonder vaak gebonden door SF3-eiwitten. Toen het team SF3-componenten gedeeltelijk uitschakelde, zowel genetisch als met een medicijn, werden de splicing-effecten van polyamine-uitputting grotendeels tenietgedaan, wat laat zien dat intacte SF3-activiteit vereist is voor deze nieuwe regulatoire route. 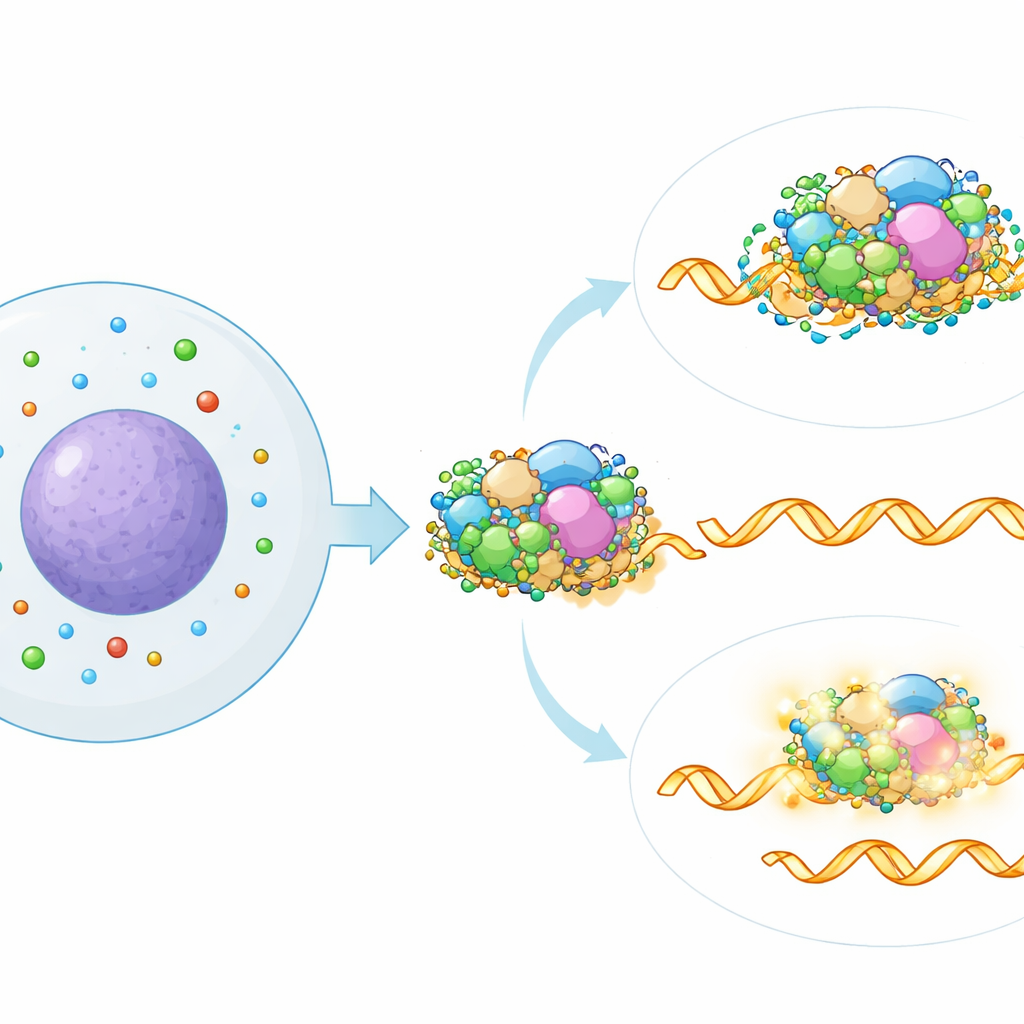
Metabolische bescherming: hoe polyaminen eiwitlabeling blokkeren
Dieper gravend merkten de onderzoekers dat de meest sterk aangetaste fosforyleringsplaatsen op SF3-eiwitten zich concentreerden in korte reeksen die rijk zijn aan negatief geladen aminozuren. Moleculair modelleren en kernspinresonantie-experimenten toonden aan dat polyaminen in deze zure patchen nestelen, meerdere elektrostatische contacten vormen en gedeeltelijk nabijgelegen serineresiduen bedekken waar normaal gesproken fosfaatgroepen worden toegevoegd. Deze fysieke "omhelzing" vermindert de toegankelijkheid van deze plekken voor proteïnekinasen—de enzymen die fosfaten aanhechten. In proefbuisexperimenten blokkeerden toegevoegde polyaminen direct een kinase genaamd CK1 om SF3-eiwitten te fosforyleren. In cellen dempte het remmen van CK1 en zijn nauwe verwant CK2 de splicingveranderingen veroorzaakt door polyamineverlies, en speciaal geconstrueerde muizen waarvan het SF3A3-eiwit drie belangrijke fosforyleringsplaatsen miste, werden grotendeels ongevoelig voor polyamine-afhankelijke splicingverschuivingen. 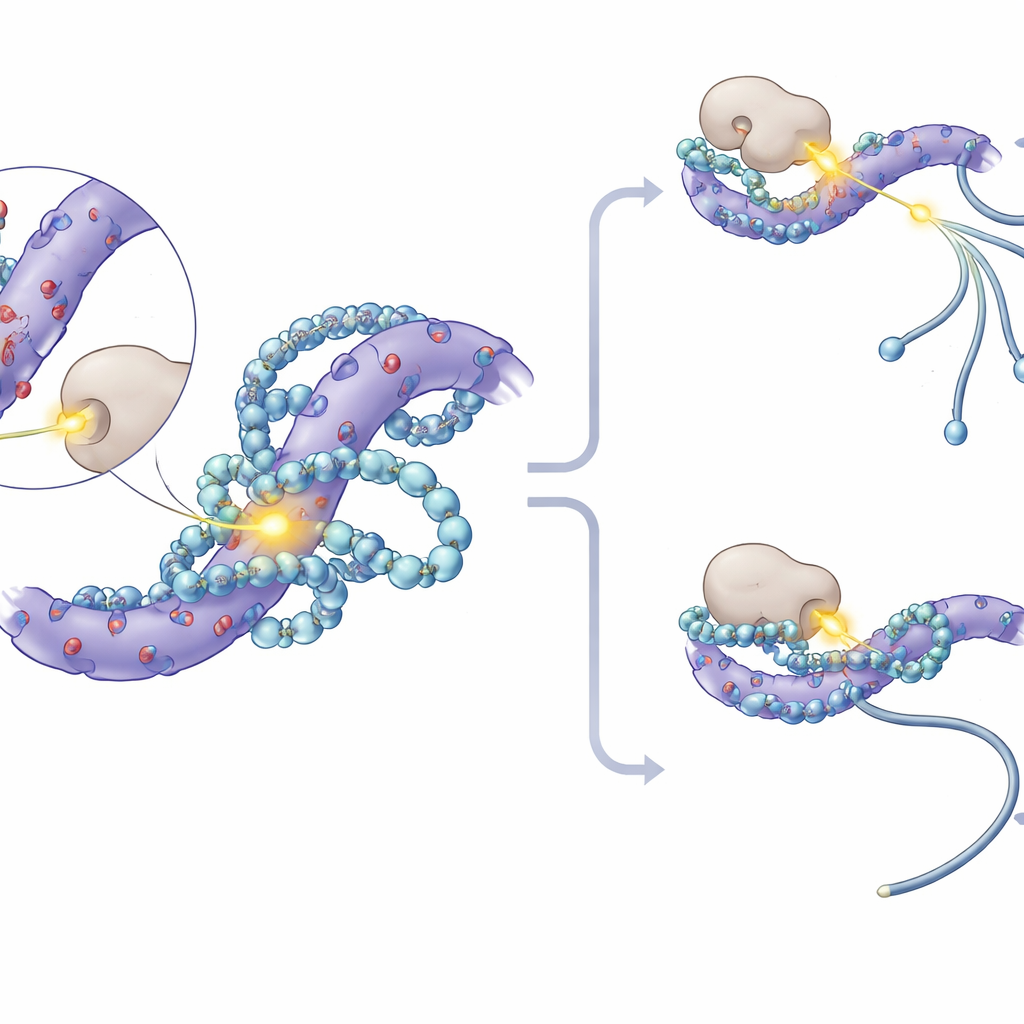
Een ontworpen molecuul dat functies scheidt
De studie introduceert ook een polyamine-achtig middel, BENSpm, dat sterker positief geladen is maar tegelijkertijd de eigen polyamineproductie van de cel uitschakelt. BENSpm bond strak aan de zure patchen van SF3 en blokkeerde kinase-activiteit, net als natuurlijke polyaminen, maar het herstelde de celgroei niet wanneer gewone polyaminen schaars waren. Dit stelde de auteurs in staat klassieke polyaminefuncties (ondersteunen van groei en metabolisme) te scheiden van de nieuw gedefinieerde beschermingsrol. In embryonale muisstamcellen duwde uitputting van polyaminen de cellen richting verlies van hun "stemness"-marker Nanog en wijzigde hun splicinglandschap. BENSpm herstelde zowel het splicingprofiel als Nanog-expressie ondanks aanhoudende onderdrukking van de normale polyaminesynthese, wat aangeeft dat metabole bescherming essentieel is voor het behoud van stamcelidentiteit.
Waarom deze ontdekking ertoe doet
In gewone bewoordingen laat dit werk zien dat polyaminen fungeren als kleine beschermende handschoenen rond gevoelige delen van belangrijke splicingeiwitten. Als de handschoenen aan zijn, kunnen kinasen die plaatsen niet makkelijk vastpakken en labelen, en blijft de RNA-bewerking op koers. Als polyaminen laag zijn, gaan de handschoenen af, stijgt de fosforylering en verschuiven splicingpatronen, met consequenties voor zowel kankercellen als stamcellen. Door dit "metabolische schild"-mechanisme te definiëren en een hulpmolecuul te bieden dat het selectief nabootst, opent de studie de deur naar nieuwe manieren om het aflezen van genen bij te sturen zonder het DNA zelf te veranderen, wat mogelijk toekomstige therapieën inspireert die splicing in kanker en regeneratieve geneeskunde gericht aanpakken.
Bronvermelding: Zabala-Letona, A., Pujana-Vaquerizo, M., Martinez-Laosa, B. et al. Polyamine-dependent metabolic shielding regulates alternative splicing. Nature 651, 819–828 (2026). https://doi.org/10.1038/s41586-025-09965-1
Trefwoorden: polyaminen, alternatieve splicing, RNA-verwerking, metabole signalering, stamcelregulatie