Clear Sky Science · nl
Veelvoorkomende variatie in meiosesgenen bepaalt menselijke recombinatie en aneuploïdie
Waarom fouten in chromosomen van embryo’s ertoe doen
Veel zwangerschappen eindigen nog voordat ze worden opgemerkt, vaak omdat een embryo het verkeerde aantal chromosomen draagt. Deze studie stelt een ogenschijnlijk eenvoudige maar ingrijpende vraag voor vruchtbaarheid en reproductieve gezondheid: hoe beïnvloeden alledaagse DNA-verschillen tussen mensen de manier waarop eicellen en zaadcellen chromosomen herschikken en delen, en hoe beïnvloedt dat op zijn beurt de kans dat een embryo er te veel of te weinig heeft? Door meer dan honderdduizend in vitro fertilisatie(IVF)-embryo’s te onderzoeken, laten de auteurs zien hoe veelvoorkomende genetische variatie in een handvol genen de kansen subtiel kan verschuiven richting of weg van deze chromosoomfouten.
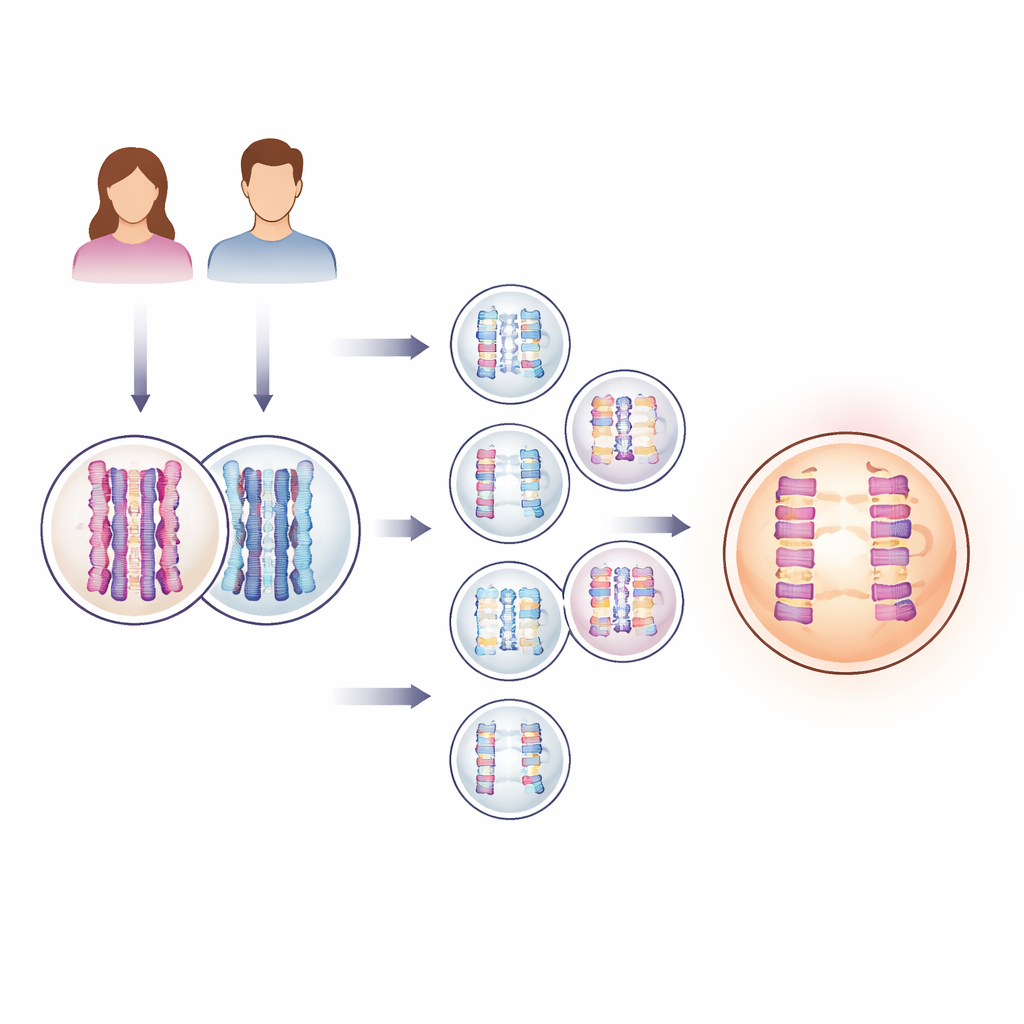
Inzicht in duizenden IVF-embryo’s
Om een probleem aan te pakken dat meestal onzichtbaar in het menselijk lichaam plaatsvindt, gebruikten de onderzoekers genetische testgegevens die routinematig tijdens IVF worden verzameld. Klinieken nemen vaak een biopsie van een paar cellen uit een embryo enkele dagen na bevruchting om chromosoomproblemen te controleren vóór terugplaatsing. In deze studie analyseerde het team DNA van 139.416 zulke embryo’s, samen met DNA van bijna 23.000 paren biologische ouders. Met een statistische methode die blokken ouderlijk DNA volgt terwijl ze in embryo’s terechtkomen, konden ze zowel het aantal ‘crossovers’ tellen — de punten waar ouderlijke chromosomen segmenten uitwisselen — als detecteren wanneer een embryo een heel chromosoom had gewonnen of verloren, een toestand die aneuploïdie wordt genoemd.
Hoe vaak komen chromosoomfouten voor en wat bepaalt ze?
De enquête toonde aan dat bijna 30% van de embryo’s ten minste één aneuploid chromosoom droeg. De meeste van deze fouten kwamen van de moeder in plaats van de vader en betroffen vaak specifieke chromosomen die al bekendstaan als gevoelig. Zoals uit de klinische praktijk verwacht, steeg het aandeel embryo’s met maternale chromosoomfouten sterk met de leeftijd van de moeder, terwijl de leeftijd van de vader weinig effect had. Cruciaal is dat, wanneer het team embryo’s met normale chromosoomaantallen vergeleek met die met fouten, ze vonden dat de foutgevoelige embryo’s de neiging hadden minder crossovers te hebben op hun verder normale chromosomen. Dit ondersteunt het idee dat crossovers een dubbele rol vervullen: ze genereren nieuwe genetische combinaties, maar werken ook als fysieke verbindingen die helpen dat chromosomen netjes van elkaar scheiden tijdens de eivorming.
Alledaagse genetische verschillen in sleutelgenen zijn van belang
Vervolgens doorzochten de auteurs het genoom van de moeders op veelvoorkomende DNA-varianten die correleerden met hoe vaak hun embryo’s aneuploid waren. Een opvallend gebied lag in de buurt van een gen dat SMC1B heet, dat deel uitmaakt van een ringvormig proteïnecomplex dat zusterchromatiden in eicellen samenhoudt. Vrouwen die een bepaalde versie van dit DNA-stuk droegen, hadden een iets hoger aandeel embryo’s met maternale chromosoomfouten, en dit risico nam toe met de leeftijd. Vervolganalyses in grote genexpressiedatasets toonden dat de risicovariant van de DNA-sequentie samenhangt met lagere activiteit van SMC1B, blijkbaar door subtiele veranderingen in hoe een transcriptiefactor aan zijn promotor bindt. Met andere woorden: een veelvoorkomende, niet-destructieve aanpassing van een regelgevend schakelaartje kan de cohesie-eiwitactiviteit net genoeg verlagen om de kans op chromosoommisverdeling meetbaar te vergroten.
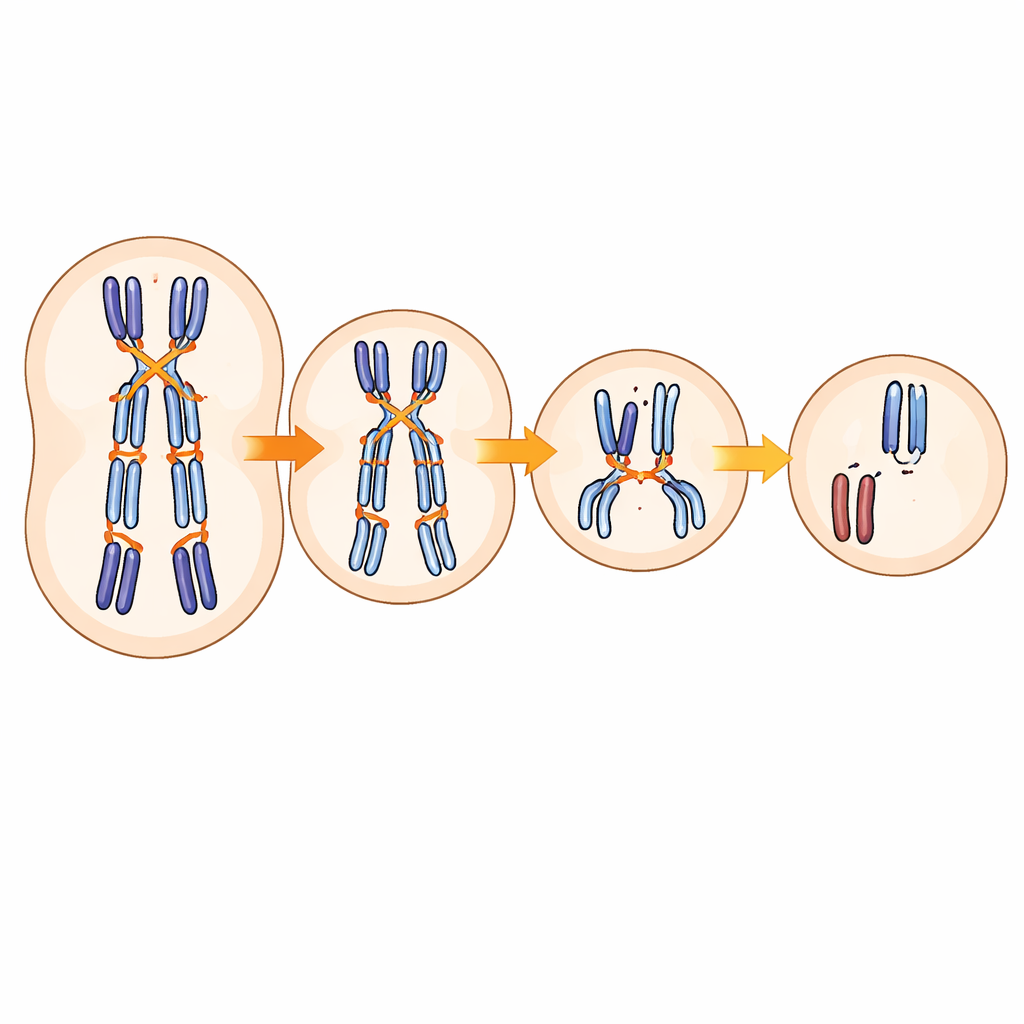
Een gedeelde genetische draad door vruchtbaarheidskenmerken
Buiten SMC1B benadrukte de studie ook andere genen die helpen chromosomen tijdens de meiose uitlijnen en verbinden, waaronder componenten van het skelet dat gepaarde chromosomen bij elkaar brengt en enzymen die markeren waar crossovers zullen optreden. Varianten in deze genen beïnvloedden niet alleen recombinatiepatronen en aneuploïdirisico in embryo’s, maar toonden ook verbanden met de timing van de puberteit en de menopauze in grote populatiestudies. Toch verklaarden veelvoorkomende varianten samen maar een klein deel van de totale variatie in chromosoomfouten bij embryo’s. Dit suggereert dat omgeving, toevallige gebeurtenissen tijdens eicelontwikkeling en zeldzamere genetische veranderingen waarschijnlijk grote rollen spelen, zelfs wanneer veel van deze invloeden samenkomen op dezelfde moleculaire mechanismen.
Wat dit betekent voor menselijke vruchtbaarheid en evolutie
Voor niet-specialisten is de kernboodschap dat dezelfde genetische processen die gezonde diversiteit in ons DNA creëren, wanneer ze in subtiel verschillende standen staan, ook het risico op vroeg verlies van een zwangerschap kunnen vergroten. Dit werk laat zien dat gewone erfelijke verschillen in een paar meiotische genen het evenwicht bescheiden kunnen verschuiven, vooral naarmate vrouwen ouder worden, maar geen enkele variant bepaalt iemands voortplantingslot. Door enorme embryo-datasets met populatiegenetica te combineren, gaat de studie ook in op een evolutionair raadsel: waarom varianten die het risico op niet-levensvatbare embryo’s verhogen, in mensen gewoon kunnen blijven voorkomen. De auteurs betogen dat omdat veel sociale en omgevingsfactoren de relatie tussen aantal embryo’s en uiteindelijke gezinsgrootte vertroebelen, natuurlijke selectie dergelijke varianten mogelijk niet effectief uitroept. Samen verdiepen deze inzichten ons begrip van waarom chromosoomfouten zo vaak voorkomen in de menselijke voortplanting en wijzen ze op biologische paden die uiteindelijk advies of interventies zouden kunnen informeren.
Bronvermelding: Carioscia, S.A., Biddanda, A., Starostik, M.R. et al. Common variation in meiosis genes shapes human recombination and aneuploidy. Nature 651, 146–153 (2026). https://doi.org/10.1038/s41586-025-09964-2
Trefwoorden: aneuploïdie, meiose, menselijke vruchtbaarheid, chromosoomrecombinatie, SMC1B