Clear Sky Science · nl
Ligand-specifieke activatietrajecten bepalen GPCR-signaaloverdracht in cellen
Hoe één receptor zich als veel schakelaars kan gedragen
Veel huidige geneesmiddelen werken op een grote familie van membraanproteïnen die G-eiwitgekoppelde receptoren of GPCR’s worden genoemd. Deze receptoren beïnvloeden hartslag, stemming, ademhaling en talloze andere lichaamsfuncties. Decennialang werden ze gezien als simpele aan/uit-schakelaars: een medicijn bindt, de schakelaar gaat om en er stroomt een signaal de cel in. Dit artikel laat zien dat de werkelijkheid veel rijker is. Met een nieuw type fluorescerende "spion" direct ingebouwd in een receptor volgen de auteurs in levende cellen hoe verschillende medicijnen dezelfde receptor langs uiteenlopende activatiepaden sturen — alsof ze verschillende routes door een stad kiezen — wat uiteenlopende signaalpatronen oplevert. Het begrijpen van deze verborgen routes kan helpen bij het ontwerpen van medicijnen die het gewenste voordeel geven en bijwerkingen vermijden.
De deurbel van een cel in realtime bekijken
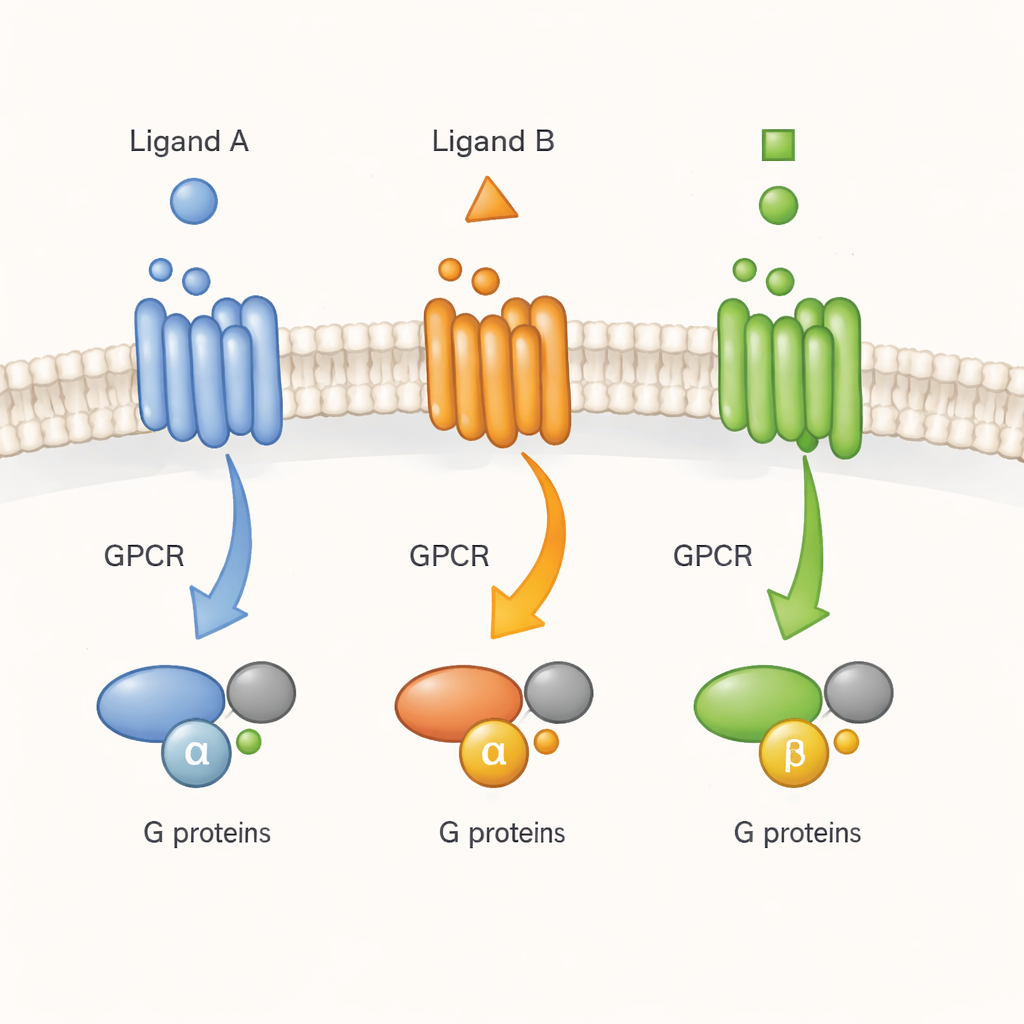
GPCR’s worden vaak beschreven als moleculaire deurbel: een signaalmolecuul (een ligand) belt van buitenaf en de receptor geeft het bericht door aan G-eiwitten aan de binnenkant. Vroeger werk met gezuiverde receptoren in detergentia suggereerde dat GPCR’s niet simpelweg omschakelen tussen één inactieve en één actieve vorm. In plaats daarvan nemen ze vele vormen aan die medicijnen tot verschillende graden kunnen stabiliseren. Maar het was onduidelijk of diezelfde complexiteit ook in de drukke, dynamische omgeving van een levende cel bestaat. Hier richten de auteurs zich op één representatieve receptor, de M2 muscarine acetylcholinereceptor, een belangrijke regulator van hart- en zenuwactiviteit, en onderzoeken ze of verschillende liganden de receptor in verschillende actieve vormen sturen die van belang zijn voor daadwerkelijke cellulaire signaaloverdracht.
Kleine lichtgevers op het receptormembraan bouwen
Om de bewegingen van de receptor te volgen zonder zijn normale functie te verstoren, gebruikte het team uitbreiding van de genetische code, een techniek waarmee zij een speciaal ontworpen aminozuur op geselecteerde posities aan de buitenzijde van de receptor konden inbouwen. Dit chemische "anker" kan in levende cellen aangeklikt worden aan een kleine fluorescerende kleurstof. Door 72 posities te scannen en alleen die te behouden die zich nog als normale receptoren gedroegen, bouwden zij een paneel van zeven M2-receptorvarianten, elk met één kleurstof op een andere buitenlusplaats. Wanneer de natuurlijke boodschapper acetylcholine werd toegepast, nam de helderheid van de kleurstof op die plaatsen op karakteristieke wijze toe of af, wat liet zien hoe elk deel van het buitenoppervlak van de receptor verschoof bij aanvang van de signaaloverdracht. Cruciaal is dat deze gelabelde receptoren nog steeds G-eiwitten konden activeren en normale internalisatie ondergingen, wat aantoont dat de reporters betrouwbaar waren en niet verstorend.
Medicijnen laten onderscheidende “conformationele vingerafdrukken” achter
De onderzoekers vergeleken vervolgens meerdere middelen die de M2-receptor allemaal activeren, maar met verschillende sterktes: het eigen acetylcholine van het lichaam, een supersterke synthetische agonist genaamd iperoxo, en twee zwakkere partiële agonisten, arecoline en pilocarpine. Elk middel produceerde een uniek patroon van fluorescentieveranderingen over de zeven reportersites — een conformationele vingerafdruk. Op de meeste posities volgde de grootte van de beweging hoe sterk het middel de receptor activeerde. Op twee posities was de relatie echter omgekeerd: de zwakkere middelen veroorzaakten de grootste veranderingen en het sterkste middel vrijwel geen. Dergelijk gedrag kan niet worden verklaard door één enkele actieve staat. In plaats daarvan wijst het erop dat dezelfde receptor in levende cellen meerdere verschillende actieve vormen kan aannemen, waarvan sommige worden bevoordeeld door sterke middelen en andere door zwakkere.
Meerdere complexen en getimede routes naar signaaloverdracht
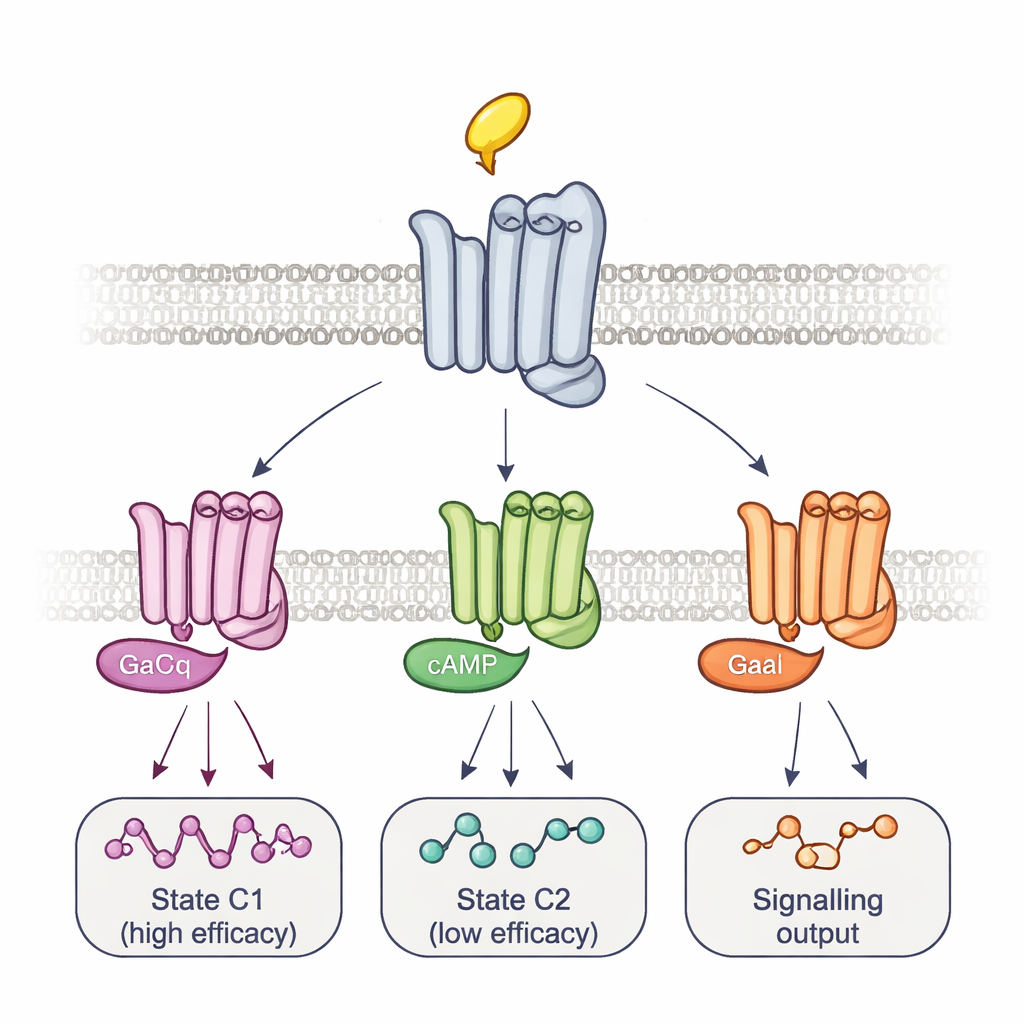
Om deze vormen aan daadwerkelijke signaaloverdracht te koppelen, wijzigde het team de G-eiwitten zelf. Overexpressie van een gemuteerd G-eiwit dat zeer sterke, langlevende complexen met receptoren vormt, veegde selectief het signaal van sommige reportersites weg terwijl het andere versterkte. Dit patroon, samen met de timing van de fluorescentieveranderingen, onthulde ten minste twee hoofdreceptor–G-eiwitcomplexen: een snelvormend, hoog-efficaciteitscomplex en een langzamer, laag-efficaciteitscomplex. Verschillende middelen verschoven de balans tussen deze complexen en gebruikten zelfs verschillende tussenstappen om daar te komen, waarmee middel-specifieke activatietrajecten werden getraceerd. Met een aparte bioluminescentieassay die een paneel van 14 G-eiwitsubtypen monitort, toonden de auteurs aan dat deze evenwichten niet alleen bepalen hoe sterk een middel de signaaloverdracht in het algemeen activeert, maar ook welke exacte G-eiwitten worden ingeschakeld. Bijvoorbeeld activeerde arecoline bepaalde Go-eiwitten bij voorkeur, terwijl pilocarpine sterk het laag-efficaciteitscomplex bevoordeelde.
Waarom dit belangrijk is voor betere medicijnen
Voor niet-specialisten is de kernboodschap dat een enkele receptor niet slechts één schakelaar is, maar een cluster van gerelateerde schakelaars, elk bereikbaar via verschillende paden en gekoppeld aan licht verschillende downstream-effecten. Deze studie biedt een direct zicht op die paden en toestanden in intacte cellen, in plaats van in vereenvoudigde reageerbuisystemen. Door in kaart te brengen hoe specifieke middelen de receptor in de richting van bepaalde complexen en G-eiwitpartners buigen, krijgen onderzoekers een blauwdruk voor het ontwerpen van "slimmere" medicijnen — verbindingen die receptoren in toestanden duwen die nuttige signalen stimuleren en toestanden vermijden die met bijwerkingen geassocieerd zijn. De hier ontwikkelde fluorescerende biosensorstrategie zou aanpasbaar moeten zijn aan vele andere receptoren en opent een venster op de realtime choreografie van medicijnwerking in levende cellen.
Bronvermelding: Thomas, R., Jacoby, P.S., De Faveri, C. et al. Ligand-specific activation trajectories dictate GPCR signalling in cells. Nature 650, 1053–1062 (2026). https://doi.org/10.1038/s41586-025-09963-3
Trefwoorden: GPCR-signaaloverdracht, ligandefficacy, G-eiwitten, conformationele biosensoren, medicijnontwikkeling