Clear Sky Science · nl
Ziektetolerantie en pathogenese van infecties: leeftijdsgebonden afwegingen bij muizen
Waarom sommige infecties naarmate we ouder worden dodelijker zijn
Waarom hebben oudere volwassenen bij ernstige infecties vaak veel slechtere uitkomsten, ook al worden ze aan dezelfde ziekteverwekkers blootgesteld als jongere mensen? Deze studie gebruikt muizen om dat raadsel te onderzoeken, met de focus op sepsis — een levensbedreigende reactie op een infectie. De onderzoekers tonen aan dat beschermende programma’s van het eigen lichaam met de leeftijd kunnen omslaan: genen die in de jeugd het hart en andere organen tegen schade beschermen, kunnen later juist schade veroorzaken. Inzicht in deze leeftijdsafhankelijke omslag kan de manier veranderen waarop we behandelingen voor infecties bij kinderen, volwassenen en ouderen ontwerpen.
Verschillende trajecten na dezelfde infectie
Om een veelvoorkomende menselijke noodsituatie na te bootsen, infecteerde het team jonge en oude muizen met een mengsel van twee vaak sepsis veroorzakende bacteriën, Escherichia coli en Staphylococcus aureus. Ze kozen zorgvuldig een dosis die ongeveer de helft van de dieren deed overlijden (een LD50), zodat sommige muizen zouden overleven en andere niet, ondanks dezelfde startblootstelling. Verrassend genoeg droegen beide leeftijdsgroepen vergelijkbare hoeveelheden bacteriën in hun organen. Wat verschilden was hoe hun lichamen met de schade omgingen. Jonge en oude muizen volgden verschillende “gezondheidstrajecten” tijdens sepsis: lichaamstemperatuur, zichtbare ziekteverschijnselen en het tijdstip van achteruitgang of herstel splitsten zich duidelijk in overlevende en niet‑overlevende trajecten. 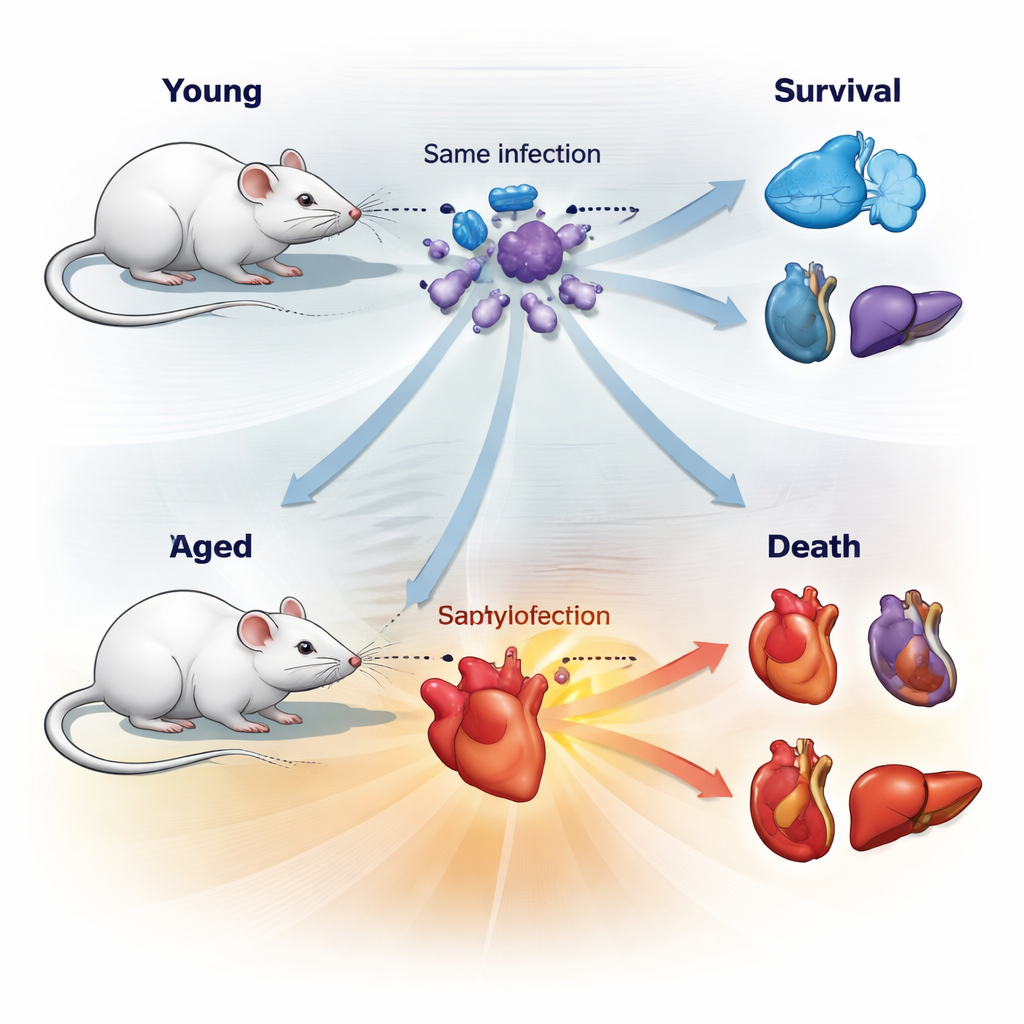
Hartveranderingen vertellen twee leeftijdsspecifieke verhalen
Bij onderzoek van de organen kwam het hart naar voren als een centrale speler. Jonge muizen die aan sepsis overleden, ontwikkelden vergrote, gezwollen harten met uitgerekte kamers — tekenen van ernstige belasting — en lieten hoge niveaus zien van bloedmarkers die in ziekenhuizen worden gebruikt om hartbeschadiging en hartfalen aan te geven. Hun nieren en lever waren ook beschadigd, maar minder dramatisch. Daarentegen toonden oude muizen die stierven het omgekeerde hartpatroon: hun harten werden kleiner en vermagerd, terwijl nierbeschadiging en verlies van nierfunctie sterker aanwezig waren. Oude overlevers hadden interessant genoeg vaak vergrote harten maar minder algemene schade. Genactiviteitsprofilering van hartweefsel bevestigde dat jonge en oude muizen verschillende remodelleringsprogramma’s activeerden: jongere harten schakelden paden aan die verband houden met groei en structurele verandering, terwijl oudere harten paden activeerden die te maken hebben met eiwitafbraak en celfagie/atrofie.
Een beschermend circuit in jonge harten
Bij nadere bestudering van deze moleculaire handtekeningen belichtten de onderzoekers een regelgen genaamd Foxo1 en een van zijn doelen, Trim63, dat codeert voor een eiwit bekend als MuRF1 dat betrokken is bij het labelen van spiereiwitten voor recycling. In harten van jonge overlevenden waren Foxo1 en Trim63 sterk geactiveerd in vergelijking met jonge muizen die stierven of nooit geïnfecteerd waren. Het blokkeren van FoxO1 met een geneesmiddel, of het specifiek verwijderen ervan in hartspiercellen, maakte jonge muizen veel vatbaarder voor ziekte en overlijden, hoewel hun bacteriële lasten en ontstekingssignalen vergelijkbaar bleven. Evenzo hadden jonge muizen zonder Trim63 ernstiger hartzwelling, meer lekkage van hartschademarkers naar het bloed en bredere beschadiging van lever en nieren. Deze resultaten wijzen erop dat het FoxO1–Trim63‑pad in de jeugd fungeert als een ziektetolerantiesysteem: het bestrijdt de microben niet direct, maar helpt het hart zich aan stress aan te passen en voorkomt multi‑orgaanfalen.
Wanneer de beschermer van gisteren de bedreiging van vandaag wordt
Dezelfde genen vertelden een ander verhaal op oudere leeftijd. Bij oude muizen hing overleving niet langer af van het opschroeven van FoxO1 in het hart. In plaats daarvan beschermde het uitschakelen van FoxO1 — hetzij genetisch in spiercellen hetzij met een geneesmiddel — oudere dieren juist tegen sepsis‑geïnduceerde ziekte en overlijden. Oude muizen zonder Trim63, of behandeld met een MuRF1‑remmer, deden het ook beter: ze hadden vergrote maar structureel gezondere harten, lagere niveaus van bloedmarkers die hartbelasting signaleren, en minder schade aan nieren en lever. Met andere woorden, hetzelfde circuit dat in jonge harten gezonde aanpassing aan infectie bevordert, dreef nu schadelijke remodellering en orgaanschade in oudere harten. Deze leeftijdsomslag in functie past bij een concept uit de evolutionaire biologie dat “antagonistische pleiotropie” wordt genoemd, waarbij eigenschappen die de fitheid vroeg in het leven verbeteren, verborgen kosten op latere leeftijd met zich meebrengen. 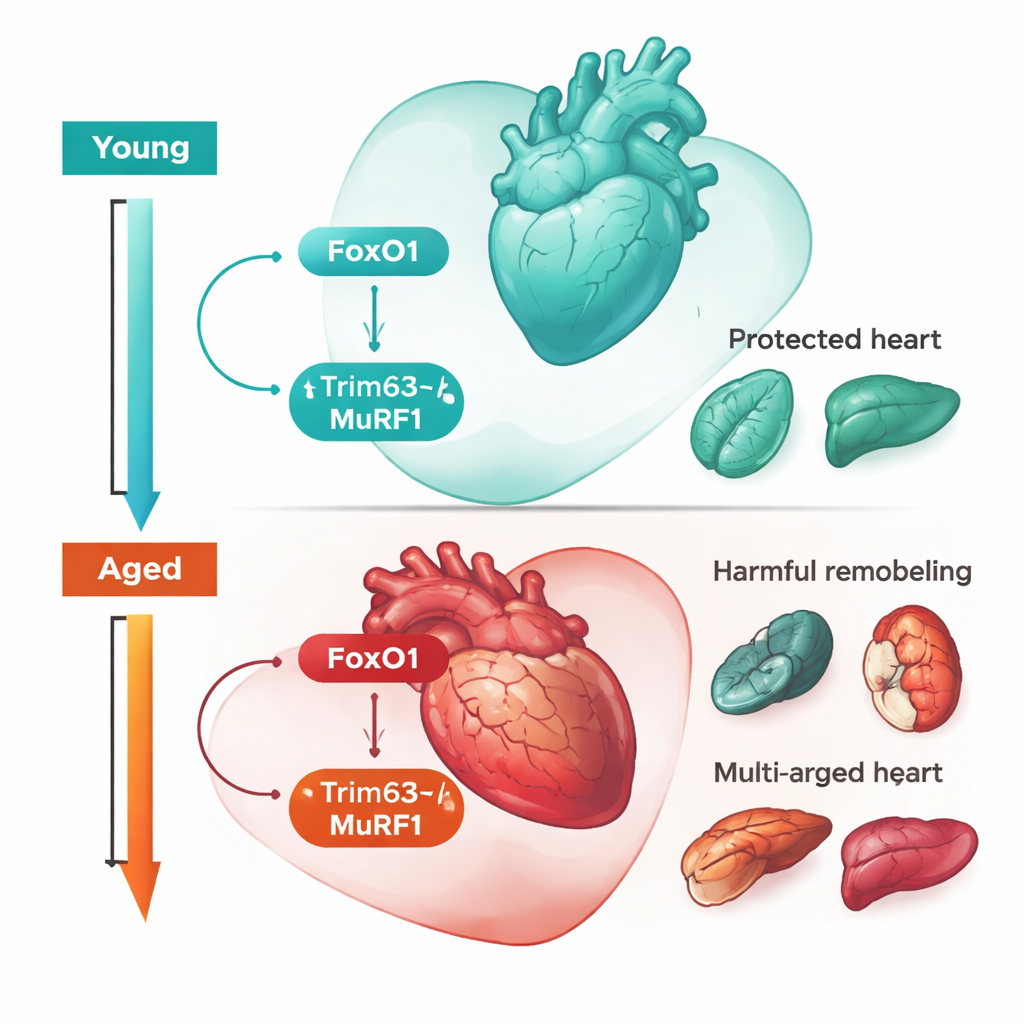
Wat dit betekent voor de behandeling van infecties gedurende het leven
Voor een lezer zonder wetenschappelijke achtergrond is de kernboodschap dat het bestrijden van ernstige infecties zoals sepsis niet alleen draait om het doden van ziekteverwekkers — het gaat ook om hoe onze organen de storm doorstaan. Deze studie toont aan dat de stressreactie van het hart, gebouwd rond FoxO1 en Trim63, jonge lichamen helpt infectie te tolereren maar met de leeftijd een nadeel kan worden. Als gevolg daarvan kan een geneesmiddel dat dit pad blokkeert levensreddend zijn voor een oudere patiënt, terwijl het gevaarlijk zou kunnen zijn voor een jongere. Het werk benadrukt dat therapieën voor infectieziekten mogelijk op leeftijd afgestemd moeten worden, rekening houdend met het feit dat hetzelfde gen twee gezichten kan hebben: beschermer in de jeugd, boosdoener op oudere leeftijd.
Bronvermelding: Sanchez, K.K., McCarville, J.L., Stengel, S.J. et al. Disease tolerance and infection pathogenesis age-related tradeoffs in mice. Nature 650, 727–735 (2026). https://doi.org/10.1038/s41586-025-09923-x
Trefwoorden: sepsis, veroudering, ziektetolerantie, hartremodellering, FoxO1 Trim63-pad