Clear Sky Science · nl
Door microbiota geïnduceerde T-celplasticiteit maakt immuungemedieerde tumorkontrole mogelijk
Hoe vriendelijke darmbacteriën kunnen helpen kanker te bestrijden
Kankerimmunotherapie heeft de behandeling voor veel patiënten veranderd, maar slechts een deel ziet dat tumoren krimpen en wegblijven. Deze studie stelt een schijnbaar eenvoudige vraag met grote implicaties: kunnen specifieke darmbacteriën immuuncellen zodanig "trainen" dat checkpoint-blokkerende geneesmiddelen, zoals anti–PD‑1-therapie, beter werken? Door de reis van immuuncellen van de dunne darm naar tumoren in muizen te volgen, onthullen de auteurs een directe, toetsbare koppeling tussen één darmmicrobe en succesvolle tumorkontrole.
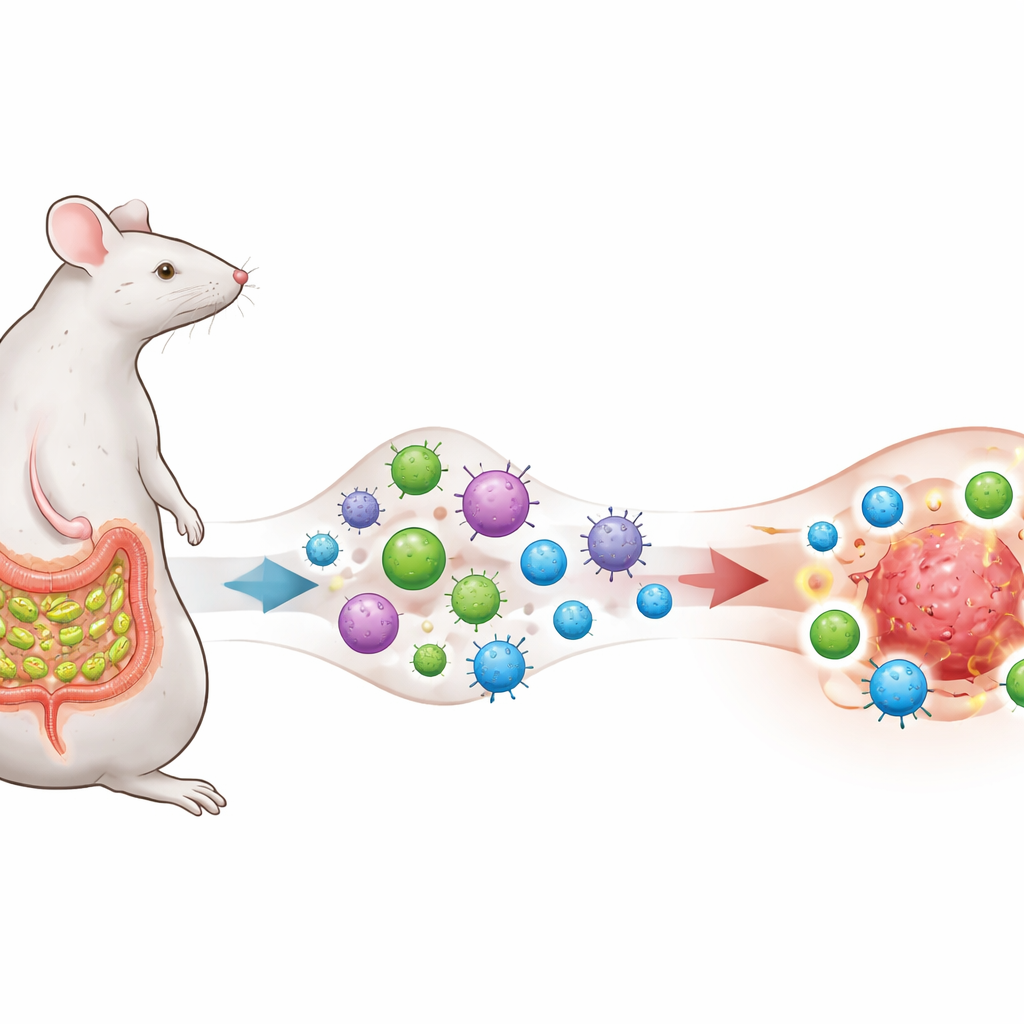
Een microbe die het immuunsysteem traint
De onderzoekers richten zich op een darmbacterie die segmented filamentous bacteria (SFB) heet, bekend om dicht bij het slijmvlies van de dunne darm bij muizen te leven en een sterke maar normaal huisvestende T helper 17 (TH17)-celrespons uit te lokken. Ze modificeren melanoma-, long- en colonkankercellen zodat die een eiwitfragment tonen dat ook in SFB voorkomt, waarmee ze een opzettelijke "antigeenovereenkomst" tussen de microbe en de tumoren creëren. Muizen blijven ofwel vrij van SFB of worden ermee gekoloniseerd, en allemaal krijgen ze anti–PD‑1-therapie, een veelgebruikte checkpoint-blokkerende antilichaamtherapie die erop gericht is de remmen op T-cellen op te heffen.
Darm-geschoolde cellen maken van koude tumoren hete tumoren
Anti–PD‑1-behandeling alleen, of SFB alleen, doet weinig om tumorgroei te vertragen. Maar wanneer tumoren het SFB-afgeleide antigeen dragen en de muizen met SFB gekoloniseerd zijn, wordt anti–PD‑1 plotseling zeer effectief: tumoren krimpen, de overleving verbetert en overlevende dieren verwerpen bij een latere tumorhertoetsing de tumor zonder extra therapie, wat wijst op aanhoudend immuungeheugen. Bij deze succesvolle muizen vullen de tumoren zich met agressieve CD8-"killer" T-cellen die interferon‑γ en andere toxische moleculen produceren, terwijl suppressieve regulerende T-cellen een kleiner aandeel van de immuunpopulatie vormen. Kort gezegd wordt de lokale omgeving rond de kanker omgevormd van relatief "koud" en ongevoelig naar "heet" en ontstoken.
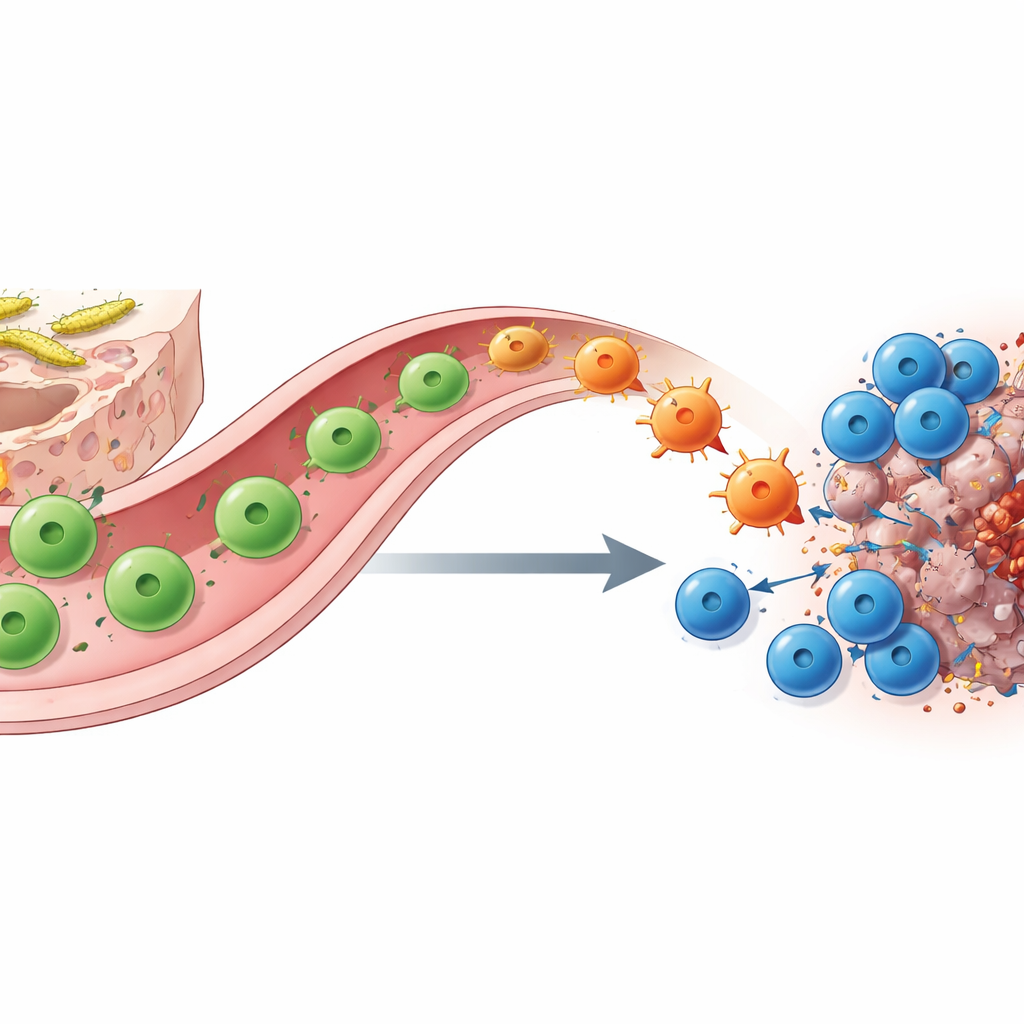
Vormveranderende helper-T-cellen overbruggen darm en tumor
Hoe zorgt SFB-kolonisatie voor deze verschuiving? Met moleculaire barcodes, single-cell sequencing en slimme genetische tracering tonen de auteurs aan dat de sleutelspelers SFB-specifieke CD4-helper-T-cellen zijn. In de dunne darm beginnen deze cellen als TH17-cellen die de barrièrefunctie ondersteunen en doorgaans het molecuul IL‑17A produceren. Wanneer ze onder checkpointblokkeering in een tumor het overeenkomende antigeen tegenkomen, migreren ze van de darm naar de tumorplaats en "her-specialiseren" ze tot TH1-achtige cellen die in plaats daarvan grote hoeveelheden interferon‑γ en TNF afscheiden. Deze omgezette "ex‑TH17"-cellen versterken antigeenpresentatie en scheiden chemische lokstoffen uit, waarmee ze CD8-killer-T-cellen aantrekken en versterken. Het verwijderen van ofwel helper- of killer-T-cellen, of het genetisch weghalen van de IL‑17A-lijncellen die als voorlopers dienen, maakt het voordeel van anti–PD‑1 grotendeels teniet, wat hun samenwerking benadrukt.
Niet alle microben geven behulpzame instructies
Om te testen of elke darmbacterie met overlappende antigenen volstaat, herhaalt het team het experiment met een andere commensale microbe, Helicobacter hepaticus. Dit organisme veroorzaakt ook sterke T-celreacties maar breidt vooral regulerende celtypen uit die ontsteking dempen. Wanneer tumoren zo zijn geconstrueerd dat ze een H. hepaticus-antigeen tonen en muizen met deze bacterie gekoloniseerd zijn, verbetert anti–PD‑1-therapie niet. Hoewel veel H. hepaticus-specifieke helper-T-cellen naar de tumor reizen, behouden ze een regulerend karakter en produceren ze weinig interferon‑γ, waardoor ze falen in het activeren van killer-T-cellen. Dit contrast laat zien dat de kwaliteit en plasticiteit van microbe-geïnduceerde T-celprogramma's—niet alleen antigeenmatching—bepalen of de microbiota kankerimmunotherapie zal helpen of belemmeren.
Wat dit kan betekenen voor toekomstige kankerzorg
Al met al levert het werk direct bewijs in dieren dat een gedefinieerde darmbacterie helper-T-cellen in de darm kan voortrainen, ze naar antigeendelende tumoren kan sturen en, onder checkpointblokkeering, hun rol kan doen omslaan zodat ze krachtige tumorbestrijdende cellen worden. Door dit darm‑naar‑tumorcircuit te verduidelijken, suggereert de studie dat zorgvuldig gekozen of ontworpen microben op den duur naast immunotherapie gebruikt zouden kunnen worden om meer patiënten hun tumoren om te zetten in behandelbare, ontstoken doelwitten—mits die microben het juiste soort flexibele, pro-inflammatoire T-celrespons opwekken in plaats van een kalmerende, regulerende respons.
Bronvermelding: Najar, T.A., Hao, Y., Hao, Y. et al. Microbiota-induced T cell plasticity enables immune-mediated tumour control. Nature 651, 201–210 (2026). https://doi.org/10.1038/s41586-025-09913-z
Trefwoorden: darmmicrobiota, kankerimmunotherapie, T-celplasticiteit, checkpointblokkeering, tumormicro-omgeving