Clear Sky Science · nl
Stress reguleert overdracht van heterochromatine via ubiquitylering van histon H3
Hoe cellen zich stress herinneren
Onze cellen hebben manieren nodig om zich eerdere stress—zoals hitte, gebrek aan voedingsstoffen of blootstelling aan geneesmiddelen—te "herinneren", zodat ze de volgende keer sneller kunnen reageren. Een krachtig geheugensysteem berust op heterochromatine, dicht opgevouwen DNA dat bepaalde genen gedurende vele celdelingen stilhoudt. Dit artikel onderzoekt hoe cellen dat geheugen actief afstemmen als reactie op stress en onthult een moleculair knooppunt dat omgevingssignalen koppelt aan langdurige veranderingen in genactiviteit. Inzicht in dit regelsysteem kan helpen verklaren hoe schimmels geneesmiddelresistentie ontwikkelen en hoe stress het epigenetische landschap van onze eigen cellen hervormt.
Een slot op het genoom
Heterochromatine kan worden gezien als een moleculair slot op stukken DNA dat nabijgelegen genen stilhoudt. Dat slot wordt opgebouwd uit chemische tags op histoneiwitten, vooral een merkteken genaamd H3K9me3. Eenmaal gevestigd kan het zichzelf kopiëren elke keer dat DNA wordt gerepliceerd, waardoor patronen van genonderdrukking erfelijk worden zonder het onderliggende DNA te veranderen. Tot nu toe suggereerden de meeste studies dat dit zelfkopiërende proces grotendeels afhankelijk is van een "lees–schrijf" feedbacklus: een enzymcomplex herkent bestaande H3K9me3‑merken en voegt hetzelfde merkteken toe aan naburige histonen, waardoor het stilgedomijn geleidelijk uitbreidt. Maar dit model kon niet volledig verklaren hoe omgevingsomstandigheden de snelheid of richting van heterochromatineverspreiding beïnvloeden.
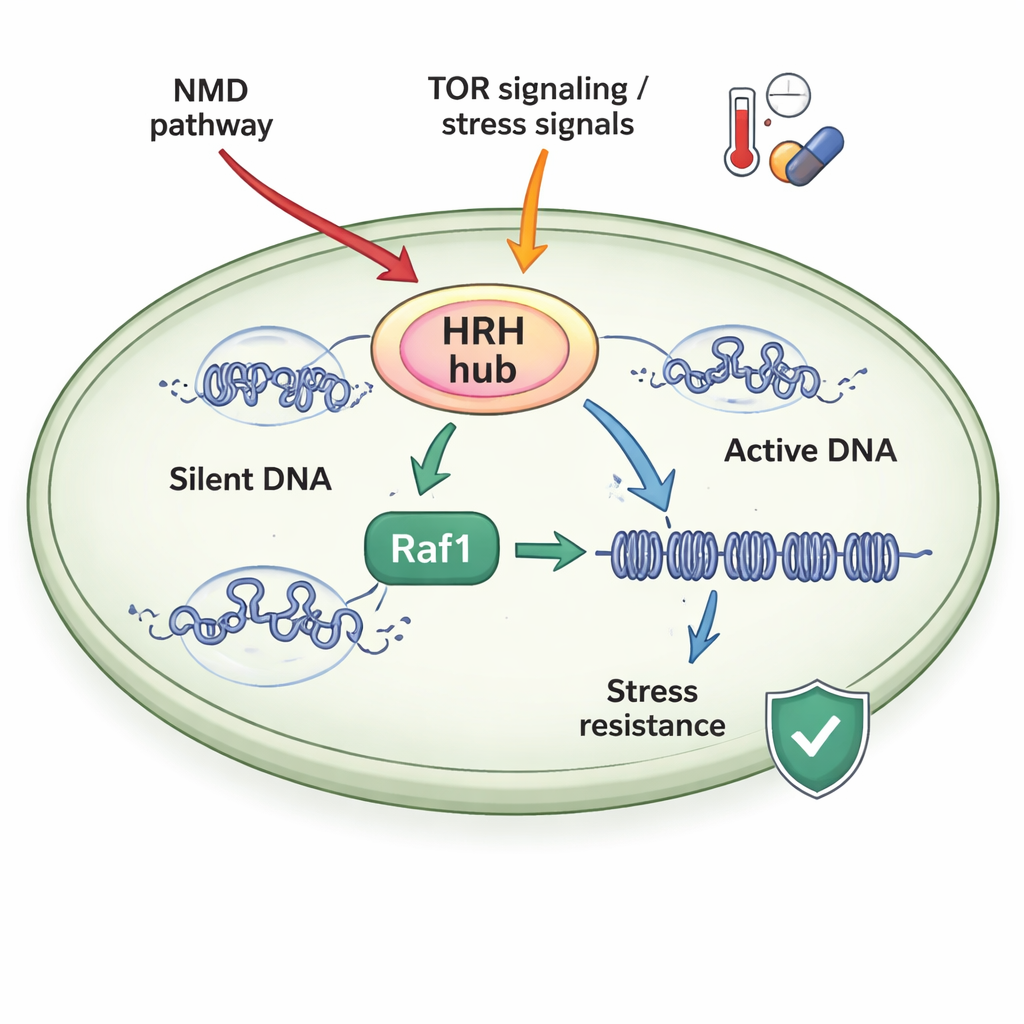
Een stressgevoelig regelknooppunt
De auteurs bestudeerden schizosaccharomyces (wantschimmel), een eenvoudig modelorganisme waarvan het chromatineapparaat sterke overeenkomsten vertoont met dat van hogere organismen. Ze richtten zich op een complex genaamd ClrC, dat zowel het H3K9me3‑merk aanbrengt als een klein eiwit, ubiquitine, aan een andere plaats op histon H3 koppelt (H3K14ub). Een cruciale subeenheid van ClrC, Raf1, fungeert als beperkende "poortwachter": wanneer Raf1 schaars is, blijft veel van het hoofdenzym (Clr4) vrij zweven in plaats van zich aan het complex op chromatine te binden, en slome gebieden verspreiden zich niet. Wanneer Raf1 overvloedig aanwezig is, wordt meer ClrC samengesteld en stabiel op DNA gebonden, waardoor H3K14ub‑ en H3K9me3‑merken langs chromosomen kunnen uitbreiden en genstilstand kunnen versterken.
Het slot fijnregelen met ubiquitine
Door chromatinemerken over het hele genoom in kaart te brengen toonde het team aan dat H3K14ub sterk verrijkt is waar heterochromatine zich vormt en dat dit merkteken vrijwel verdwijnt als Raf1 wordt verwijderd. Wanneer cellen een mutatie dragen die de ubiquitine‑toevoeging blokkeert (terwijl H3K9me3 op de startplaats intact blijft), kunnen stille domeinen zich niet naar buiten uitbreiden. Met andere woorden: H3K14ub is niet louter decoratief; het is vereist om het front van heterochromatine vooruit te duwen. Biochemische en beeldvormingsexperimenten verklaren waarom: H3K14ub verhoogt de activiteit van het Clr4‑enzym sterk en helpt het hele complex op chromatine te parkeren, waardoor de lokale dichtheid van H3K9me3 boven de drempel komt die nodig is voor stabiele overerving. Opmerkelijk is dat verhoging van Raf1‑niveaus meerdere andere factoren kan omzeilen die normaal nodig zijn om deze stille domeinen te behouden, wat benadrukt dat door Raf1 aangedreven ubiquitylering een centraal regelhefbom is.
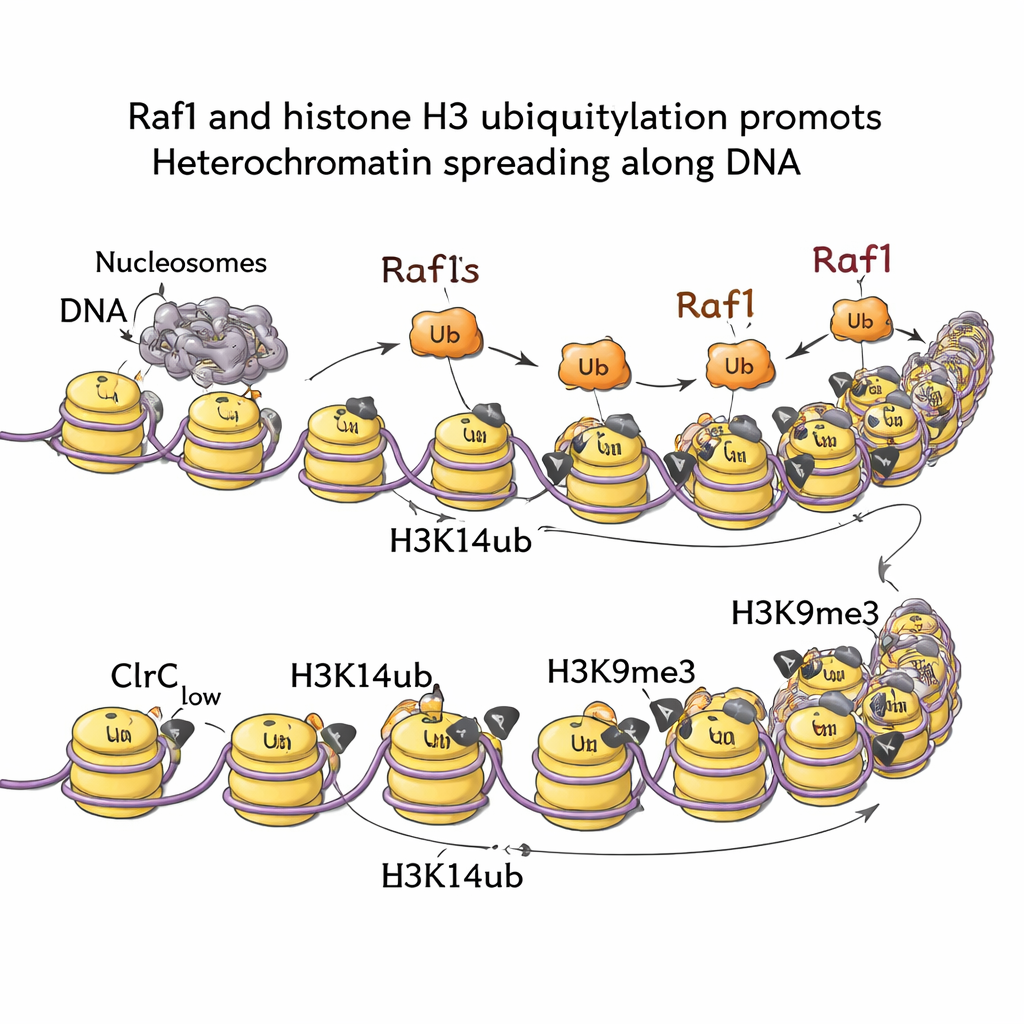
Signalen van RNA‑afbraak en groeipaden
Cellen laten Raf1‑niveaus niet aan het toeval over. De studie toont aan dat twee belangrijke stress‑responsieve systemen invoeden op wat de auteurs een regulerend knooppunt voor heterochromatineerfelijkheid (HRH) noemen, gecentreerd rond Raf1. Ten eerste richt de nonsense‑gemedieerde afbraak (NMD)‑route—het meest bekend om het vernietigen van foutieve boodschapper‑RNA's—zich op het boodschapper‑RNA dat Raf1 codeert, waardoor Raf1‑niveaus onder normale omstandigheden laag blijven. Het uitschakelen van NMD stabiliseert Raf1‑RNA, verhoogt de hoeveelheid Raf1‑eiwit en herstelt heterochromatineverspreiding in mutanten die anders geen stille domeinen kunnen handhaven. Ten tweede bevordert een sensor voor groei en stress genaamd TORC2, werkend via de kinase Gad8, de expressie van Raf1. Hoge temperatuur schakelt deze route uit, verlaagt Raf1‑niveaus, verzwakt heterochromatine en maakt het moeilijker voor cellen om stille toestanden te behouden, tenzij Raf1 experimenteel wordt verhoogd.
Stress, geneesmiddelresistentie en bredere implicaties
De auteurs verbinden dit moleculaire knooppunt vervolgens met adaptatie in de praktijk. Blootstelling van gist aan cafeïne, een stress die ook bekendstaat om NMD in andere systemen te dempen, verhoogt Raf1‑niveaus en bevordert de verspreiding van heterochromatine naar nieuwe locaties, inclusief genen waarvan de stillegging resistentie tegen cafeïne en schimmelwerende middelen geeft. Evenzo worden cellen met kunstmatig verhoogd Raf1 resistenter tegen fluconazol en clotrimazol, veelgebruikte antischimmelmiddelen. Omgekeerd, wanneer Raf1 wordt verminderd—door hitte of door verlies van TORC2–Gad8‑signalering—wordt heterochromatine instabiel en vervaagt het epigenetische geheugen, tenzij Raf1 wordt hersteld. Omdat Raf1‑achtige eiwitten, het ClrC‑complex en het H3K14ub‑merkteken allemaal tegenhangers hebben in pathogene schimmels en in zoogdieren, suggereren deze bevindingen dat een vergelijkbaar stress‑zintuigend epigenetisch knooppunt geneesmiddelresistentie, ontwikkeling en ziekte in veel soorten kan beïnvloeden.
Waarom dit ertoe doet
In gewone bewoordingen laat dit werk zien dat genstillegging door chromatine geen star slot is, maar een slim, aanpasbaar systeem. Cellen gebruiken een centraal knooppunt om omgevingssignalen te lezen—temperatuurschommelingen, voedingsstatus, chemische stressen—en regelen Raf1 naar boven of naar beneden. Dat bepaalt vervolgens welk deel van het genoom in langdurige stilte wordt gewikkeld en hoe gemakkelijk cellen zichzelf kunnen "herprogrammeren" zonder hun DNA te muteren. Door de sleutelrol van ubiquitylering van histon H3 en de dosering van Raf1 in dit proces bloot te leggen, biedt de studie een blauwdruk voor hoe stress snel het epigenetische landschap kan hervormen—en geeft het aanwijzingen voor nieuwe manieren om schimmelresistentie tegen geneesmiddelen of abnormale genstillegging bij menselijke ziekte te beïnvloeden.
Bronvermelding: Bhatt, B., Wei, Y., Pradhan, A.K. et al. Stress controls heterochromatin inheritance via histone H3 ubiquitylation. Nature 650, 768–778 (2026). https://doi.org/10.1038/s41586-025-09899-8
Trefwoorden: heterochromatine, epigenetische overerving, histon ubiquitinylering, stressadaptatie, schimmelresistentie tegen geneesmiddelen