Clear Sky Science · nl
Biomimetische vesicles vervaardigd uit gemodificeerde tumorcellen fungeren als gepersonaliseerde vaccins voor postoperatieve kankerimmunotherapie
Tumorrestanten omzetten in een tweede verdedigingslinie
Voor veel mensen met solide tumoren is chirurgie slechts de eerste ronde in een lange strijd. Zelfs wanneer het grootste deel van een tumor wordt verwijderd, kunnen kleine clusters kankercellen ontsnappen en later dodelijke uitzaaiingen vormen. Deze studie onderzoekt een vindingrijke manier om de tumorcellen van een patiënt om te zetten in een gepersonaliseerd vaccin, bedoeld om deze resten na de operatie op te sporen en het immuunsysteem te helpen voorkomen dat de kanker terugkeert.
Waarom achtergebleven kankercellen zo moeilijk uit te roeien zijn
Standaardbehandelingen hebben moeite met de cellen die achterblijven nadat een chirurg het hoofdvolume van de tumor heeft verwijderd. Deze verspreide cellen verbergen zich vaak in verre organen en zijn afgeschermd tegen geneesmiddelen en immuunaanvallen. Bestaande immuungebaseerde vaccins proberen het lichaam te trainen om tumormerkers te herkennen met gespecialiseerde immuuncellen, dendritische cellen genoemd, maar deze levende vaccins zijn moeilijk te produceren, bereiken immuunorganen niet efficiënt en hebben in de kliniek slechts bescheiden voordelen laten zien. Een centrale uitdaging is dat de kanker van elke patiënt een unieke mix van mutaties draagt, waardoor kant-en-klare vaccins meestal belangrijke doelen missen.
Een verborgen schakel die kankercellen opvallender maakt
De onderzoekers begonnen met het zoeken naar natuurlijke schakelaars in het immuunsysteem die cellen beter maken in het tonen van hun interne inhoud aan immuunwachters. Ze richtten zich op een eiwit genaamd syntaxine 11, normaal gesproken overvloedig aanwezig in immuuncellen maar schaars in veel tumoren. Door dit eiwit te verhogen in agressieve borstkankercellen uit muismodellen ontdekten ze dat de kankercellen zich meer gingen gedragen als professionele immuunwachters: ze toonden hogere niveaus van moleculaire "naamkaartjes" en hulp-signalen aan hun oppervlak. In feite werden de tumorcellen opnieuw geprogrammeerd om meer van hun unieke eigenschappen aan het immuunsysteem te onthullen in plaats van ze te verbergen.
Het bouwen van kleine imitatie-immuunboodschappers
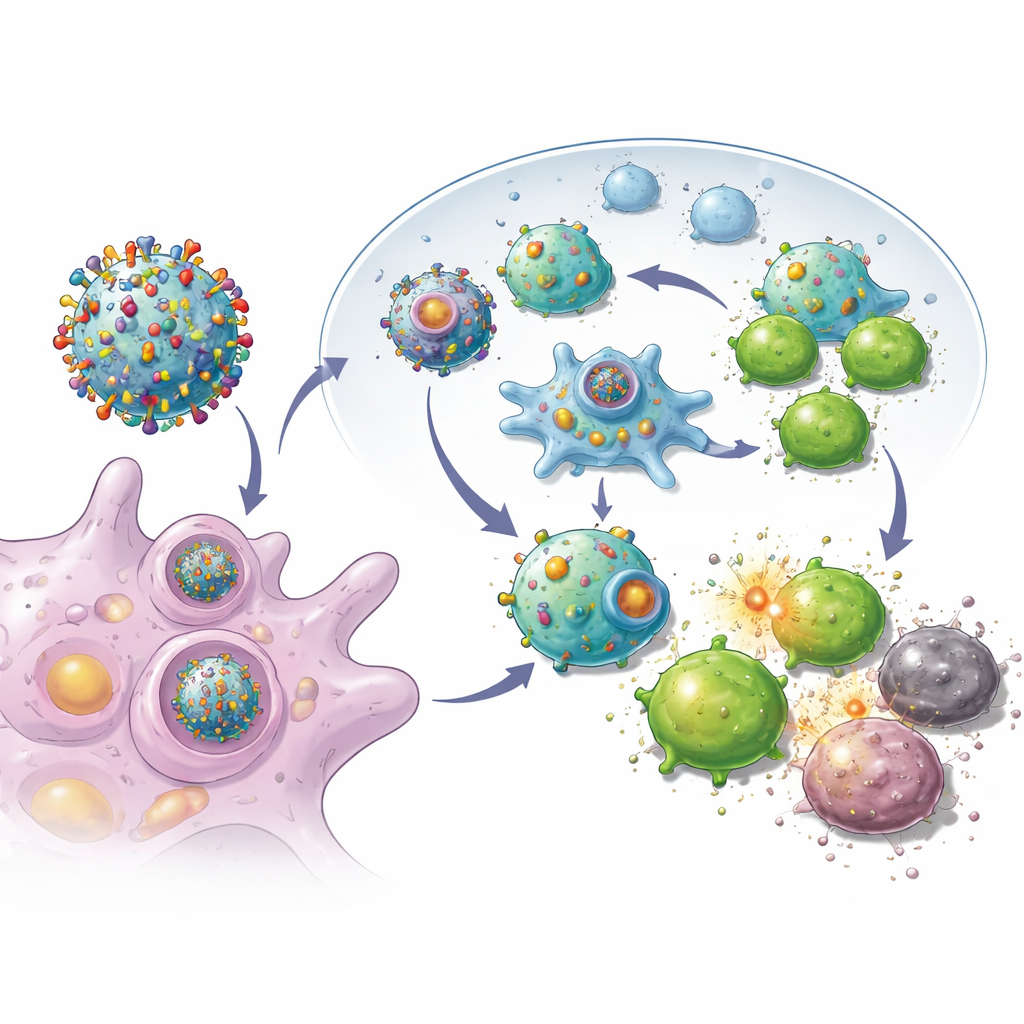
Gewapend met deze gereprogrammeerde tumorcellen verwijderde het team hun buitenmembraan en gebruikte die membranen om biologisch afbreekbare nanodeeltjes te coaten die waren geladen met een klein immuunstimulerend middel. Het resultaat was een zwerm nanometerschaalige vesicles, elk met de volledige verzameling markers van die tumor plus ingebouwde "activerings"-signalen voor cytotoxische T-cellen. Wanneer onder de huid geïnjecteerd bij muizen na de operatie, reisden deze vesicles efficiënt naar naburige lymfeklieren, waar immuuncellen worden getraind. Daar konden ze zowel rechtstreeks cytotoxische T-cellen aanspreken als worden opgenomen door natuurlijke immuunwachters, die de respons verder versterkten. Experimenten toonden aan dat T-cellen die met deze vesicles in aanraking kwamen krachtiger vermenigvuldigd werden en beter in staat waren kankercellen te vernietigen dan T-cellen geprimed met eenvoudigere nanopartikelontwerpen.
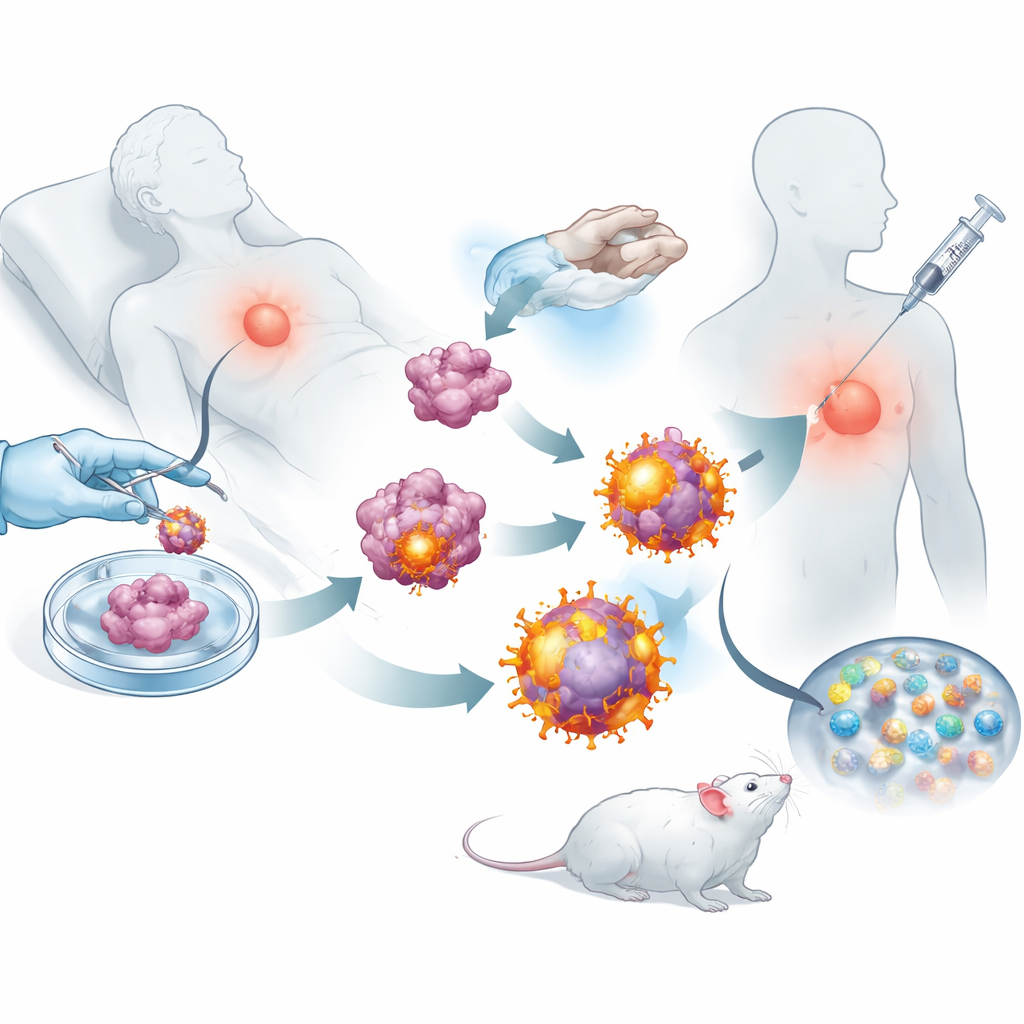
Kanker op afstand houden na een operatie
Met behulp van meerdere muismodellen voor borstkanker en melanoom testten de onderzoekers of dit op maat gemaakte vaccin daadwerkelijk het ziekteverloop kon veranderen. Bij dieren waarbij het grootste deel van een borstumor chirurgisch was verwijderd, ontwikkelden gevaccineerde muizen kleinere recidieven en veel minder longmetastasen dan onbehandelde dieren. Lymfeklieren, milt en tumoren van behandelde muizen zaten vol actieve cytotoxische T-cellen en langlevende geheugencellen, wat suggereert dat het immuunsysteem zowel was geactiveerd als op lange termijn getraind. In combinatie met een goedgekeurd checkpoint-blokkerend antilichaam dat voorkomt dat tumoren T-cellen verlammen, leidde het vaccin tot duurzame tumorcontrole en bij veel muizen tot volledige regressie en langdurig overleven.
Een gepersonaliseerde behandeling versnellen
Een obstakel om dit concept naar een klinische therapie te brengen is tijd: genetische methoden om tumorcellen te herprogrammeren kunnen traag zijn. Om dit aan te pakken screenden de onderzoekers natuurlijke verbindingen en ontdekten ze deoxypodofyllotoxine, een klein molecuul dat snel de niveaus van de sleutel-schakel en dezelfde immuunstimulerende oppervlaktemerkers verhoogt. Met deze verkorte route bouwden ze vergelijkbare vesicle-gecoate nanodeeltjes in minder tijd, terwijl ze hun vermogen om sterke, tumorspecifieke immuunreacties op te roepen behielden. Tests toonden aan dat vaccins gemaakt met dit middel net zo effectief waren als die geproduceerd met de gen-gebaseerde methode, en hun voordelen hingen af van herkenning van het juiste tumortype in plaats van van algemene vergiftiging van kankercellen.
Wat dit kan betekenen voor toekomstige kankerzorg
Voor niet-specialisten is de kernboodschap dat iemands eigen tumor kan worden omgevormd tot een klein trainingsinstrument voor het immuunsysteem. Door kankercellen om te zetten in bronnen van rijke, gepersonaliseerde informatie en die informatie te verpakken op robuuste nanoscopische dragers, poogt deze aanpak de cellen op te ruimen die de chirurgie achterlaat en te voorkomen dat nieuwe groeisels zich vormen. Hoewel er nog vele stappen nodig zijn voordat zulke vaccins routinematig aan mensen kunnen worden aangeboden — waaronder het aantonen van veiligheid en effectiviteit in menselijke tumoren en het opzetten van betrouwbare productieprocessen — schetst dit werk een pad naar sterk geïndividualiseerde postoperatieve behandelingen die de verdedigingslinies van het lichaam inschakelen om af te maken wat de chirurg is begonnen.
Bronvermelding: Yu, P., Jin, Z., Meng, L. et al. Biomimetic vesicles engineered from modified tumour cells act as personalized vaccines for post-surgical cancer immunotherapy. Nat. Nanotechnol. 21, 443–454 (2026). https://doi.org/10.1038/s41565-025-02113-w
Trefwoorden: kankervaccin, immunotherapie, nanomedicine, postoperatieve behandeling, gepersonaliseerde oncologie