Clear Sky Science · nl
Beoordeling van de structurele integriteit en farmacokinetiek van DNA-origami in vivo
Het bekijken van miniatuurlijke DNA-machines in het lichaam
DNA kan, net als papier, worden gevouwen tot kleine driedimensionale vormen; een techniek die bekendstaat als DNA-origami. Deze nanostructuren kunnen geprogrammeerd worden om geneesmiddelen, vaccins of signaalmoleculen met grote precisie te dragen. Maar zodra ze in het lichaam zijn geïnjecteerd, blijven ze dan lang genoeg intact om te werken, of vallen ze snel uiteen? Dit artikel introduceert een nieuwe manier om deze DNA-machines in actie te volgen in levende dieren, en laat zien hoe lang ze overleven, hoe ze zich door de bloedbaan verplaatsen en zelfs welke delen van elke structuur het eerst afbreken.
Waarom het vouwen van DNA de geneeskunde kan veranderen
DNA-origami maakt gebruik van dezelfde base-pairing regels die onze genetische informatie opslaan, maar hergebruikt die regels om objecten op nanoschaal te bouwen. Onderzoekers kunnen eiwitten, geneesmiddelen of immuunstimulerende signalen op deze objecten rangschikken alsof het pinnen op een Lego-plaat zijn, waardoor ze zeer gecontroleerde therapieën voor kanker, auto-immuunziekten en infecties kunnen creëren. Voor zulke precieze behandelingen veilig en effectief zijn, moeten regelgevers en wetenschappers weten hoe intact deze structuren in het lichaam blijven en hoe snel ze worden geklaard—samen bekend als hun farmacokinetiek. Bestaande detectiemethoden koppelen meestal fluorescentie‑kleurstoffen of tellen eenvoudigweg DNA‑fragmenten, wat uiteen gevallen puin kan laten lijken op volledig intacte nanostructuren. Tot nu toe bestond er geen praktische manier om, in levende dieren, te bepalen of de oorspronkelijke DNA-origami‑vormen zelf nog heel zijn.
Een moleculaire "integriteitstest" voor DNA-origami
Het team ontwikkelde een methode die ze PLASTIQ noemen, een afkorting voor proximity ligation assay for structural tracking and integrity quantification. Het kernidee is dat de DNA-origami zelf rapporteert over zijn staat. Op specifieke posities in elke structuur plaatsen de onderzoekers paren korte DNA-staples die schouder aan schouder langs een helix liggen wanneer het origami correct is gevouwen. Eén van elk paar draagt een klein chemisch label waarmee ze enzymatisch kunnen worden verbonden, of geligeerd, maar alleen als ze nog dicht bij elkaar worden gehouden door een intacte scaffoldstreng. Als de structuur smelt, breekt of wordt afgebroken door enzymen, drijven die twee stukken uit elkaar en kunnen ze niet meer worden geligeerd. Na ligatie worden de verbonden paren vermenigvuldigd met standaard polymerasekettingreactie en gekwantificeerd met gevoelige qPCR of sequencering, waardoor de aanwezigheid van intacte lokale segmenten meetbare signalen oplevert vanuit slechts microliters bloed.
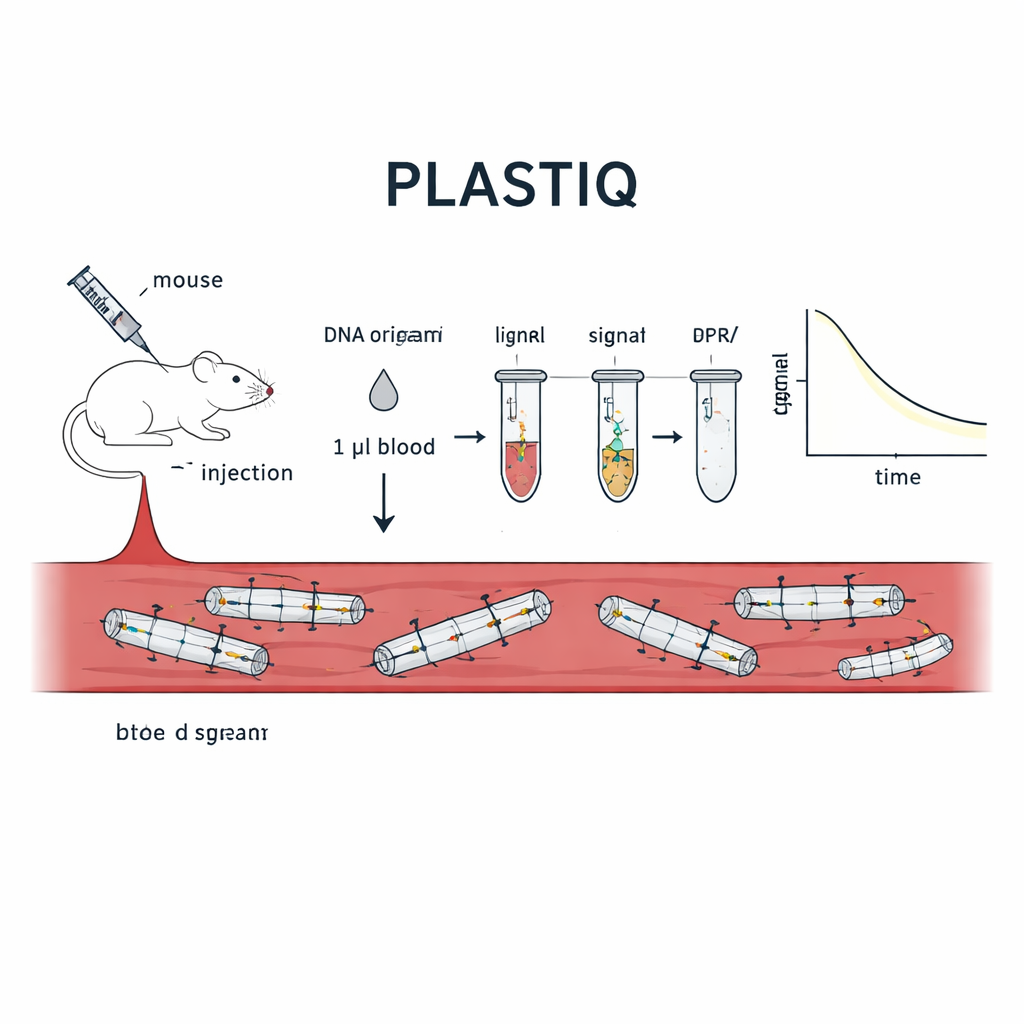
De test toepassen in levende muizen
Om te bewijzen dat PLASTIQ daadwerkelijk structurele integriteit meet, pasten de auteurs het eerst toe op eenvoudige staafvormige DNA-origami-ontwerpen in reageerbuizen. Signalen verschenen alleen wanneer de staven intact waren en verdwenen na warmte‑geïnduceerde ontvouwing, terwijl meer traditionele DNA-gebaseerde assays nog steeds DNA registreerden ongeacht de vorm. Daarna injecteerden ze deze staven bij muizen via verschillende routes—direct in de bloedbaan, in de buikholte, in de spier en onder de huid—en namen ze slechts één microliter bloed op verschillende tijdstippen. PLASTIQ toonde hoe de concentratie van intacte structuren piekte en vervolgens daalde, afhankelijk van de injectieroute, overeenkomend met algemene verwachtingen uit de farmacologie maar met veel fijnere structurele details. De methode was gevoelig tot 0,01 femtomolair en vereiste minimale hoeveelheden bloed, waardoor herhaalde bemonstering van hetzelfde dier over uren mogelijk was.
Beschermende coatings en verborgen zwakke plekken testen
Veel groepen proberen DNA-origami te beschermen door ze te coaten met polymeren zoals PEG, draden te crosslinken met ultraviolet licht of chemische binders toe te voegen, maar het is moeilijk geweest om te zien hoeveel deze trucs in vivo daadwerkelijk helpen. Met PLASTIQ lieten de auteurs zien dat PEG-gecoate staven in de bloedbaan iets langer intact blijven dan naakte exemplaren, maar ook sneller worden geklaard zodra ze in circulatie komen, en dat de coating niet verhindert dat de PLASTIQ-enzymen hun werk doen. Door PLASTIQ te combineren met eenvoudige wiskundige modellen, konden ze absorptie- en eliminatiesnelheden extraheren voor verschillende injectieroutes en coatings, en zelfs herhaalde doses simuleren. Vervolgens zetten ze de methode verder in op een dubbelgelaagde trommelvormige origami, dichter verpakt aan de binnenzijde dan aan de buitenzijde. PLASTIQ-metingen toonden dat staples op het blootgestelde buitenoppervlak sneller integriteit verloren dan die in de binnenste holte, waarmee direct werd bevestigd dat begraven helices worden afgeschermd tegen afbrekende enzymen in bloed.
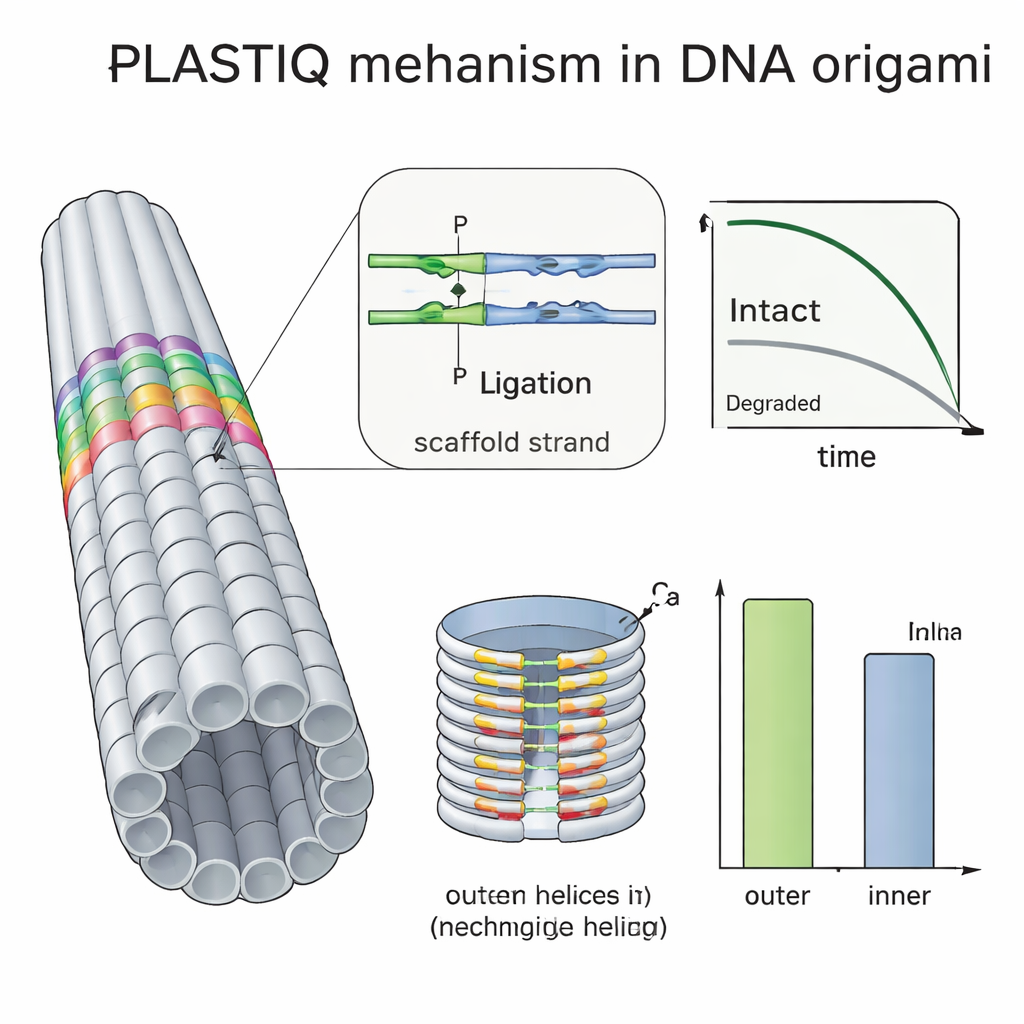
Wat dit betekent voor toekomstige DNA-gebaseerde therapieën
Voor niet‑specialisten kan PLASTIQ worden gezien als een structurele controle voor nanoschaal DNA‑apparaten die door het lichaam reizen. In plaats van alleen te vragen "zit er DNA aanwezig?", vraagt het "is dit DNA nog steeds gevouwen tot het precieze object dat we hebben ontworpen?". Door die vraag met hoge gevoeligheid te beantwoorden uit kleine bloedmonsters, biedt PLASTIQ geneesmiddelenontwikkelaars een manier om het ontwerp, de coating en de dosering van op DNA-origami gebaseerde medicijnen en vaccins te optimaliseren. In de loop van de tijd kan zulke gedetailleerde, kwantitatieve inzicht in hoe deze nanostructuren zich in echte biologische omgevingen gedragen, helpen om DNA-origami van een elegant laboratoriumconcept te transformeren naar betrouwbare, regelgeverklare therapieën.
Bronvermelding: Wang, Y., Rocamonde-Lago, I., Waldvogel, J. et al. Resolving DNA origami structural integrity and pharmacokinetics in vivo. Nat. Nanotechnol. 21, 268–276 (2026). https://doi.org/10.1038/s41565-025-02091-z
Trefwoorden: DNA-origami, nanotherapie, geneesmiddelbezorging, farmacokinetiek, nanotechnologie