Clear Sky Science · nl
mRNA-vaccinatie overwint haemozoin-geïnduceerde vermindering van hele-parasiet malariavaccins bij muizen
Waarom eerdere malaria vaccins minder krachtig maakt
Malaria doodt jaarlijks honderdduizenden mensen, en een van de meest veelbelovende vaccins gebruikt hele, verzwakte parasieten om het immuunsysteem te trainen. Toch werkt deze "gouden standaard" aanpak opvallend beter bij mensen die nooit malaria hebben gehad dan bij mensen die zijn opgegroeid in gebieden waar de ziekte veel voorkomt. Deze studie, uitgevoerd bij muizen, stelt een eenvoudige maar cruciale vraag: wat is het aan eerdere malariainfecties dat een bijzonder werkzaam vaccin plotseling minder effectief maakt — en kan een nieuw soort mRNA-vaccin het probleem oplossen?
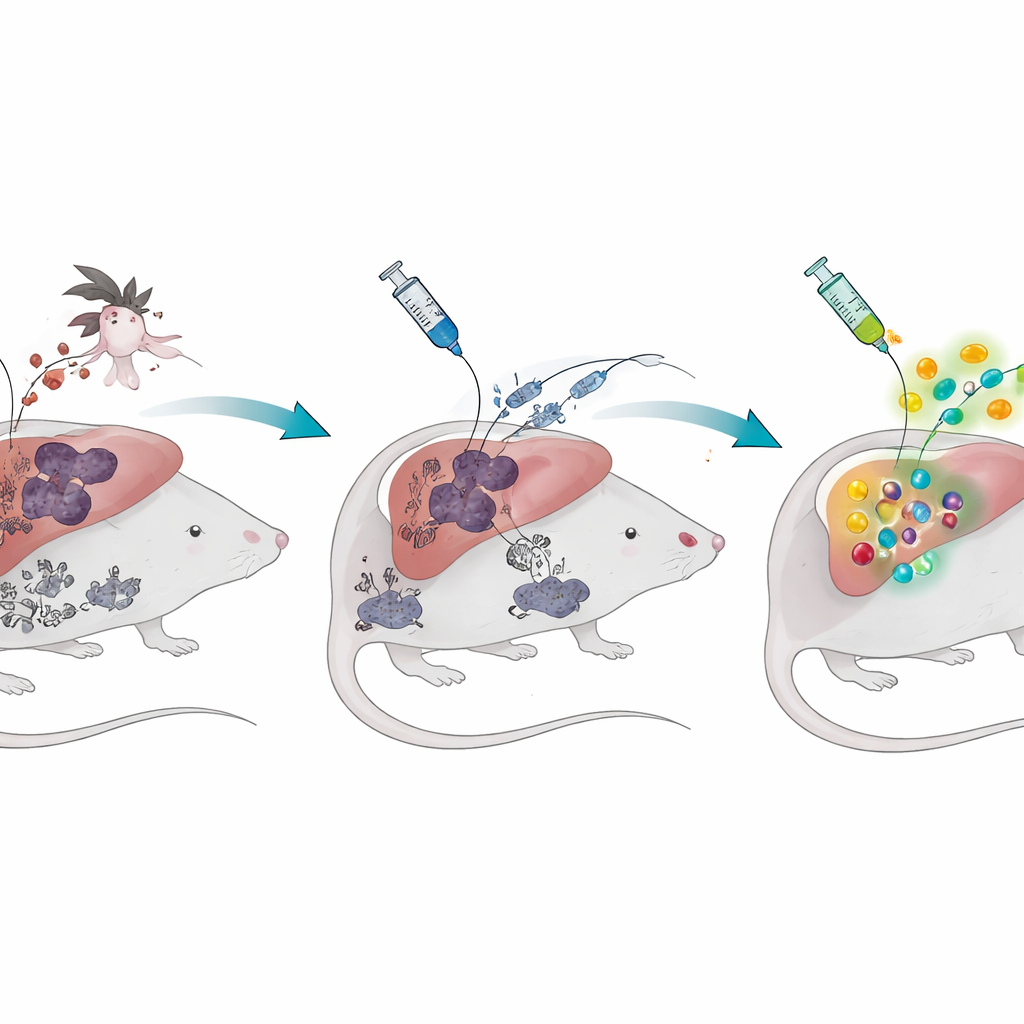
Een verhaal van twee levensstadia van malaria
De malariaparasiet heeft twee belangrijke stadia in het menselijk lichaam. Eerst, na een muggenbeet, infecteert hij geruisloos de lever. Later valt hij de rode bloedcellen aan, wat koorts en ziekte veroorzaakt. Hele-parasietvaccins, zogenaamde door bestraling verzwakte sporozoïeten, richten zich op het stille leverstadium: de parasieten dringen levercellen binnen maar kunnen hun levenscyclus niet voltooien, waardoor het immuunsysteem een veilige preview krijgt. Bij malarianaieve muizen creëert deze strategie grote aantallen gespecialiseerde cytotoxische T-cellen die zich in de lever vestigen en parasieten kunnen uitroeien voordat ze ziekte veroorzaken. Maar toen de onderzoekers muizen eerst een bloedstadium-infectie lieten doormaken en die lieten uitzieken, produceerde hetzelfde vaccin veel minder beschermende T-cellen en waren de dieren veel minder beschermd bij blootstelling aan levende parasieten.
Een hardnekkig pigment dat niet verdwijnt
Het team vroeg zich vervolgens af wat er anders was bij deze "malaria-ervaren" muizen. Een opvallende verdachte was haemozoin, een donker, kristalachtig pigment dat de parasiet maakt in rode bloedcellen om het ijzerrijke afval van de afbraak van hemoglobine te detoxificeren. Dit pigment verdwijnt niet wanneer de infectie voorbij is; het kan maandenlang in de lever, milt en het beenmerg achterblijven. De wetenschappers vonden dat zelfs meer dan een jaar nadat een bloedstadiuminfectie was geëindigd, muizen nog steeds opgeslagen haemozoin en een verzwakte T-celrespons op het leverstadiumvaccin vertoonden. Het toedienen van gezuiverd synthetisch haemozoin alleen — zonder levende parasieten — was voldoende om deze lang aanhoudende vaccinzwakte te imiteren en de bescherming tegen een latere malariablootstelling te verminderen.
Hoe haemozoin immuunsurveillanten in de war brengt
Dieper gravend richtten de onderzoekers zich op dendritische cellen, de surveillanten van het immuunsysteem die stukjes pathogenen opnemen en presenteren aan T-cellen. Voor het hele-parasiet levervaccin om te werken moeten dendritische cellen parasietmateriaal dat uit geïnfecteerde levercellen komt oppakken en tonen aan cytotoxische T-cellen. In celkweekexperimenten toonde het team aan dat haemozoin direct interfereert met deze opnamefase: hoe meer haemozoin dendritische cellen hadden gezien, hoe minder efficiënt ze eiwitantigenen insloten. Dit defect trad op zowel in muizencellen als in menselijke immuuncellen afgeleid van bloeddonoren, en het leek niet afhankelijk van een bekend ontstekingssensor-mechanisme, wat suggereert dat haemozoin zelf fungeert als een fysiek of biochemisch obstakel voor normaal antigenbeheer.
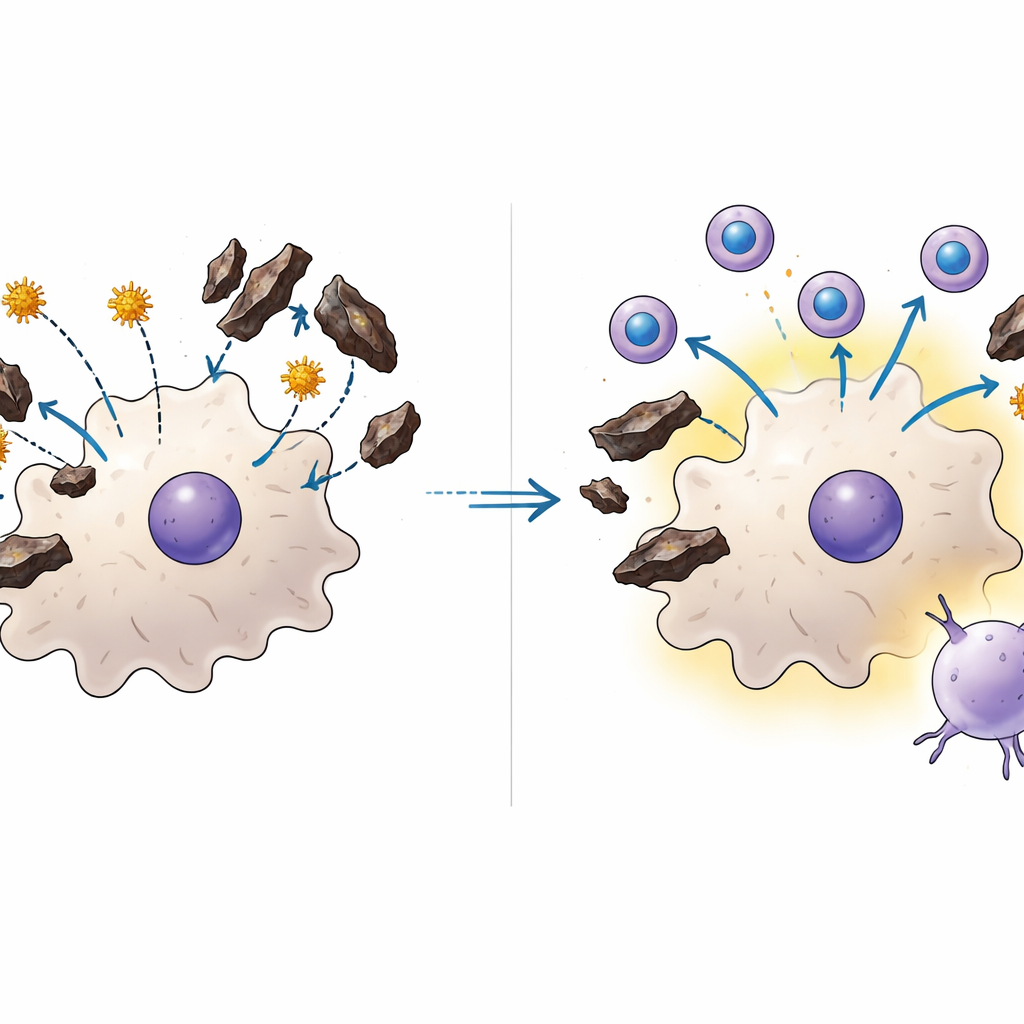
mRNA-vaccins vinden een weg om het obstakel heen
Om te onderzoeken of een ander vaccinformaat dit probleem kon omzeilen, ontwierpen de wetenschappers een mRNA-vaccin verpakt in lipidenandeeltjes. In plaats van parasieteiwitten van buitenaf te leveren, geeft deze aanpak gastheercellen genetische instructies om korte stukjes van meerdere parasieteiwitten binnenin de cel te maken. Bij muizen met en zonder eerdere malaria genereerde het mRNA-vaccin vergelijkbaar sterke cytotoxische T-celresponsen en verbeterde controle van leverinfectie. Opmerkelijk was dat, wanneer het mRNA-vaccin werd gecombineerd met een enkele dosis van het hele-parasiet levervaccin, muizen bijzonder grote pools T-cellen opbouwden die langdurig in de lever verbleven — een celpopulatie die bekendstaat als cruciaal voor snelle bescherming. In kweek bleek dat haemozoin de opname of functie van de mRNA-geladen nanodeeltjes niet blokkeerde, wat verklaart hoe deze strategie kan slagen waar het oudere vaccin alleen faalt.
Wat dit betekent voor toekomstige malariavaccins
In gewone bewoordingen laat de studie zien dat eerdere malariainfecties microscopisch klein, minerale-achtige resten achterlaten die de manier verstoppen waarop bepaalde immuuncellen normaal van vaccins leren, en daarmee een toonaangevende hele-parasiet malariashot verzwakken. Maar door over te schakelen naar, of te combineren met, een mRNA-gebaseerd vaccin dat de instructies voor parasietfragmenten rechtstreeks in cellen binnensluipt, kunnen wetenschappers dit puin omzeilen en sterke bescherming herstellen bij malaria-ervaren gastheren — althans bij muizen. Het werk wijst op haemozoin als een belangrijk obstakel voor vaccins bij mensen die in endemische gebieden wonen, en suggereert dat zorgvuldig ontworpen mRNA- of gecombineerde vaccinregimes een veelbelovende weg kunnen zijn naar effectievere, breed toepasbare malariabescherming.
Bronvermelding: Hassert, M., Drewry, L.L., Pewe, L.L. et al. mRNA vaccination overcomes haemozoin-mediated impairment of whole-parasite malaria vaccines in mice. Nat Microbiol 11, 718–730 (2026). https://doi.org/10.1038/s41564-026-02263-0
Trefwoorden: malariavaccins, hemozoin, mRNA-vaccin, T-celimmuniteit, Plasmodium-infectie