Clear Sky Science · nl
Vergelijkende analyse van deep mutational scanning-datasets in enterovirussen A en B identificeert functionele divergentie en therapeutische doelwitten
Waarom kleine RNA-virusjes belangrijk voor ons zijn
Enterovirussen vormen een grote groep kleine RNA‑virussen die wereldwijd stilletjes circuleren; meestal veroorzaken ze milde verkoudheden of maag-darmklachten, maar soms leiden ze tot verlamming, hartschade of andere ernstige ziekten. We hebben weinig vaccins en nog minder breed werkende medicijnen tegen deze virussen, deels omdat ze zo snel evolueren. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote praktische gevolgen: wanneer deze virussen muteren, welke onderdelen van hun machinerie kunnen vrij veranderen en welke onderdelen zijn zo vitaal dat evolutie ze min of meer bevroren houdt? De antwoorden wijzen op nieuwe strategieën om behandelingen te ontwerpen die het virus moeilijk kan omzeilen.
Het uitlezen van het virale instructieboek, mutatie voor mutatie
De onderzoekers richtten zich op twee humane enterovirussen die heel verschillende ziekten veroorzaken: Enterovirus A71, gekoppeld aan ernstige neurologische aandoeningen bij kinderen, en coxsackievirus B3, geassocieerd met hartontsteking en zelfs alvleesklierkanker. Met een techniek die deep mutational scanning heet, maakten ze virale bibliotheken waarin bijna elke positie in de virale eiwitten systematisch werd veranderd. Deze gemuteerde virussen mochten cellen in kweek infecteren en met hoogdoorvoersequencing werd gemeten hoe elke verandering de virusgroei beïnvloedde. Door elke mutant te vergelijken met het oorspronkelijke virus bouwde het team een gedetailleerde kaart van welke plaatsen in het virale proteoom veranderingen verdragen en welke sterk beperkt zijn. 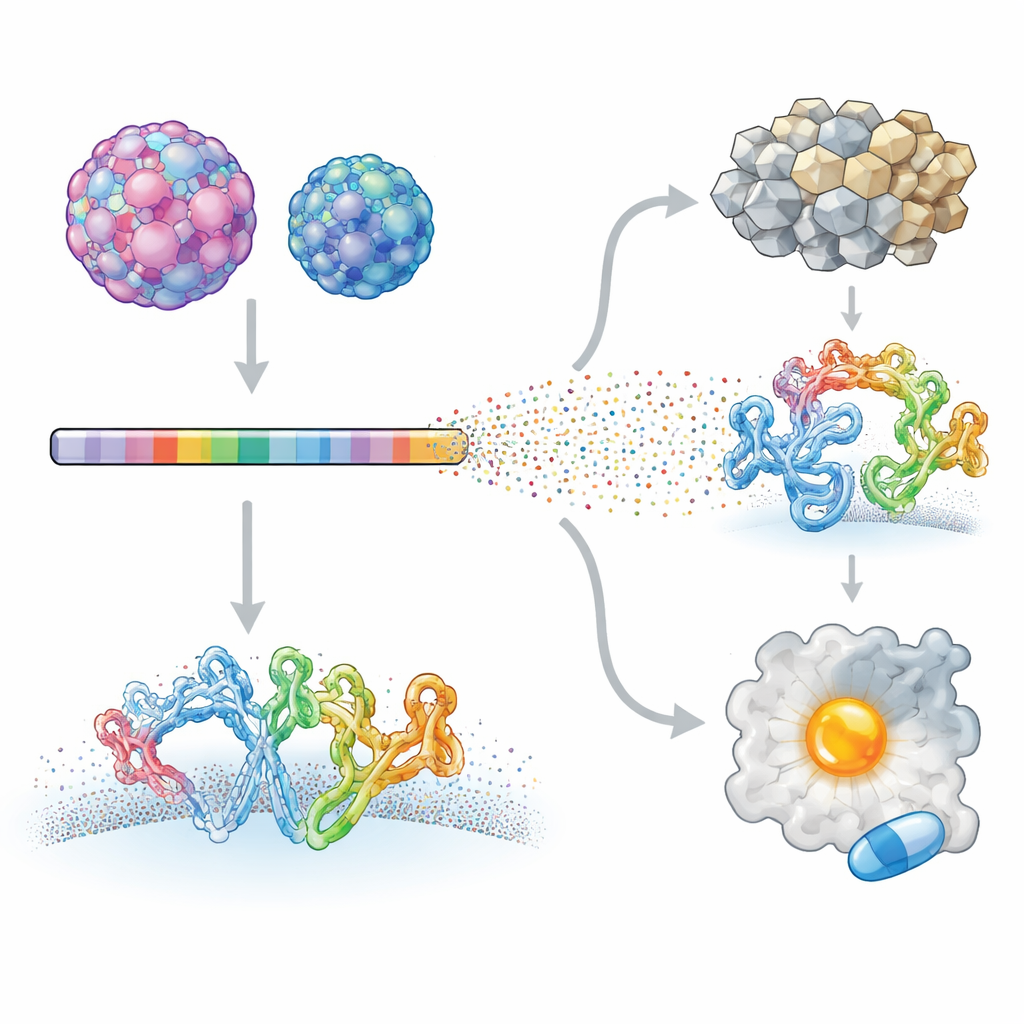
Gedeelde harde grenzen en virus‑specifieke flexibiliteit
Ondanks dat ze slechts ongeveer de helft van hun aminozuursequenties delen, vertoonden de twee virussen opvallend vergelijkbare algemene patronen van beperking. De interne enzymatische “werkpaarden” die het genoom kopiëren, virale eiwitten knippen en RNA ontwinden, waren in beide virussen zeer gevoelig voor mutatie. Evenzo bleken de verborgen oppervlakken die de eiwitmantel (capside) bij elkaar houden moeilijk te wijzigen zonder het virus te beschadigen. Daarentegen waren veel naar buiten gerichte en gastheer-interagerende regio’s vrijer om te veranderen en verschilden vaak sterk tussen de twee soorten. Structurele analyse toonde aan dat geconserveerde, mutatie-intolerante regio’s rond actieve centra en assemblage‑interfaces clusteren, terwijl regio’s die gastheerreceptoren, membranen of immuunsignalen aanraken hotspots van soortspecifieke flexibiliteit vormden.
Hoe virussen cellen binnendringen en afweer ontwijken
Het team zoomde vervolgens in op de moleculaire handdruk tussen virus en gastheer. Enterovirus A71 en coxsackievirus B3 gebruiken verschillende cellulaire receptoren om binnen te komen, en de studie vond dat de exacte contactvlekken op het capsideovervlak behoren tot de meest uiteenlopende regio’s wat betreft mutatietolerantie. Residuen die de receptor voor het ene virus vastgrijpen, zijn in dat virus sterk beperkt maar relatief permissief in het andere, wat weerspiegelt hoe elk zijn aangrijpplatform heeft fijn afgesteld. Eenzelfde divergentie kwam naar voren in een klein membraangebonden eiwit dat 3A heet en helpt bij het herschikken van cellulaire membranen en het aantrekken van gastheerfactoren voor genoomreplicatie. Modellering suggereerde dat de twee virussen deels verschillende contactvlekken op 3A gebruiken om dezelfde gastheerfactor, GBF1, te engageren en mogelijk dit eiwit op verschillende dieptes in membranen invoegen. Deze verschillen helpen verklaren waarom nauwverwante virussen verschillende weefsels kunnen infecteren en uiteenlopende ziektepatronen veroorzaken.
Wat laboratoriumevolutie mist—en wat het goed vastlegt
Om hun celkweekexperimenten in een realistische context te plaatsen, vergeleken de auteurs hun mutatiekaarten met duizenden natuurlijke virussequenties uit patiëntmonsters. Over het algemeen waren plaatsen die in het lab flexibel bleken ook in de natuur variabel, vooral bij bredere vergelijkingen op soortniveau. Wanneer ze echter onderzochten welke specifieke aminozuren op elke plaats werden geprefereerd, kwamen natuurlijke evolutie en labselectie het meest overeen binnen één virussoort. De grootste mismatches waren opvallend aanwezig op het buitenoppervlak van de capsid en op gastheer‑interacterende regio’s van niet‑structurele eiwitten 2A en 3A—juist daar waar immuunreacties en complexe gastheeromgevingen naar verwachting het meest van belang zijn. Dit suggereert dat deep mutational scanning de basismechanische beperkingen van virale eiwitten vastlegt, terwijl echte infecties extra druklagen van immuniteit en weefsel‑tropisme opleggen die moeilijker in vitro te reproduceren zijn.
Het vinden van een gedeelde zwakke plek voor toekomstige geneesmiddelen
Tot slot vroegen de onderzoekers of deze kaarten een gemeenschappelijke achilleshiel voor medicijnontwikkeling konden aanwijzen. Met computationele tools doorzochten ze beide virussen op pockets op eiwitoppervlakken die in principe kleine molecuurgeneesmiddelen zouden kunnen binden. Ze legden daar vervolgens de mutatiegegevens overheen om te zien welke pockets uit residuen bestaan die het virus niet gemakkelijk kan veranderen zonder zichzelf te schaden. Eén pocket stak eruit: gelegen op de 2C helicase—een ringvormige motor die helpt het virale RNA te ontwinden. De vorm en samenstellende residuen zijn sterk geconserveerd over vier grote humane enterovirussoorten, de pocket ligt weg van reeds bekende actieve centra en veranderingen daar zijn zeldzaam in de natuur en sterk nadelig in laboratoriumtests. 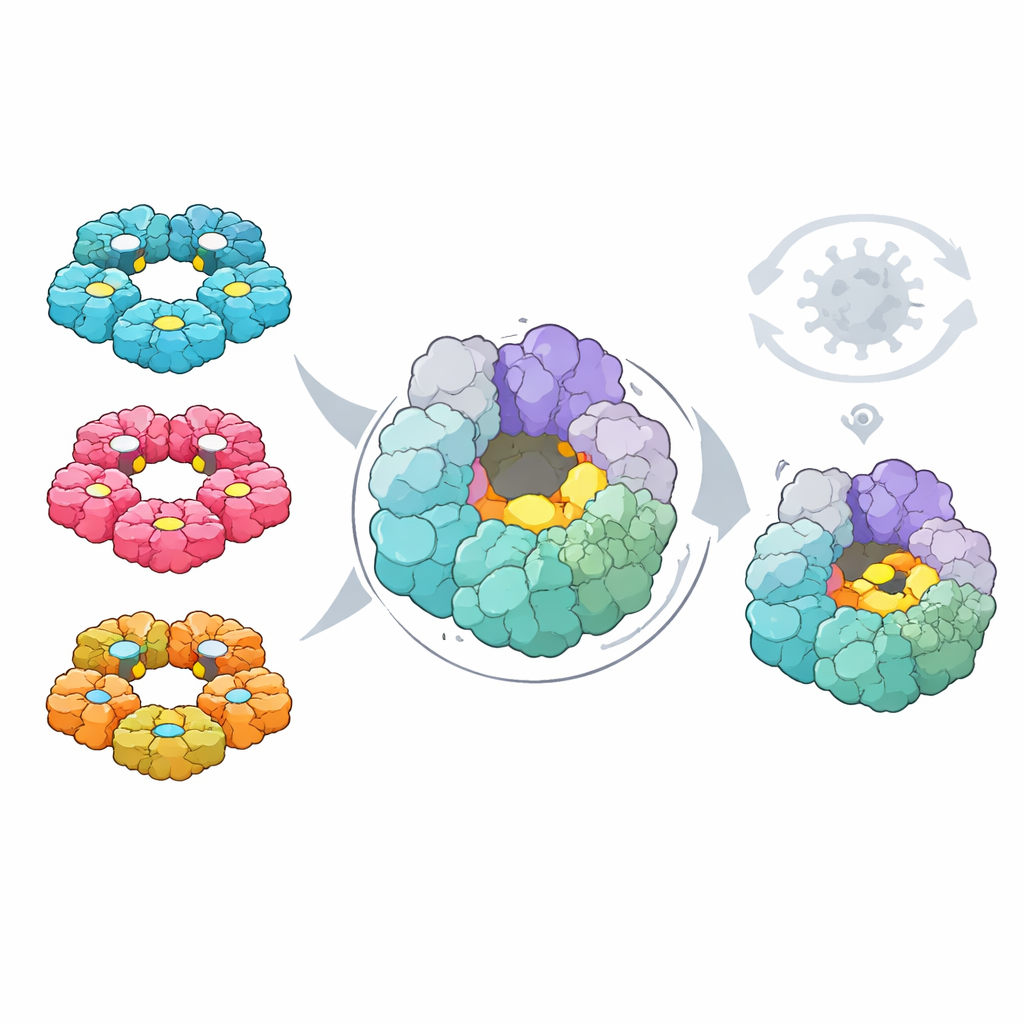
Wat dit betekent voor toekomstige behandelingen
Door systematisch te onderzoeken hoe elke mogelijke enkelvoudige lettersubstitutie twee belangrijke enterovirussen beïnvloedt, onthult deze studie een duidelijke scheiding tussen een gedeelde, starre kern van virale machinerie en meer flexibele, virus‑specifieke interfacegebieden met de gastheer. De geconserveerde kern omvat een nieuw belichte pocket op de 2C helicase die het virus blijkbaar moeilijk kan muteren zonder fitheid te verliezen, waardoor het een aantrekkelijk doelwit is voor breedwerkende antiviralia met een hoge barrière voor resistentie. Tegelijk verklaren de meer aanpasbare buitenoppervlakken en gastheercontactplaatsen waarom verwante virussen zich zo verschillend in het lichaam gedragen en wijzen ze op waar vaccins en immuun-gebaseerde therapieën rekening moeten houden met snelle evolutie. Gezamenlijk bieden deze bevindingen een routekaart voor het ontwerpen van behandelingen die de evolutionaire grenzen van het virus benutten.
Bronvermelding: Álvarez-Rodríguez, B., Bakhache, W., McCormick, L. et al. Comparative analysis of deep mutational scanning datasets in enteroviruses A and B identifies functional divergence and therapeutic targets. Nat Ecol Evol 10, 467–480 (2026). https://doi.org/10.1038/s41559-026-02993-8
Trefwoorden: enterovirussen, virale evolutie, deep mutational scanning, antivirale doelwitten, 2C helicase