Clear Sky Science · nl
Inheemse H2-routes maken biocompatibele hydrogenering van metabolische alkenen in bacteriën mogelijk
Microben veranderen in kleine groene fabrieken
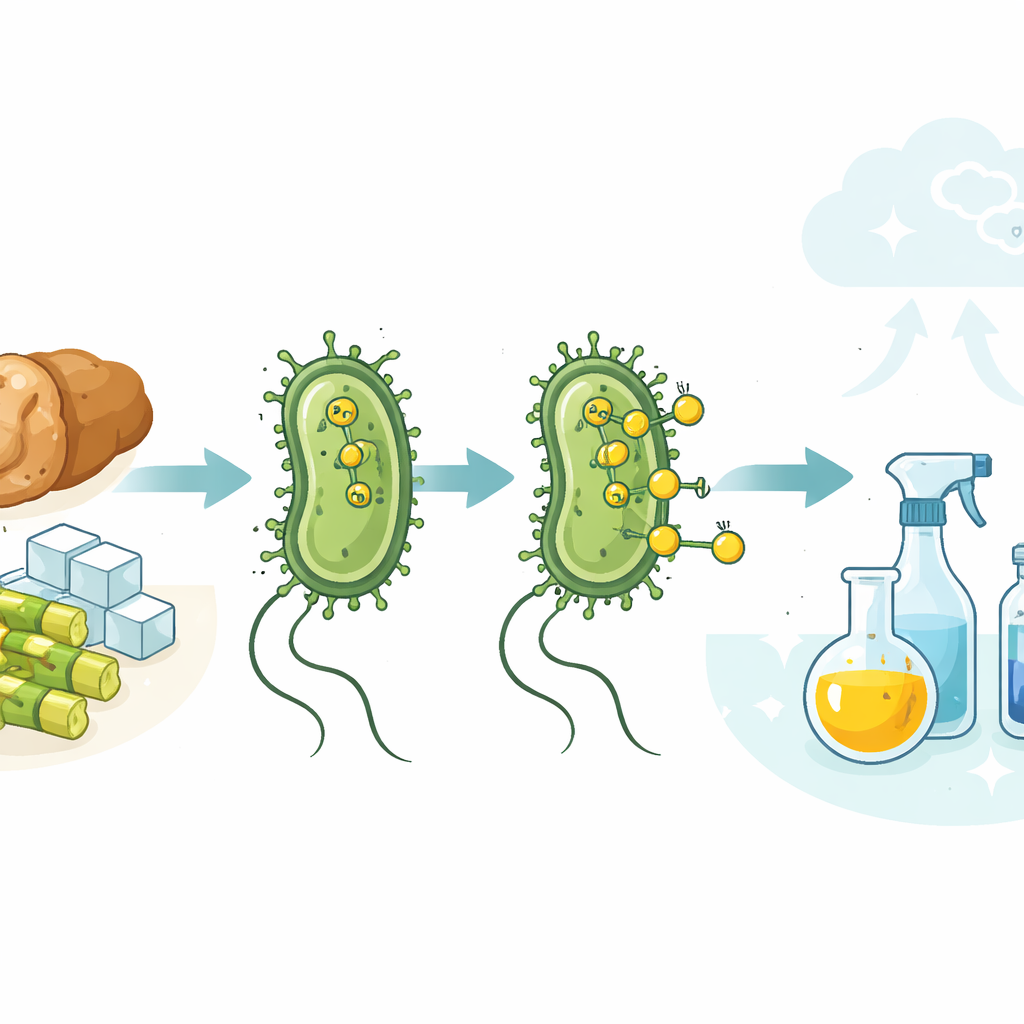
Stel je voor dat gewone darmbacteriën fossiele brandstoffen zouden kunnen vervangen bij de productie van alledaagse chemicaliën — van voedselconserveermiddelen tot kunststoffen — terwijl ze tegelijkertijd voedselafval opruimen. Deze studie laat zien dat standaard laboratoriumstammen van Escherichia coli precies dat kunnen: ze produceren van nature waterstofgas in hun cellen, en die waterstof kan aan het celoppervlak worden benut om industriële chemische reacties uit te voeren onder milde, watergedragen omstandigheden. Door levende microben te combineren met een vast metaal-katalysator schetsen de onderzoekers een route naar schonere, koolstofbesparende productie.
Waarom waterstof belangrijk is voor alledaagse producten
Waterstofgas staat centraal in moderne chemie. Het wordt gebruikt om vloeibare oliën te veranderen in smeerbare producten, ruwe brandstoffen te upgraden en vele ingrediënten voor geneesmiddelen en kunststoffen te maken. Tegenwoordig komt vrijwel al die waterstof uit fossiele brandstoffen, voornamelijk aardgas en steenkool, wat grote hoeveelheden kooldioxide uitstoot. Tegelijk produceren veel microben van nature waterstof wanneer ze suikers afbreken onder zuurstofarme omstandigheden. De uitdaging die de auteurs aangaan, is hoe je deze zachte, biologische waterstofstroom kunt aanboren om dezelfde soorten reacties aan te drijven die de industrie nu uitvoert met hoge drukken, organische oplosmiddelen en fossiele gasbronnen.
Bacteriën een metaal-katalysator laten aandrijven
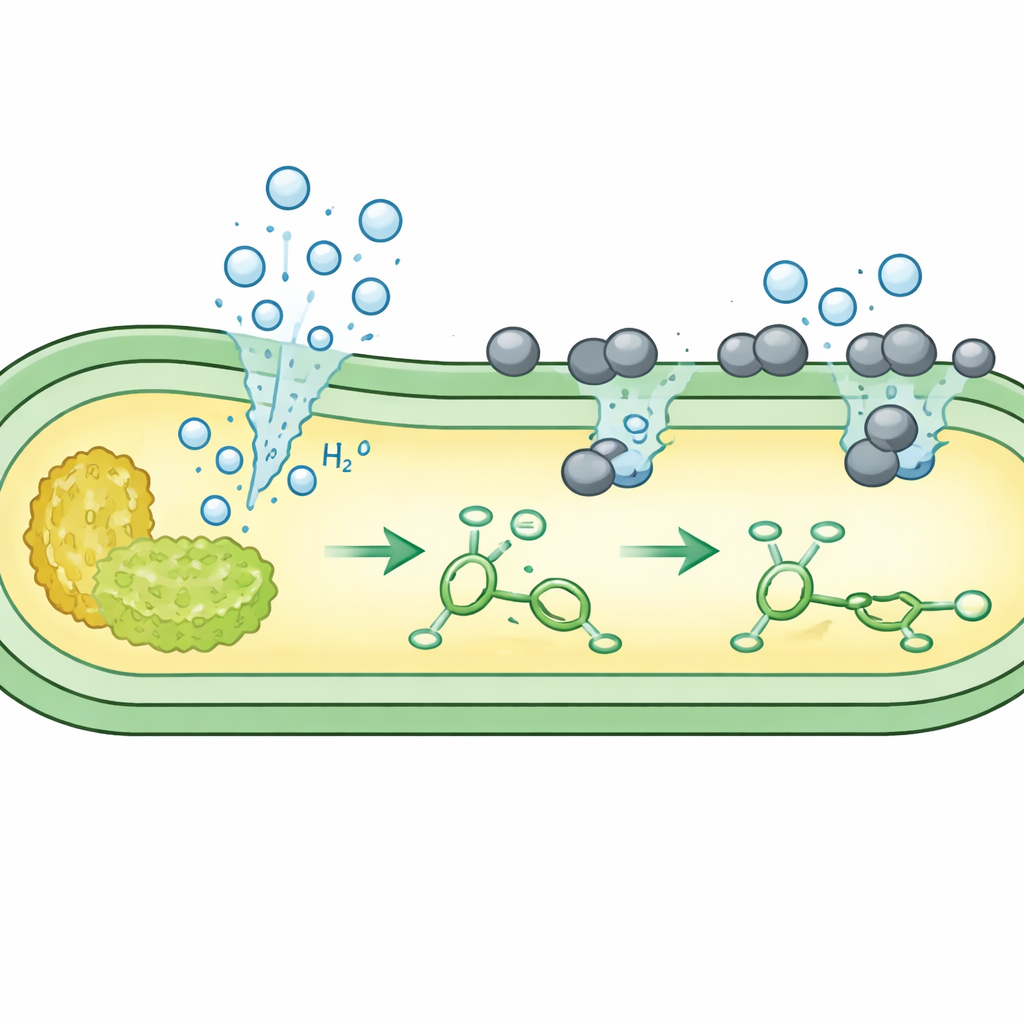
Het team richtte zich op eenvoudige waterstof-toevoegreacties, waarbij een dubbele binding in een molecuul wordt "verzadigd" met waterstof. Ze kweekten meerdere ongemodificeerde E. coli-stammen in suikerhoudende media en voegden vervolgens een fijnverpreide palladiumkatalysator toe die compatibel is met levende cellen. Onder zuurstofvrije omstandigheden zette het native metabolisme van de bacteriën suiker om in formiaat en vervolgens in waterstofgas aan de binnenzijde van het celmembraan. Microscopen toonden dat de positief geladen katalysatordeeltjes zich hechten aan het negatief geladen celoppervlak, waar ze de ontsnappende waterstof ontmoeten. Daar gebruikt het metaal de microbieel geproduceerde waterstof om een testmolecuul, cafeïnezuur, te reduceren tot het verzadigde product met zeer hoge opbrengsten — vaak beter dan die behaald met een eerdere, sterk gemodificeerde stam.
Het assortiment aan producten en grondstoffen uitbreiden
Zodra de basale reactie werkte, probeerden de onderzoekers een breed scala aan moleculen met koolstof–koolstof dubbele bindingen, waaronder plantenafgeleide zuren en langketenige vetachtige verbindingen. Veel werden soepel omgezet in hun verzadigde vormen, sommige vrijwel kwantitatief. Ze bouwden ook E. coli-stammen die extra waterstof produceren door meer metabolische flux naar de native waterstof-vormende route te leiden. Deze versterkte stammen maakten vergelijkbare omzettingen mogelijk met minder metaal-katalysator. In een opvallende wending verving het team pure suiker door gevloeide restjes brood als voedingsbron. Enzymen braken het oude brood af tot glucose, die de bacteriën even effectief fermenteerden, waardoor een veelvoorkomend voedselafval werd omgezet in zowel biologische waterstof als waardetoegevoegde chemicaliën.
Zowel ingrediënt als brandstof in één cel maken
Vervolgens vroegen de auteurs zich af of één enkele bacterie niet alleen de waterstof "reagens" kon maken, maar ook het onverzadigde "substraat" dat bewerkt moest worden. Ze ontwierpen E. coli zo dat suiker eerst stroomt naar routes die aromatische bouwstenen produceren, zoals cinnamisch en coumarinezuur, en naar een andere route die waterstof produceert. Toen de cultuur deze interne metabolieten had opgebouwd, voegden ze de palladiumkatalysator toe. Aan het celoppervlak gebruikte de katalysator de in situ geproduceerde waterstof om de nieuw gevormde dubbele-binding metabolieten om te zetten in volledig verzadigde producten zoals hydrochinamisch zuur, desaminotyrosine en adipinezuur, een belangrijke voorloper voor nylon. In sommige opzetten bereikte deze cometamolisatie bijna volledige conversie, allemaal binnen dezelfde levende cultuur.
De klimaatwinst meten
Om te onderzoeken of deze slimme biochemie daadwerkelijk de planeet ten goede komt, voerde het team een levenscyclusanalyse uit waarin hun hybride "chemo-microbiële" aanpak werd vergeleken met standaard hydrogeneringsroutes aangedreven door fossiele of elektrolytische waterstof. Wanneer biologische waterstof en in-cel productie van substraten werden gecombineerd in een enkel, warmte-efficiënt proces, daalden de totale broeikasgasemissies aanzienlijk. Het gebruik van restbrood als grondstof duwde het systeem nog verder: door storten of verbranding te vermijden en weggegooid voedsel om te zetten in chemicaliën, werden sommige scenario's netto koolstofnegatief, wat betekent dat ze meer broeikasgassen verwijderen dan ze uitstoten.
Wat dit betekent voor toekomstige productie
Simpel gezegd laat de studie zien dat alledaagse bacteriën kunnen worden verleid om zowel de energiebron als de ingrediëntfabriek te zijn voor belangrijke chemische reacties, terwijl een vast metaal op hun oppervlak stilletjes het werk afmaakt. Omdat alles in water gebeurt, bij bijna lichaamstemperatuur en met hernieuwbare of afvalsuikers, zou deze benadering op termijn schonere alternatieven voor traditionele petrochemische fabrieken kunnen bieden. Met verdere engineering van microbieel metabolisme en katalysatoren kan dit levende-celplatform een nieuwe generatie duurzame processen mogelijk maken die hernieuwbare koolstof en weggegooid voedsel omzetten in nuttige producten met een veel kleinere klimaatvoetafdruk.
Bronvermelding: White, M.F.M., Trotter, C.L., Steele, J.F.C. et al. Native H2 pathways enable biocompatible hydrogenation of metabolic alkenes in bacteria. Nat. Chem. 18, 535–543 (2026). https://doi.org/10.1038/s41557-025-02052-y
Trefwoorden: microbieel waterstof, groene chemie, biokatalyse, afval-naar-chemicaliën, duurzame productie