Clear Sky Science · nl
Monovalente pseudo-natuurlijke producten versnellen de afbraak van IDO1 door zijn natuurlijke E3 KLHDC3
Een kankervriendelijk enzym uitschakelen
Ons immuunsysteem speurt voortdurend naar kankercellen, maar tumoren slaan vaak terug door de chemie van het lichaam te kapen. Een centrale speler in dit kat-en-muisspel is een enzym genaamd IDO1, dat tumoren helpt immuuncellen te ontwapenen. Deze studie beschrijft een nieuwe klasse van kleine moleculen die meer doen dan alleen de activiteit van IDO1 blokkeren — ze zetten cellen ertoe aan het enzym helemaal weg te ruimen. Door gebruik te maken van de natuurlijke afvalverwerkingsmachinerie van de cel, kunnen deze verbindingen immuunreacties tegen tumoren herstellen op manieren die oudere medicijnen niet konden.
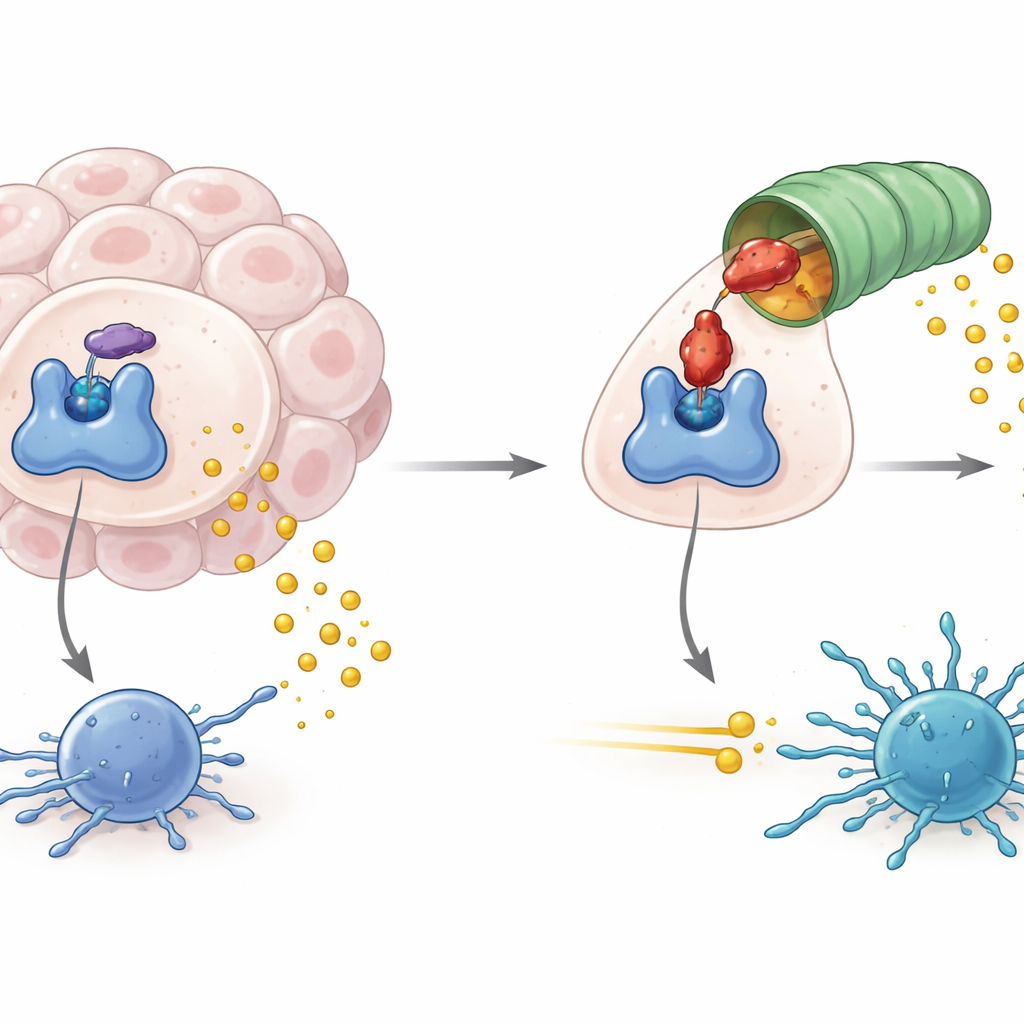
Hoe tumoren een metabole poortwachter uitbuiten
IDO1 zit bij de ingang van een metabole route die het aminozuur tryptofaan afbreekt tot een product dat kynurine heet. Wanneer IDO1 overvloedig en actief is, dalen de tryptofaanniveaus en stijgt kynurine, waardoor een chemische omgeving ontstaat die de activiteit van immuuncellen, waaronder T‑cellen die tumoren bestrijden, dempt. Hoge IDO1‑activiteit is in verband gebracht met niet alleen een zwakkere antitumorimmuniteit maar ook met door virussen veroorzaakte lymfomen en bepaalde vormen van neurodegeneratie. Medicijnontwikkelaars hebben zich daarom gericht op het blokkeren van de enzymatische activiteit van IDO1, in de hoop dit immunosuppressieve signaal af te snijden en bestaande kankerimmunotherapieën effectiever te maken.
Waarom eenvoudige enzymremmers tekortschieten
Ondanks sterke resultaten in dierstudies zijn klinische onderzoeken met traditionele IDO1‑remmers teleurstellend geweest. Een opkomende verklaring is dat IDO1 meer is dan een simpele katalysator. Zelfs wanneer de chemische activiteit wordt geblokkeerd, kan het eiwit zelf als een signaalcentrum fungeren dat nog steeds tumorgroei en -uitzaaiing bevordert. Sommige remmers stabiliseren IDO1 zelfs, waardoor de hoeveelheid van het eiwit in cellen toeneemt. Met andere woorden: alleen het katalytische functioneren uitschakelen kan de pro‑tumor, niet‑enzymatische rollen ongemoeid laten — of erger nog, deze zelfs versterken.
Ontwerpen van verbindingen die zelfvernietiging opwekken
De auteurs doorzochten een grote bibliotheek van "pseudo‑natuurlijke" moleculen — synthetische verbindingen opgebouwd uit fragmenten geïnspireerd door natuurlijke producten maar op nieuwe manieren hercombineerd. Ze vonden een familie moleculen, iDegs genoemd, afgeleid van een plantaardig bouwblok genaamd (−)-myrtanol. Deze verbindingen binden in de gebruikelijke pocket van IDO1 voor zijn ijzerhoudende cofactor, heem. Door heem te verdringen verzwakken iDegs zowel het vermogen van IDO1 om kynurine te produceren als, cruciaal, ze herschikken een deel van de staartregio van het eiwit. Hoge‑resolutie kristalstructuren laten zien dat wanneer iDegs de heemplaats bezetten, ze een C‑terminale helix lossmaken en deels disorder veroorzaken die normaal in een compacte, beschermde conformatie gehouden wordt.
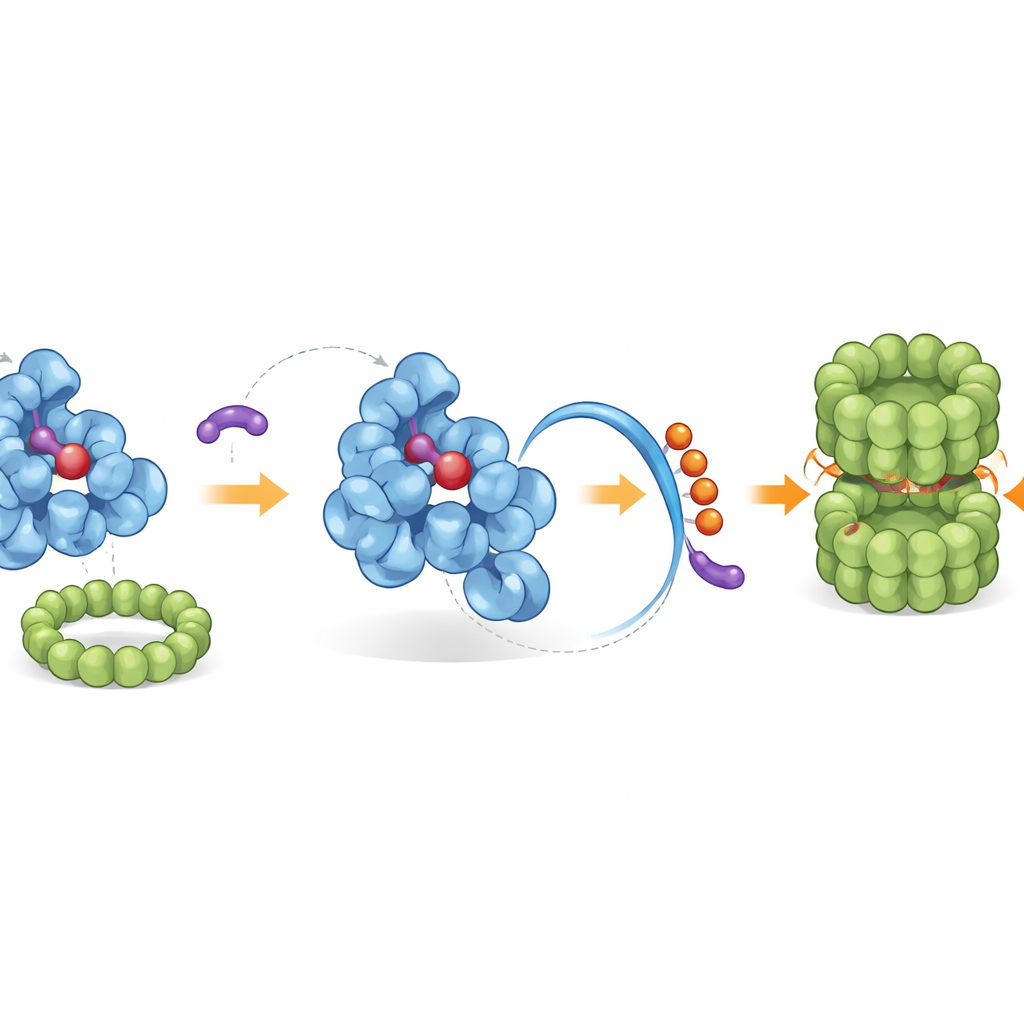
De natuurlijke opruimploeg van de cel inschakelen
De herconfigureerde staart onthult een ingebouwd "eindlabel" dat de afvalverwerkingsmachinerie van de cel herkent. Met behulp van genetische screens en biochemische reconstructie identificeerden de onderzoekers een specifiek ligasecomplex, CRL2–KLHDC3 genaamd, dat op natuurlijke wijze kleine ubiquitine‑"vlaggetjes" aan IDO1’s blootliggende staart bevestigt, waardoor het gemarkeerd wordt voor vernietiging door het proteasoom — de moleculaire versnipperaar van de cel. Onder normale omstandigheden wordt alleen de heem‑vrije vorm van IDO1 efficiënt op deze manier gemarkeerd, terwijl heem‑gebonden IDO1 beschermd is. iDegs verschuiven dit evenwicht door uitsluitend aan de heem‑vrije vorm te binden en zo de natuurlijke afbraakroute te versterken. Krachtige leden van de serie blokkeren niet alleen kynurineproductie maar verhogen ook de ubiquitine‑labeling van IDO1 en verlagen scherp de eiwitniveaus in verschillende kankerceltypes.
Het lot van IDO1 — en immuunreacties — veranderen
Dit tweevoudige werkingsmechanisme heeft belangrijke functionele consequenties. In migratieassays met eierstokkankercellen versnelde een klinisch onderzochte IDO1‑remmer die het enzym stabiliseert de celbeweging juist, in overeenstemming met IDO1’s niet‑enzymatische, pro‑tumorale rol. Daarentegen vertraagde een iDeg‑verbinding de migratie, wat overeenkomt met zowel enzymremming als verlies van het eiwit zelf. De studie onthult daarmee een nieuwe manier om IDO1 te manipuleren: niet door het met een omvangrijk ontworpen molecuul geforceerd naar een vreemd ligase te trekken, maar door een bestaande, native afbraakroute in cellen te "overklokken".
Wat dit kan betekenen voor toekomstige kankertherapieën
Voor niet‑specialisten is de kernboodschap dat de kwaliteit — niet alleen de hoeveelheid — van enzyminhibitie ertoe doet. Deze nieuwe kleine moleculen werken als precieze schakelaars: ze vergrendelen IDO1 in een kwetsbare vorm die de cel klaar is om te vernietigen, en snijden zo zowel diens metabole als signaalgevende bijdragen aan het overleven van tumoren af. Omdat iDegs compact, geneesmiddelachtige eigenschappen hebben en vertrouwen op het eigen ligase van de cel voor het verwijderen van IDO1, bieden ze mogelijk een subtielere en breder toepasbare benadering dan eerdere "eiwit‑verwoester"‑geneesmiddelen. Als vergelijkbare strategieën op andere probleem‑eiwitten kunnen worden toegepast, wijst dit werk op een nieuwe generatie therapieën die zieke cellen ertoe brengen hun eigen moleculaire wapens te ontmantelen.
Bronvermelding: Hennes, E., Lucas, B., Scholes, N.S. et al. Monovalent pseudo-natural products supercharge degradation of IDO1 by its native E3 KLHDC3. Nat. Chem. 18, 585–596 (2026). https://doi.org/10.1038/s41557-025-02021-5
Trefwoorden: IDO1, kankerimmunotherapie, gerichte eiwitafbraak, ubiquitine-ligase, klein-moleculaire degrader