Clear Sky Science · nl
Biocompatibele ligandbalancering in overgangsmetaalcoördinatie maakt goedaardige eiwit-arylering in cellen mogelijk
Metalen als zachte gereedschappen voor cellen
Veel krachtige chemische reacties berusten op metalen, maar breng diezelfde metalen in de buurt van levende cellen en er ontstaat meestal problemen: schade, stress en celdood. Deze studie laat zien dat met de juiste moleculaire "greep" rond een nikkelatoom het mogelijk is een verfijnde reactie binnen levende cellen uit te voeren zonder ze te schaden. Die doorbraak stelt wetenschappers in staat duizenden specifieke plekken op eiwitten te markeren en zelfs de verschijning van moeilijk te volgen pathogenen te volgen, wat nieuwe wegen opent om in kaart te brengen wat er werkelijk in cellen gebeurt bij gezondheid en ziekte.
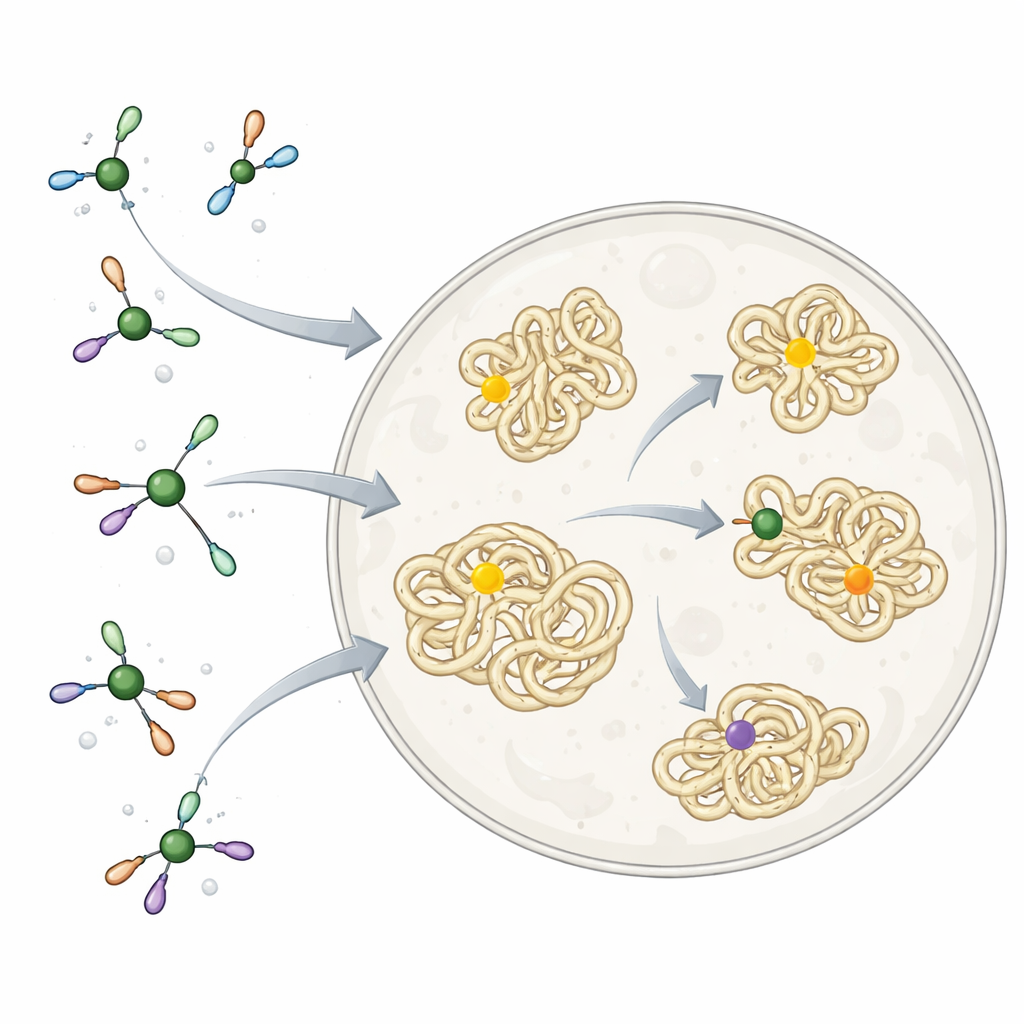
Waarom metalen zowel vriend als vijand zijn
Nikkel en andere metalen functioneren al stilletjes in ons lichaam als onderdelen van natuurlijke enzymen, maar ze kunnen ook toxisch zijn als ze zich op de verkeerde plek binden. De natuur lost dit op door metalen te omringen met zorgvuldig gekozen kleine moleculen en eiwitten die ze naar de juiste doelen sturen en ongewenste reacties blokkeren. Chemici gebruiken daarentegen vaak metaalreagentia die extreem reactief zijn en totaal niet op het leven zijn afgestemd. Deze zijn uitstekende hulpmiddelen om complexe moleculen in een reageerbuis te bouwen, maar veel te hard om vrij in cellen te gebruiken, vooral wanneer het doel is een kleine "tag" op een specifiek aminozuur in een eiwit te koppelen zonder de rest van de cel te verstoren.
Ontwerp van een vriendelijker nikkelreagens
De onderzoekers lieten zich inspireren door hoe cellen zelf met nikkel omgaan. Ze bouwden een reeks nikkelcomplexen gewikkeld in een eenvoudige, biocompatibele ligand genaamd TMEDA. Dit kleine molecuul werkt als een zachte klem: strak genoeg om te voorkomen dat nikkel zich aan de verkeerde cellulaire componenten hecht, maar los genoeg om een sleutelreactie te laten verlopen. De reactie koppelt een "aryl"-fragment — een plat, ringvormig groepje dat vaak in geneesmiddelen voorkomt — aan het zwavelatoom van het aminozuur cysteïne in eiwitten. Aan gezuiverde eiwitten in oplossing hechtten deze nikkelcomplexen zeer snel en selectief arylgroepen aan enkele cysteïneplaatsen, en ze werkten op veel verschillende eiwitsvormen en posities, wat aantoonde dat de chemie breed compatibel was met echte biologische moleculen.
Eiwitten in levende cellen bewerken
Vervolgens vroegen de onderzoekers of deze reagents ook in levende cellen konden werken zonder giftig te zijn. Ze vergeleken eenvoudige nikkelsaldi, waarvan bekend is dat ze schadelijk zijn, met de TMEDA-gebonden nikkelcomplexen. In mammalencellen veroorzaakten de eenvoudige nikkelbronnen aanzienlijke celdood bij relatief lage doses, maar de ligand‑gebalanceerde complexen bleven goed verdragen, zelfs bij millimolaire concentraties. Dat veiligheidsvenster stelde de onderzoekers in staat bacteriële en mammelencellen lang genoeg in de nikkelreagentia te baden zodat deze naar binnen konden glippen en eiwitten konden modificeren. Door in één versie van de arylgroep een azide-"greep" in te bouwen, konden ze na de reactie fluorescerende kleurstoffen of biotintags aan klikken, wat een duidelijke, dosisafhankelijke kleuring van eiwitten door het cytoplasma en de kern van levende cellen onthulde.
Reactieve eiwitplaatsen in het hele proteoom in kaart brengen
Met een veilige en snelle in‑cellreactie in handen zetten de auteurs deze om tot een ontdekkingstool. Ze behandelden levende menselijke cellen met het azide‑dragende nikkelreagens en gebruikten vervolgens een photocleaveerbare biotintag en geavanceerde massaspectrometrie om precies te zien welke cysteïnes gemodificeerd waren. In één experiment detecteerden ze bijna 11.000 cysteïneplaatsen verspreid over bijna 5.000 eiwitten — ongeveer twee keer zoveel eiwitten als alle eerdere levende‑cel cysteïne‑profileringstudies samen. De labeling was sterk selectief voor cysteïne en toonde weinig bias voor bepaalde eiwittypes, locaties of bekende actieve centra. Opmerkelijk was dat veel van de doelwit‑eiwitten als "niet‑ligandabel" werden beschouwd volgens de huidige standaarden van geneesmiddelenontdekking, waaronder eiwitten met lage abundanties in signaalroutes en redox‑gevoelige schakelaars die moeilijk alleen via genetica te bestuderen zijn.
Verborgen pathogenen in realtime volgen
Dezelfde chemie bleek ook gevoelig genoeg om vreemde eiwitten die tijdens een infectie worden gemaakt op te sporen. In menselijke cellen met latente virale sequenties detecteerde de methode virale transcriptiefactoren die in extreem lage hoeveelheden aanwezig waren, inclusief alternatieve splice‑vormen. Het team infecteerde daarna cellen met twee heel verschillende pathogenen: de intracellulaire bacterie Chlamydia trachomatis en Sindbisvirus, een RNA‑virus verwant aan chikungunya. Door geïnfecteerde cellen op verschillende tijdstippen met het nikkelreagens te pulseren, konden ze cysteïneplaatsen vastleggen op belangrijke bacteriële ribosomale en regulatorische eiwitten terwijl de bacterie tussen levenscyclusstadia schakelde, en op kritische virale niet‑structurele eiwitten die de RNA‑replicatie aandrijven. Deze gemarkeerde plaatsen vormen nu opvallende potentiële kwetsbaarheden voor toekomstige antivirale of antibacteriële strategieën.
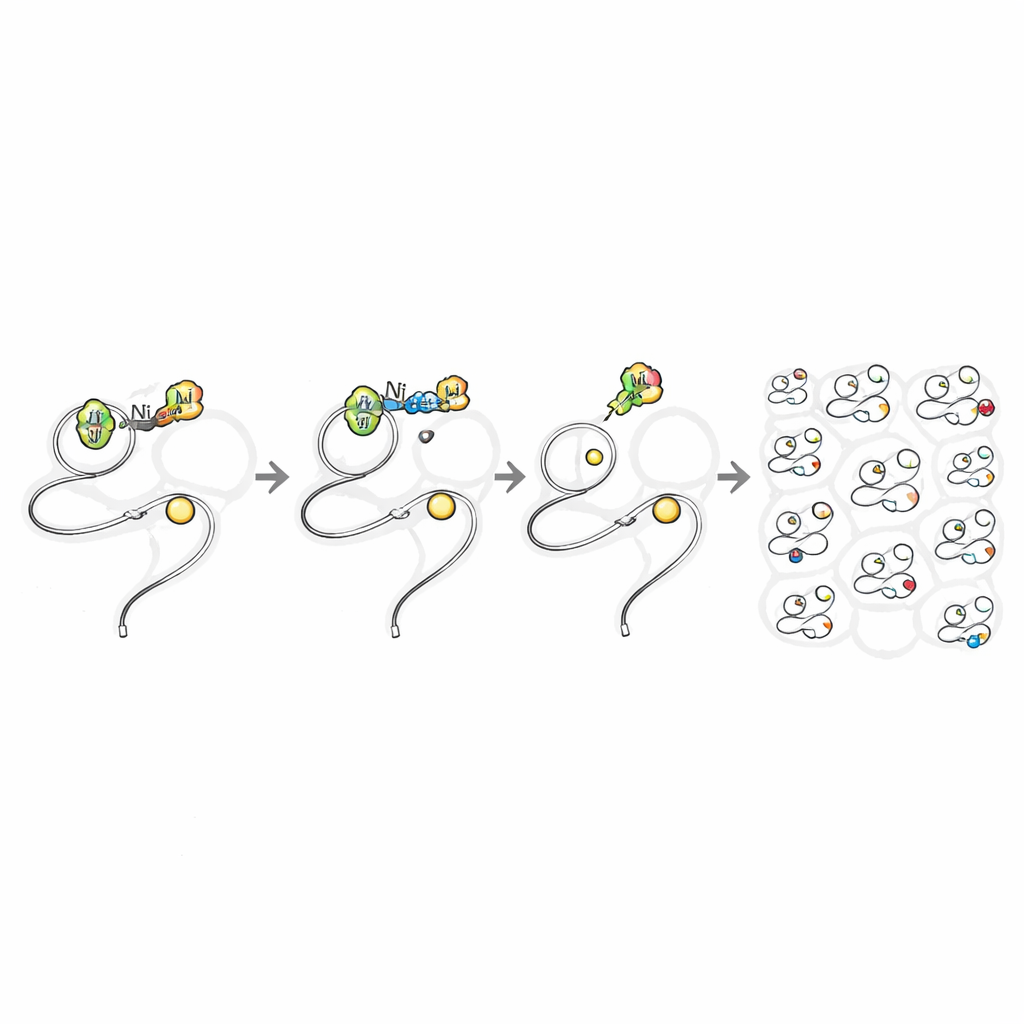
Wat dit betekent voor toekomstige celchemie
Door de ligandenschil rond nikkel zorgvuldig te balanceren, toont dit werk aan dat een traditioneel risicovolle metaal een precieze, covalente eiwit‑bewerkingsreactie diep binnen levende cellen kan uitvoeren met minimale schade. Dat maakt het mogelijk een gedetailleerde, functionele kaart te tekenen van reactieve cysteïneplaatsen in het hele proteoom, inclusief eiwitten die schaars, vluchtig of moeilijk te beïnvloeden zijn met geneesmiddelen. Het biedt ook een manier om pathogenen binnen hun gastheercellen op het niveau van individuele aminozuren te volgen en te onderzoeken. Breder gezien suggereert de studie dat veel andere "verboden" metaalchemieën op vergelijkbare wijze kunnen worden getemd, waarmee een nieuw tijdperk wordt geopend waarin de krachtige gereedschappen van de synthetische chemie veilig binnen levende systemen kunnen opereren.
Bronvermelding: Fu, X., Liu, W., Demyanenko, Y. et al. Biocompatible ligand balancing in transition metal coordination enables benign in-cell protein arylation. Nat. Chem. 18, 457–472 (2026). https://doi.org/10.1038/s41557-025-02017-1
Trefwoorden: cysteïneprofilering, nikkelbioconjugatie, eiwitlabeling in levende cellen, chemoproteomica, pathogeenproteoommapping