Clear Sky Science · nl
Lysine-11-ubiquitinering stuurt type I/III interferoninductie door cGAS–STING en Toll-like receptoren 3 en 4
Hoe onze cellen alarm slaan
Wanneer virussen of gevaarlijke moleculen het lichaam binnendringen, moeten onze cellen binnen enkele minuten beslissen of ze krachtige antivirale alarmsignalen, interferonen genoemd, moeten activeren. Deze signalen kunnen ons beschermen tegen ernstige infecties — maar bij verkeerde activering veroorzaken ze ook schadelijke auto-immuunziekten. Deze studie onthult een tot nu toe verborgen moleculair “schakelbord” in cellen dat helpt te bepalen wanneer interferonreacties aan moeten en wanneer ze onderdrukt moeten worden. Inzicht in dit schakelbord geeft aanknopingspunten voor betere vaccins, antivirale therapieën en behandelingen voor interferon-gedreven aandoeningen.
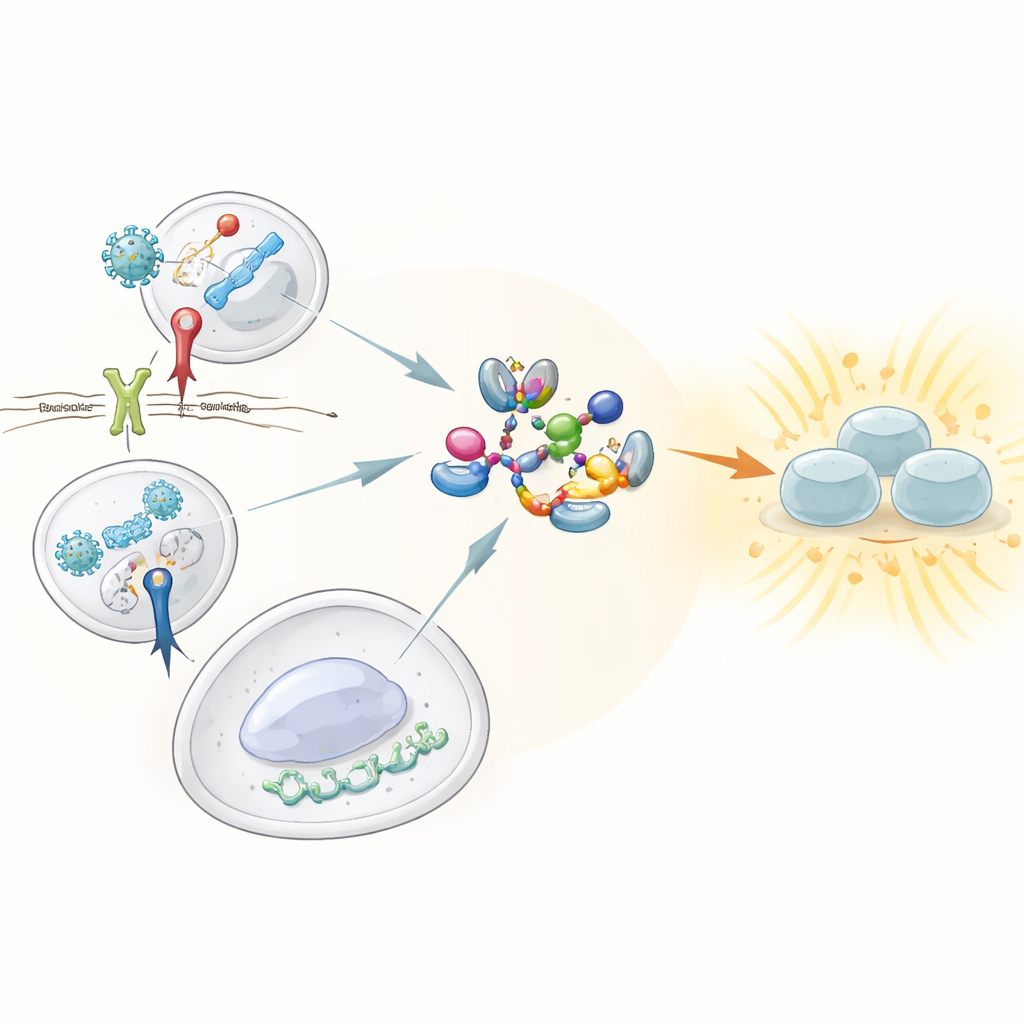
Wachters die gevaar detecteren
Ons aangeboren immuunsysteem steunt op wachters, de patroonherkenningsreceptoren, die patrouilleren op herkenbare kenmerken van virussen en bacteriën. Drie ervan springen eruit vanwege hun vermogen sterke interferonreacties te veroorzaken: Toll-like receptor 3 (TLR3), die dubbelstrengs viraal RNA herkent; Toll-like receptor 4 (TLR4), die een bestanddeel van bacteriële celwanden detecteert; en de cGAS–STING-route, die vreemd DNA op de verkeerde plaats binnen cellen signaleert. Alle drie moeten een centraal enzym, TBK1, activeren, dat op zijn beurt de transcriptiefactor IRF3 inschakelt om de productie van type I- en III-interferonen op gang te brengen. Tot nu toe was onduidelijk hoe deze sensoren samenkomen op TBK1 om het in zijn actieve toestand te zetten.
Een verborgen moleculaire schakel
De onderzoekers ontdekten dat een eiwit genaamd ANKIB1 fungeert als cruciale verbinding tussen deze sensoren en TBK1. ANKIB1 is een enzym dat kleine moleculaire labels, bekend als ubiquitineketens, aan andere eiwitten koppelt. Belangrijk is dat het een specifiek type keten bouwt, gebaseerd op een koppeling genaamd “K11”, die eerder vooral bekend was vanwege rollen in celdeling en niet zozeer in immuniteit. In menselijke cellen zonder ANKIB1 leidde stimulatie van TLR3 of activatie van STING niet meer tot correcte activering van TBK1 en IRF3, en interferongenen werden nauwelijks aangezet. Het terugplaatsen van ANKIB1 herstelde de reactie, wat toont dat dit ene enzym zowel noodzakelijk als voldoende is om deze tak van het antivirale alarm aan te jagen.
Een aanlegplek bouwen voor relais-eiwitten
Nauwkeuriger onderzoek onthulde hoe ANKIB1 zijn invloed uitoefent. Wanneer TLR3 of STING gevaar detecteren, assembleren ze multi-eiwitplatforms die signalosomen worden genoemd. ANKIB1 wordt naar deze platforms gerekruteerd via een regio die ubiquitine herkent. Eenmaal daar voorziet het verschillende sleutelcomponenten — waaronder de adaptereiwitten TRIF en STING zelf, evenals andere signaalelementen — van K11-gekoppelde ubiquitineketens. Deze ketens dienen niet simpelweg als merktekens voor afbraak; in plaats daarvan werken ze als moleculair klittenband. Een ander eiwit, Optineurin (OPTN), wordt specifiek naar deze gewijzigde plekken aangetrokken. Als relaisadapter brengt OPTN vervolgens TBK1 in het complex zodat het geactiveerd kan worden en het signaal doorgeeft aan IRF3 en interferongenen. Wanneer OPTN werd verwijderd, viel de TBK1-activatie weg, wat benadrukt dat K11-gebonden tagging door ANKIB1 en OPTN-binding een enkele, essentiële as vormen.
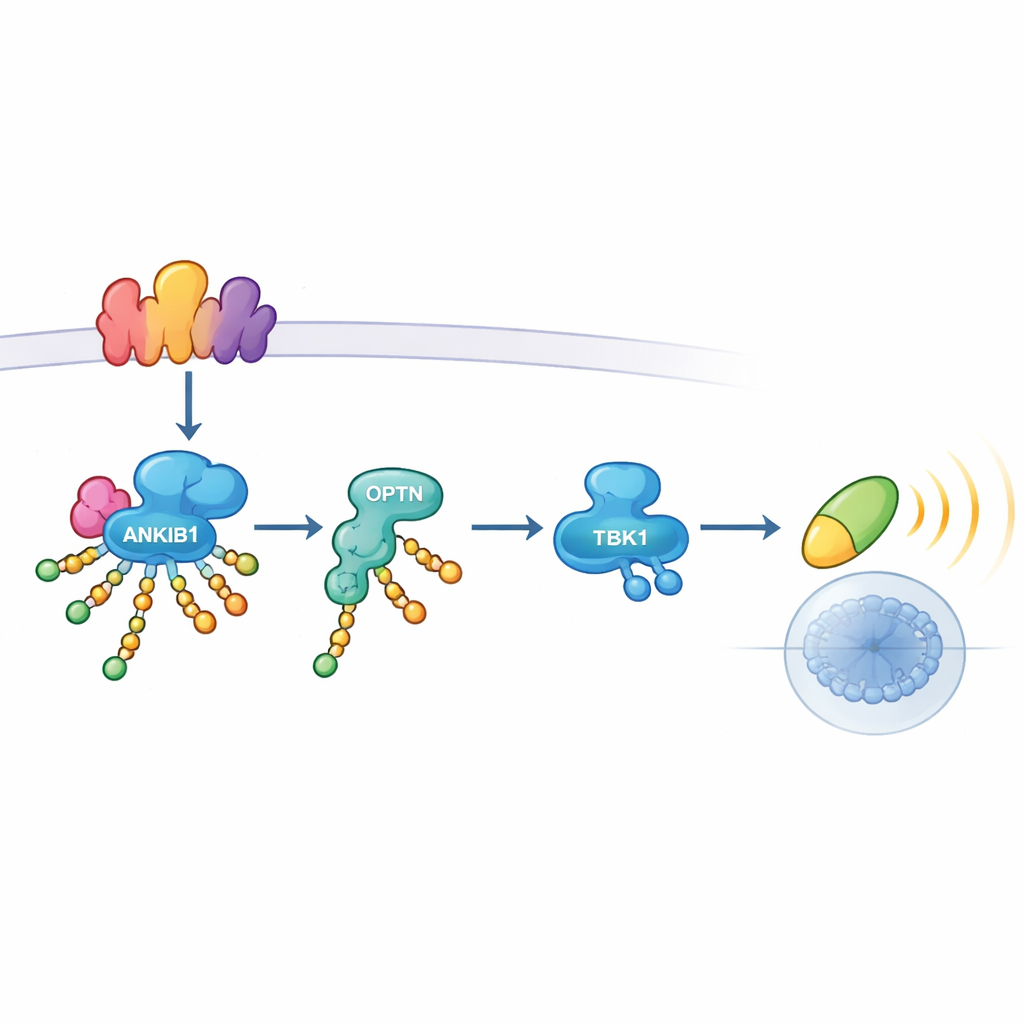
Wanneer deze route van belang is — en wanneer niet
Het team vroeg zich vervolgens af of dit mechanisme universeel is voor alle antivirale sensoren. Ze ontdekten dat ANKIB1 cruciaal is voor interferoninductie via TLR3, de TRIF-afhankelijke arm van TLR4, en de cGAS–STING-route, die allemaal OPTN gebruiken als belangrijke adapter naar TBK1. Ter vergelijking vertrouwt een andere sensor, RIG-I, die viraal RNA detecteert, op een andere set adaptereiwitten en heeft geen ANKIB1 of OPTN nodig om TBK1 te activeren. Experimenten in muizen weerspiegelden deze celgebaseerde bevindingen. Dieren zonder Ankib1 produceerden veel minder interferon na activatie van TLR3 of STING, waren beschermd tegen een dodelend interferon-gedreven ontstekingssyndroom, maar werden veel gevoeliger voor infectie met herpes simplex virus 1, een DNA-virus dat sterk afhankelijk is van cGAS–STING-gedreven interferon voor controle. Reacties op influenzavirus, dat voornamelijk door RIG-I wordt gedetecteerd, bleven grotendeels intact.
Bescherming en schade in balans
Samen onthullen deze resultaten dat door ANKIB1 gegenereerde K11-gekoppelde ubiquitineketens een centrale valuta vormen in een belangrijke tak van aangeboren antivirale signalering. Door aanlegplaatsen voor OPTN te creëren, helpt ANKIB1 de precieze moleculaire relaisopbouw samen te stellen die door TLR3, TLR4 (via TRIF) en cGAS–STING waargenomen gevaar omzet in robuuste interferonproductie. Deze as heeft twee kanten: ze is essentieel voor de verdediging tegen bepaalde virussen, maar voedt ook interferon-gedreven ontstekingsziekte wanneer ze overactief wordt. Omdat de katalytische activiteit en specifieke domeinen van ANKIB1 voor deze functie vereist zijn, vormen ze aantrekkelijke doelen voor toekomstige geneesmiddelen die ofwel schadelijke interferonreacties bij auto-immuun aandoeningen willen dempen of antivirale immuniteit willen versterken waar die te zwak is.
Bronvermelding: Betrancourt, A., Cinko, M.T., Varanda, A.B. et al. Lysine-11 ubiquitination drives type-I/III interferon induction by cGAS–STING and Toll-like receptors 3 and 4. Nat Cell Biol 28, 608–621 (2026). https://doi.org/10.1038/s41556-026-01886-z
Trefwoorden: aangeboren immuniteit, interferonsignalering, ubiquitinering, cGAS–STING-route, virale infectie