Clear Sky Science · nl
Peritumoraal vetweefsel drijft immuunontduiking bij colorectale kanker via adipose–mesenchymale transformatie
Waarom buikvet rond tumoren er toe doet
Colorectale kanker groeit in de darmwand, maar ligt vlak naast een dikke laag buikvet. De meeste mensen zien dat vet als passieve vulling. Deze studie onthult iets onverwachts: het vet rond de tumor kan stilletjes immuuncellen die kanker bestrijden weghalen bij de tumor, waardoor de kanker zich kan verbergen voor het immuunsysteem. Inzicht in dit verborgen touwtrekken wijst op nieuwe manieren om te voorspellen wie op immunotherapie zal reageren en hoe die behandelingen beter kunnen werken.
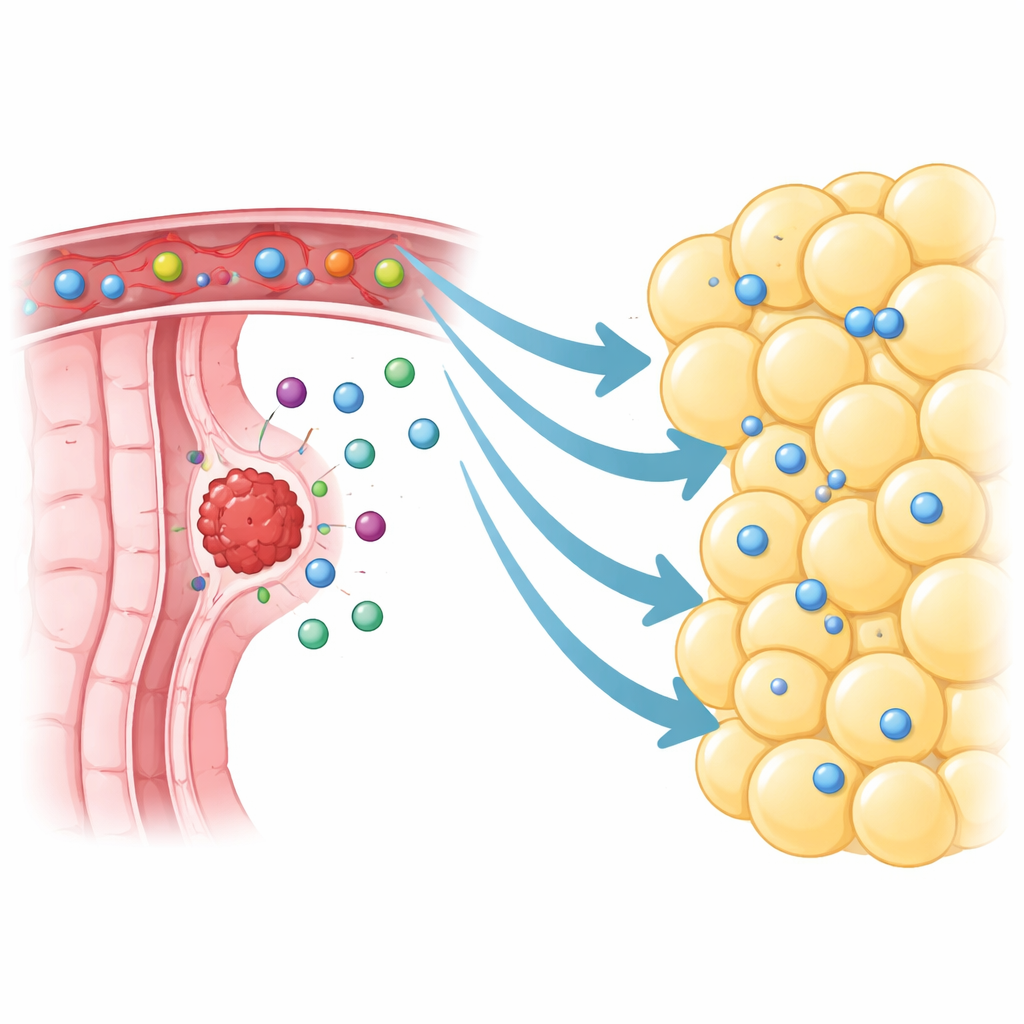
Een druk immuunnabuurschap naast de tumor
De onderzoekers richtten zich op visceraal vet dat direct rond colorectale tumoren ligt, peritumoraal visceraal adipose weefsel genoemd. Met single‑cell RNA‑sequencing brachten ze meer dan 370.000 individuele cellen in kaart uit tumoren, nabijgelegen vet, verder weg gelegen vet en normaal weefsel. In plaats van stil en inactief te zijn, zat het vet naast tumoren vol immuuncellen, met name T‑cellen en B‑cellen. Ze vonden zelfs georganiseerde clusters die op mini‑lymfeklieren leken, een aanwijzing dat dit weefsel actieve immuunreacties kan herbergen. Vergeleken met verder verwijderd vet bevatte het peritumoraal vet veel meer lymfocyten, waaronder geheugen‑ en tumor‑specifieke killer‑T‑cellen die in theorie op zoek zouden moeten zijn naar kanker.
Als behulpzame immuuncellen op de verkeerde plek terechtkomen
Om te onderzoeken of dit immuunrijke vet hielp of juist hinderde, gebruikten de onderzoekers muismodellen waarin tumoren werden geïmplanteerd naast een vetkussen dat lijkt op de menselijke situatie. Ze verwijderden vervolgens dit nabijgelegen vet chirurgisch of losten het chemisch op. Contra‑intuïtief vertraagde het verwijderen van het peritumoraal vet de tumor‑groei. Tumoren van muizen die dit vet kwijt waren, bevatten meer CD4‑ en CD8‑T‑cellen, inclusief T‑cellen die tumorantigenen herkenden. Aanvullende experimenten waarin donorcellen werden gevolgd toonden dat, wanneer het vet aanwezig was, veel van deze cellen zich ophoopten in het vetkussen in plaats van in de tumor. Het weghalen van het vet leidde ertoe dat de cellen richting de tumor gingen en de antikankerrespons versterkten. Met andere woorden: het vet fungeerde als een concurrerend reservoir dat immuuncellen opslorpte en verhinderde dat ze hun echte doel bereikten.
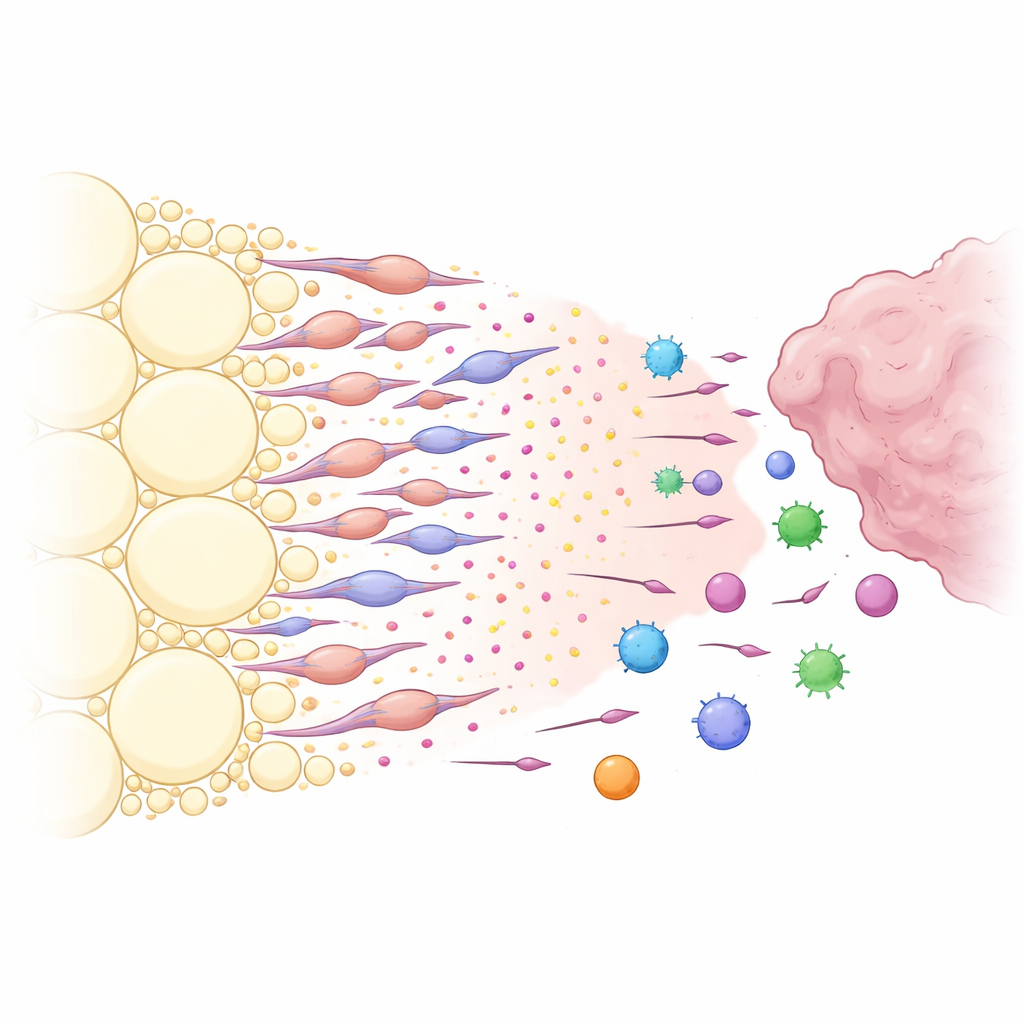
Een chemische lokroep opgebouwd door getransformeerde vetcellen
Wat maakte het peritumoraal vet zo goed in het vangen van immuuncellen? Door de communicatie tussen celtypen te analyseren identificeerden de onderzoekers een krachtig chemisch pad dat draait om het molecuul CXCL12 en zijn receptor CXCR4. Stromale cellen in het vet nabij de tumor produceerden hoge niveaus van CXCL12, terwijl veel immuuncellen CXCR4 tot expressie brachten en daardoor gevoelig waren voor dit signaal. Het lokaal blokkeren van CXCL12 in het vet, of het genetisch verwijderen ervan in het vetstroma, deed tumoren krimpen en maakte het mogelijk dat meer CXCR4‑positieve immuuncellen de tumor binnendrongen in plaats van afgeleid te worden. Het team ontdekte vervolgens dat de belangrijkste CXCL12‑producenten geen gewone vetcellen waren, maar een speciale groep vet‑afgeleide, fibroblast‑achtige cellen die zij adipose‑afgeleide cancer‑associated fibroblasts noemden. Door tumor‑afgegeven factoren, met name de groeifactor TGF‑β1, werden lokale adipose stromale cellen gedwongen te transformeren tot deze fibroblast‑achtige cellen, die op hun beurt grote hoeveelheden CXCL12 en andere groei‑bevorderende signalen afscheidden.
Een schild veranderen in een zwakke plek
Aangezien deze getransformeerde cellen immuuncellen wegsturen van tumoren, onderzochten de onderzoekers of het ontmantelen van deze “immuunsink” de immunotherapie kon verbeteren. In muizen die zo waren geconstrueerd dat de adipose‑afgeleide cancer‑associated fibroblasts selectief konden worden verwijderd, werd een behandeling met een PD‑1‑blokkerende antilichaam veel effectiever: tumoren groeiden minder en meer tumor‑specifieke en CXCR4‑positieve T‑cellen infiltreerden de kanker. Evenzo werkten geneesmiddelen of antilichamen die ofwel CXCL12 ofwel zijn receptor CXCR4 blokkeerden synergetisch met PD‑1‑blokkade in zowel subcutane als orthotopische modellen van colorectale kanker. Deze combinaties verminderden niet alleen de tumoromvang maar hervormden ook het immuurlandschap binnenin de tumor.
Aanwijzingen uit patiëntscans en wat hierna komt
Het team vroeg zich vervolgens af of hun bevindingen relevant waren bij echte patiënten. In een groep mensen met lokaal gevorderde colorectale kanker die gecombineerde chemotherapie, radiotherapie en PD‑1‑immunotherapie kregen, hadden degenen met een complete respons de neiging een kleiner volume peritumoraal visceraal vet op MRI te hebben vóór de behandeling. Kwantitatief voorspelde het oppervlak van dit vet de therapierespons beter dan enkele standaard weefselmarkeerders, en patiënten met grote volumes peritumoraal vet hadden veel lagere responspercentages. Voor een niet‑specialist is de conclusie opmerkelijk: niet alleen de tumor zelf, maar ook het vet dat er direct omheen ligt, kan bepalen hoe goed immunotherapie werkt. Door op dit vet te focussen — hetzij door het te meten om behandelbeslissingen te sturen, hetzij door de getransformeerde stromale cellen en het CXCL12–CXCR4‑signaal aan te pakken — kan het mogelijk zijn een beschermend schild voor de tumor om te buigen naar een therapeutische zwakke plek.
Bronvermelding: Wang, JH., Zheng, YQ., Qian, ZY. et al. Peritumoural adipose tissue drives immune evasion in colorectal cancer via adipose–mesenchymal transformation. Nat Cell Biol 28, 581–595 (2026). https://doi.org/10.1038/s41556-026-01885-0
Trefwoorden: colorectale kanker, tumormicro‑omgeving, visceraal vet, immunotherapie, CXCL12 CXCR4