Clear Sky Science · nl
Herverdeling van het ER is een kenmerk van veroudering en hangt af van ER‑fagie
Waarom de binnenplooien van de cel ertoe doen naarmate we ouder worden
De cellen in ons lichaam zijn gevuld met een doolhofachtig membraansysteem dat het endoplasmatisch reticulum (ER) genoemd wordt. Deze structuur helpt bij de aanmaak van vetten en eiwitten, regelt suiker en calcium en staat voortdurend in wisselwerking met andere celonderdelen. Omdat zoveel vitale functies via dit netwerk lopen, kan iedere langdurige hervorming van het ER invloed hebben op hoe weefsels verouderen, hoe veerkrachtig ze zijn tegen stress en uiteindelijk hoe lang we gezond blijven. Deze studie stelt een schijnbaar eenvoudige vraag: veroudert het ER zelf op een specifieke, georganiseerde manier, en zo ja, is die verandering schadelijke slijtage of een ingebouwde beschermingsstrategie?
Een verborgen verschuiving op het werkbankje van de cel
Met geavanceerde microscopen en fluorescerende markers in het kleine wormpje Caenorhabditis elegans volgden de onderzoekers het ER binnen levende dieren terwijl ze van jonge volwassenheid naar ouderdom gingen. In jeugdige cellen vormt het ER brede, gestapelde bladen bezaaid met eiwitproducerende machinerie, die lijken op keurig gerangschikte fabrieksvloeren. Naarmate de wormen ouder werden, krimptes die bladen in volume en maakten plaats voor een dunnere, meer buisachtige structuur die minder ruimte inneemt. Metingen toonden aan dat de totale ER‑inhoud sterk afneemt terwijl de vorm verandert, wat wijst op niet alleen willekeurige schade maar op een gecoördineerde inkrimping en herconfiguratie van het organel.
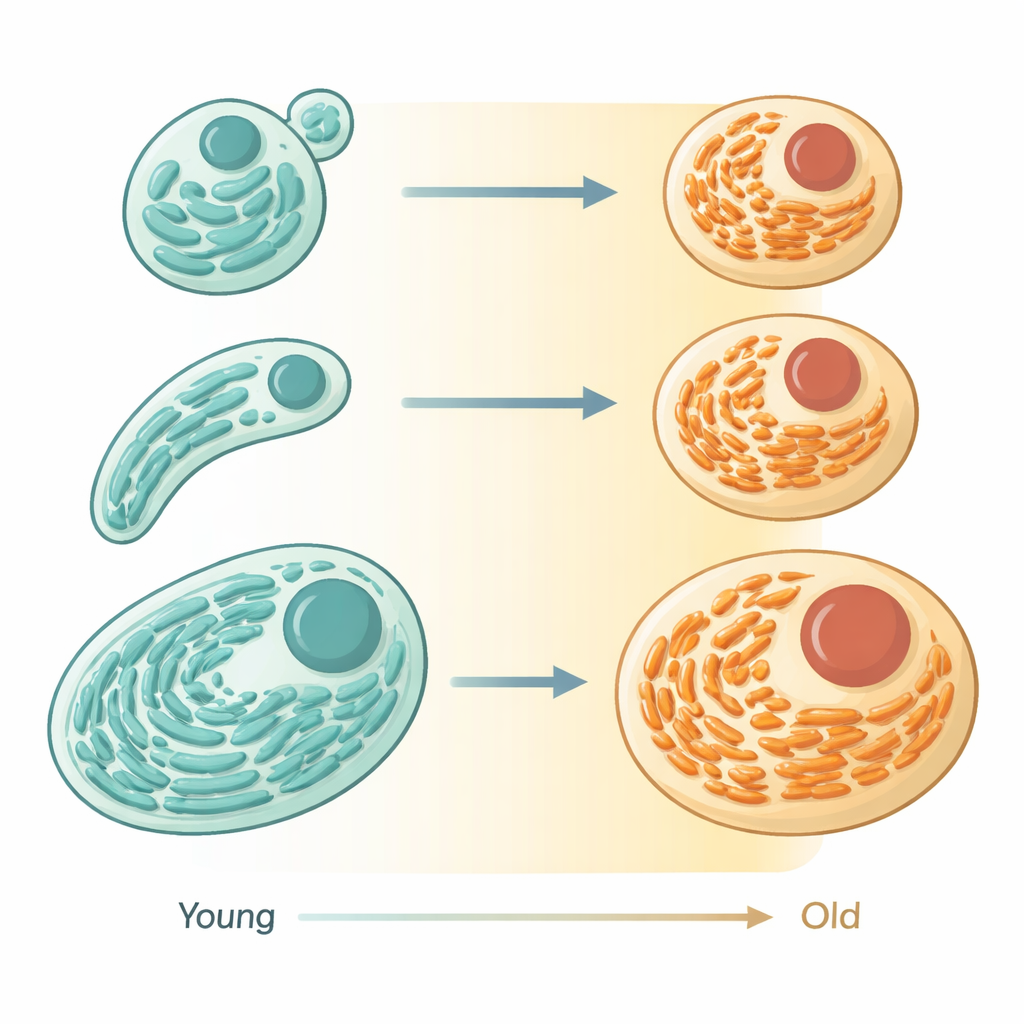
Van eiwitproductie naar vetverwerking
Vorm in de biologie duidt vaak op functie, en dat bleek hier eveneens het geval. De onderzoekers vergeleken hoe ER‑gerelateerde eiwitten in de tijd veranderen in verschillende weefsels van de worm. Eiwitten betrokken bij opbouw, vouwing en controle van andere eiwitten daalden met de leeftijd, in overeenstemming met het verlies van bladachtige ER. Daarentegen bleven veel ER‑eiwitten die gelinkt zijn aan vet‑ en membraanmetabolisme constant of namen zelfs toe. Gezamenlijk suggereren deze patronen dat verouderende cellen de grootschalige eiwitproductie terugschalen en de middelen van het ER heroriënteren naar beheer van vetten en membranen. Opmerkelijk genoeg zagen de auteurs in grote datasets van verouderende muizen een vergelijkbaar beeld: ER‑eiwitten voor secretie en eiwitverwerking neigden te dalen, terwijl die betrokken bij lipidenmetabolisme en autofagie relatief behouden bleven of toenamen.
Een cellulair recyclingpad achter de herstructurering
Wat drijft deze grootschalige herschikking? Het team traceerde de veranderingen naar ER‑fagie, een vorm van selectief zelfopeten waarbij de cel stukken ER verpakt in recyclende vesikels voor afbraak in lysosomen. Het blokkeren van kern‑autofagiegenen in wormen verhinderde het normale leeftijdsgebonden verlies van ER‑massa en de verschuiving van bladen naar buisjes, wat aantoont dat deze recyclingsroute niet slechts opruimt, maar actief het organel vormt. Onafhankelijke experimenten in gist bevestigden dat ER‑componenten tijdens veroudering naar het recyclagecentrum van de cel worden omgeleid, ook afhankelijk van autofagie. Elektronenmicroscopie toonde ER‑fragmenten binnen afbrekende compartimenten, fysiek bewijs dat stukken van het netwerk doelbewust worden verwijderd.

Weefsel‑specifieke controle van een gemeenschappelijk verouderingsprogramma
Hoewel ER‑herstructurering in veel wormweefsels werd waargenomen—darm, huidachtig hypodermis, spier en neuronen—bleken de triggers weefsel‑specifiek te zijn. In het hypodermis koppelde een eerder weinig bekend membraaneiwit, TMEM‑131, ER‑omloop aan collageenverwerking. Wanneer TMEM‑131 werd verlaagd, werd het leeftijdsgebonden verlies van ER in dit weefsel grotendeels voorkomen, wat impliceert dat het ER wordt verkleind wanneer zijn collageen “klanten” afnemen. In de darm was daarentegen de belangrijkste regulator de IRE‑1–XBP‑1‑arm van de ongevouwingseiwitrespons, een centraal stress‑detecterende route. Het uitschakelen van deze signaalarm bewaarde het intestinale ER tijdens veroudering, wat suggereert dat in dit orgaan ER‑stresssignalen helpen beslissen wanneer delen van het ER opgeofferd moeten worden.
Het ER herbedraden voor een langer leven
De studie verbindt ER‑herstructurering ook met levensduurverlenging. In wormen induceerden verschillende bekende levensverlengende interventies—het dempen van insulineachtige signalen, het verlagen van mTOR‑nutrientgrootheid, het verwijderen van de kiemlijn of het licht vertragen van eiwitsynthese—allemaal vroege in volwassenheid ER‑verkleining en toename van buisachtige netwerken, in plaats van te wachten tot de hoge leeftijd. Belangrijk is dat wanneer ER‑fagie werd uitgeschakeld, de normaal door mTOR‑remming veroorzaakte levensverlenging in zowel gist als wormen sterk verminderd of verloren ging. Dit duidt erop dat zorgvuldig beheerste ER‑snoei niet slechts een bijproduct is van veroudering of behandeling, maar een van de mechanismen waardoor cellen een duurzamer stadium bereiken.
Wat dit betekent voor gezond ouder worden
Voor een niet‑deskundige klinkt het verliezen van een aanzienlijk deel van een essentieel celstructuur tijdens veroudering mogelijk puur schadelijk. Dit werk schetst echter een genuanceerder beeld. Het ER lijkt actief te worden hervormd—via selectief zelfopeten en weefsel‑specifieke regulatoren—zodat verouderende cellen minder nieuwe eiwitten produceren, meer investeren in lipiden‑ en membraanbeheer en mogelijk het risico op chronische stress verminderen. Deze herstructurering blijkt geconserveerd van gist tot zoogdieren en is vereist voor ten minste sommige vormen van levensduurverlenging. Op de lange termijn kan het verkleinen van het ER echter gepaard gaan met afwegingen, die beïnvloeden hoe goed cellen andere organellen herstellen en omgaan met achteruitgang op latere leeftijd. Door ER‑fagie en ER‑dynamiek als kernaspecten van normale en vertraagde veroudering te onthullen, belicht dit onderzoek een nieuwe reeks aangrijpingspunten die mogelijk ooit bijgesteld kunnen worden om gezondere, veerkrachtigere weefsels te bevorderen.
Bronvermelding: Donahue, E.K.F., Hepowit, N.L., Ruark, E.M. et al. ER remodelling is a feature of ageing and depends on ER-phagy. Nat Cell Biol 28, 449–464 (2026). https://doi.org/10.1038/s41556-025-01860-1
Trefwoorden: endoplasmatisch reticulum, autofagie, cellulair verouderingsproces, eiwit‑homeostase, lipidenmetabolisme