Clear Sky Science · nl
Tijdsgedreven functionele genomica met deep learning onthult globale hiërarchische controle van autofagie
Hoe cellen zichzelf recyclen — en weten wanneer ze moeten stoppen
Onze cellen overleven magere tijden door hun eigen onderdelen te recyclen via een proces dat autofagie heet — letterlijk „zelf‑eten”. Te weinig recycling leidt tot ophoping van beschadigde componenten; te veel en de cel begint zichzelf te kannibaliseren. Deze studie stelt een schijnbaar eenvoudige vraag met grote implicaties voor veroudering en ziekte: hoe schakelt een levende cel autofagie precies aan en uit op de juiste momenten als de beschikbaarheid van nutriënten stijgt en daalt?
Duizenden cellen volgen tijdens een cyclus van overvloed naar schaarste
Om dit aan te pakken gebruikten de onderzoekers bakkersgist als model en volgden ze bijna zesduizend verschillende mutante stammen tijdens uithongering en herstel. Elke giststam droeg fluorescerende merkers die structuren die bij autofagie betrokken zijn markeerden, waardoor een krachtige microscoop elk uur beelden kon vastleggen terwijl de nutriënten werden verwijderd en vervolgens hersteld. In plaats van die beelden handmatig te classificeren, trainde het team deep‑learning‑algoritmen om te herkennen wanneer een cel zich in een autofagische toestand bevond, uitsluitend op basis van afbeeldingskenmerken en niet van menselijke interpretatie. Dit leverde nauwkeurige tijdseries van autofagie‑activiteit op voor bijna het hele gistgenoom, en toonde hoe snel en hoe sterk elke mutant op nutriëntveranderingen reageerde. 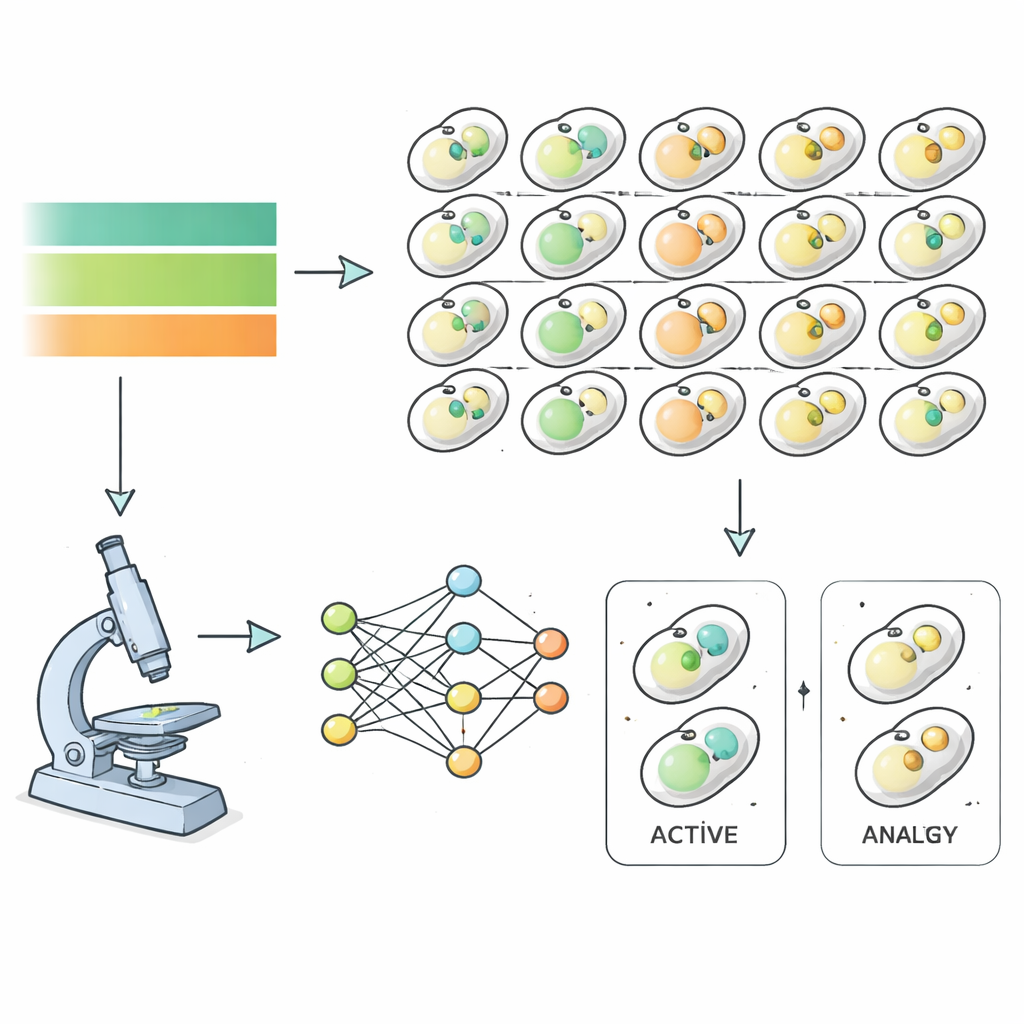
Zes verschillende manieren waarop cellen recycling slecht afhandelen
Door deze tijdseries wiskundig te modelleren, haalden de auteurs gedetailleerde „kinetische vingerafdrukken” uit elke mutant — hoe snel autofagie werd ingeschakeld, hoe lang het hoog bleef en hoe abrupt het weer afsloeg. Het groeperen van deze signaturen onthulde zes brede gedragstypen. Sommige mutanten waren „ultragevoelig” en reageerden zeer snel op uithongering en herbevoorrading. Andere waren „hypogevoelig” en reageerden traag. Een „hyperactieve” groep vertoonde abnormaal hoge basale recycling, terwijl meerdere groepen uiteenlopende gradaties van falen toonden om überhaupt een juiste respons op te bouwen. Belangrijk is dat bekende kerngenen voor autofagie in de ernstigste klassen vielen, wat bevestigt dat de methode echte biologische signalen oppikt en geen meetruis.
Een hiërarchie van controle over autofagie in kaart brengen
Autofagie vindt niet geïsoleerd plaats; het is ingebed in breder regelgevende netwerken van de cel. Het team legde hun dynamische profielen over grote kaarten van genetische en eiwitinteracties in gist. Genen waarvan het verlies sterke autofagiedefecten veroorzaakte, lagen vaak dicht bij de bekende „kernmachine” van autofagie in deze netwerken, terwijl subtielere mutanten verder weg zaten, wat wijst op meer indirecte controle. Door te onderzoeken welke cellulaire processen in elke gedragsklasse oververtegenwoordigd waren, vonden ze dat activatie door uithongering sterk wordt gevormd door paden die RNA, eiwitsynthese en energiemetabolisme regelen, terwijl het afsluiten van autofagie na terugkeer van nutriënten meer afhankelijk is van membranen verkeer en fusie‑stappen die recyclingvesikels opruimen.
Inzoomen op hoe vesikels zich vormen en worden verwijderd
Autofagie verloopt via twee hoofdstadia: het opbouwen van cargo‑gevulde vesikels en vervolgens het fuseren daarvan met het recyclingcompartiment van de cel voor afbraak. Om deze stadia te ontleden, onderzochten de onderzoekers de „latente ruimte” binnen hun neurale netwerk — de gecomprimeerde representatie die het gebruikt om beelden te onderscheiden. Door deze interne representatie op een tweedimensionale kaart te projecteren, konden ze zien hoe celpopulaties zich verplaatsen van een gebied zonder vesikels, via een gebied met veel vrije vesikels, naar een gebied waar vesikels waren geruimd. Met statistische vergelijkingen tegen referentiemutanten die vastzitten in verschillende stadia, kwantificeerden ze voor elk gen of het vooral de vesikelvorming, de vesikelruiming of beide beïnvloedde. Deze analyse liet zien dat de regeling van vesikelvorming over de tijd sterk gevoelig is voor stikstofniveaus, terwijl de ruimingsmachinerie constanter gedrag vertoont en vaak de belangrijkste beperkende factor is voor de totale recyclingflux. 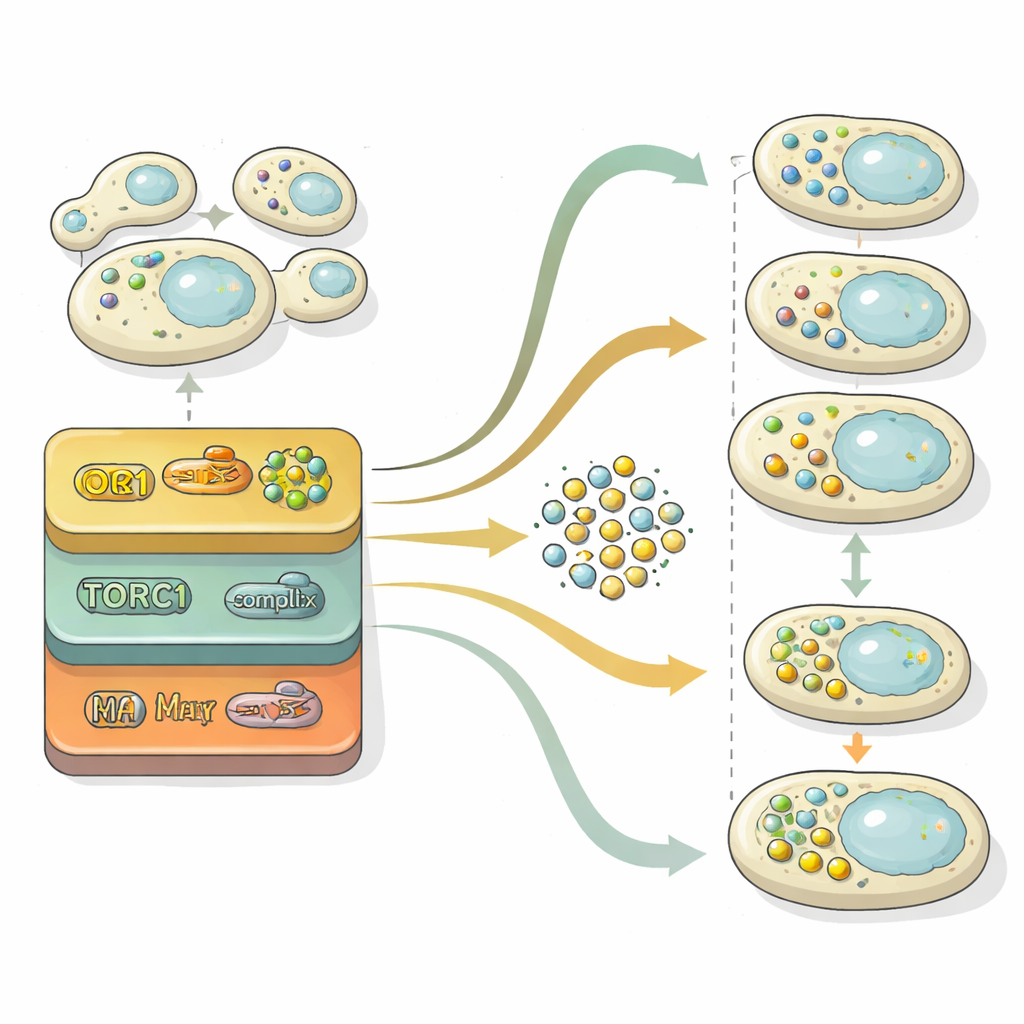
Een verborgen rem op recycling: de retrograde route
Een van de meest opvallende ontdekkingen betrof het zogenoemde retrograde (RTG) pad, dat signalen van mitochondriën naar de kern doorgeeft. Gistcellen zonder RTG‑componenten produceerden te veel autophagosomen, zelfs wanneer nutriënten ruim aanwezig waren, en hadden moeite deze te verwijderen zodra de nutriënten terugkeerden. Gedetailleerde vervolgexperimenten toonden aan dat dit pad de expressie van sleutelgenen voor autofagie regelt, met name de hoofdinitiator ATG1, grotendeels onafhankelijk van de bekende voedingssensor TORC1 die door geneesmiddelen zoals rapamycine wordt aangetast. In feite fungeert RTG‑signaalgeving als een tijdsafhankelijke rem die voorkomt dat autofagie ontspoort in rijke omstandigheden en helpt de respons te beëindigen wanneer de omstandigheden verbeteren.
Waarom dit belangrijk is voor gezondheid en therapie
Alles bij elkaar levert dit werk een genoom‑wijd, tijdsresoluut overzicht van hoe cellen autofagie afstemmen bij wisselende nutriëntcondities. Het toont aan dat activering en afsluiting geen spiegelbeelden zijn: veel meer genen beïnvloeden hoe recycling begint dan hoe het stopt, en de langetermijnbalans hangt sterk af van vesikelruiming en transcriptionele remmen zoals het RTG‑pad. Voor de algemene lezer is de kernboodschap dat cellulair zelf‑kannibalisme onder gelaagde, hiërarchische controle staat, en dat we deze lagen nu met hoge precisie in kaart kunnen brengen. Dit soort systeemniveau‑inzicht zou uiteindelijk kunnen leiden tot meer genuanceerde therapieën die autofagie in specifieke fasen bijsturen — het stimuleren van nuttige recycling zonder de schadelijke gevolgen van chronische, ongecontroleerde zelf‑afbraak te veroorzaken.
Bronvermelding: Chica, N., Andersen, A.N., Orellana-Muñoz, S. et al. Time-resolved functional genomics using deep learning reveals global hierarchical control of autophagy. Nat Cell Biol 28, 465–479 (2026). https://doi.org/10.1038/s41556-025-01837-0
Trefwoorden: autofagie, deep learning, gistgenetica, nutriëntdetectie, cellulair recyclen