Clear Sky Science · nl
Geraffineerde fenotypering van vaccinreacties onthult transcriptomische bepalers van heterogeniteit in neutraliserende antilichamen
Waarom sommige vaccins beter werken bij bepaalde mensen
Wanneer we ons laten prikken tegen COVID-19, gaan we er wellicht van uit dat ieders immuunsysteem hetzelfde reageert. In werkelijkheid verschillen mensen sterk in hoe snel en hoe krachtig ze beschermende antilichamen opbouwen. Deze studie volgde volwassenen die geïnactiveerde SARS-CoV-2-vaccins kregen en laat zien dat vaccinreacties in onderscheiden patronen vallen, elk aangedreven door verschillende vroege immuursignalen die in onze genen en bloedcellen zijn vastgelegd. Inzicht in deze patronen zou op een dag kunnen helpen vaccinatieschema’s af te stemmen zodat iedereen de bescherming krijgt die hij of zij nodig heeft.
Drie paden naar bescherming na dezelfde prik
De onderzoekers volgden 73 gezonde volwassenen die twee doses van een geïnactiveerd COVID-19-vaccin kregen. Ze maten neutraliserende antilichamen—deze die het virus kunnen blokkeren—voor de vaccinatie, een week na de tweede dosis en nogmaals ongeveer een maand later. In plaats van mensen simpelweg in “hoge” en “lage” responders te verdelen, gebruikten ze data-gedreven methoden om mensen te groeperen op basis van hoe hun antilichaamniveaus in de tijd veranderden. Drie duidelijke patronen kwamen naar voren: een “laag-vertraagd” groep met een trage, bescheiden toename van antilichamen; een “snel-stabiel” groep waarvan de antilichamen snel piekten en vervolgens stabiliseerden; en een “continu-toenemend” groep waarvan de antilichamen bleven stijgen naar de hoogste niveaus. Deze patronen werden niet verklaard door leeftijd, geslacht of lichaamsgewicht en slechts gedeeltelijk door welk merk geïnactiveerd vaccin mensen ontvingen.
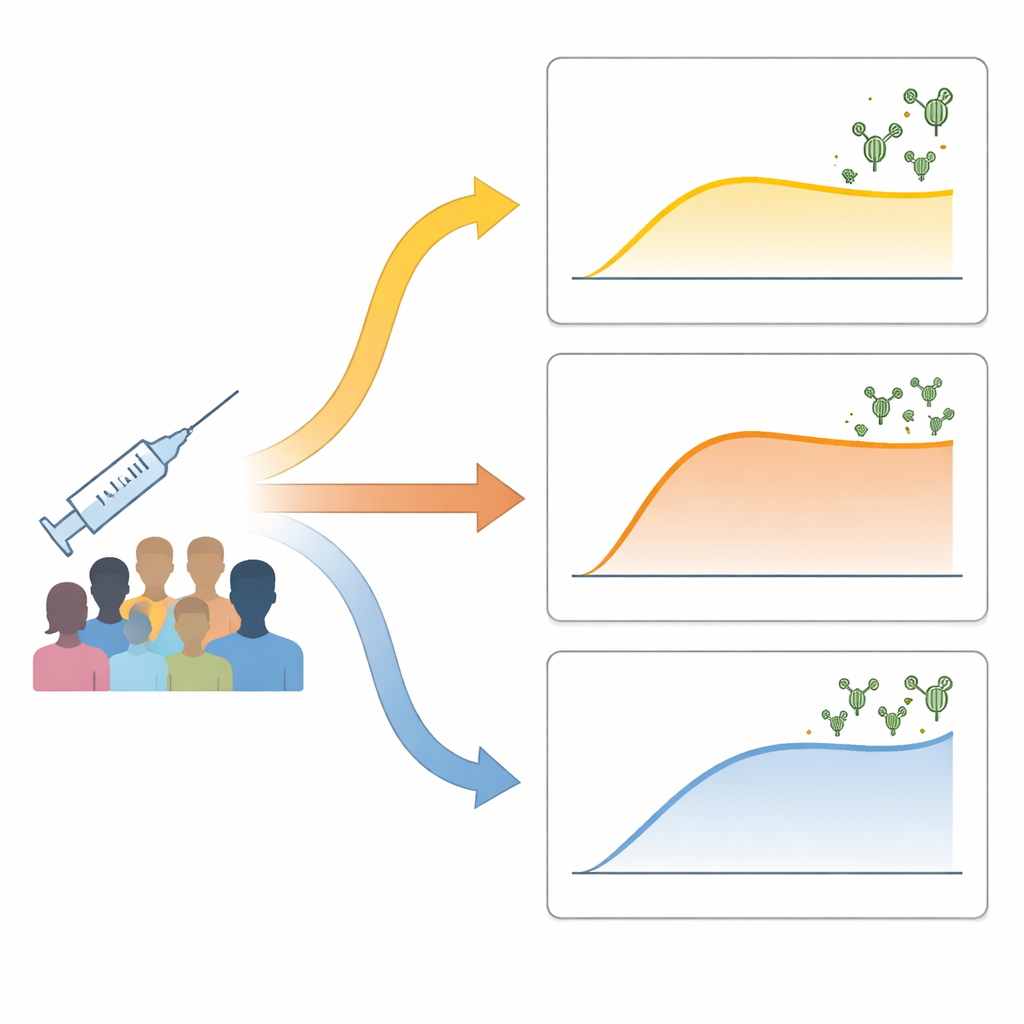
Hoe vroege immuunactiviteit de uitkomst vormgeeft
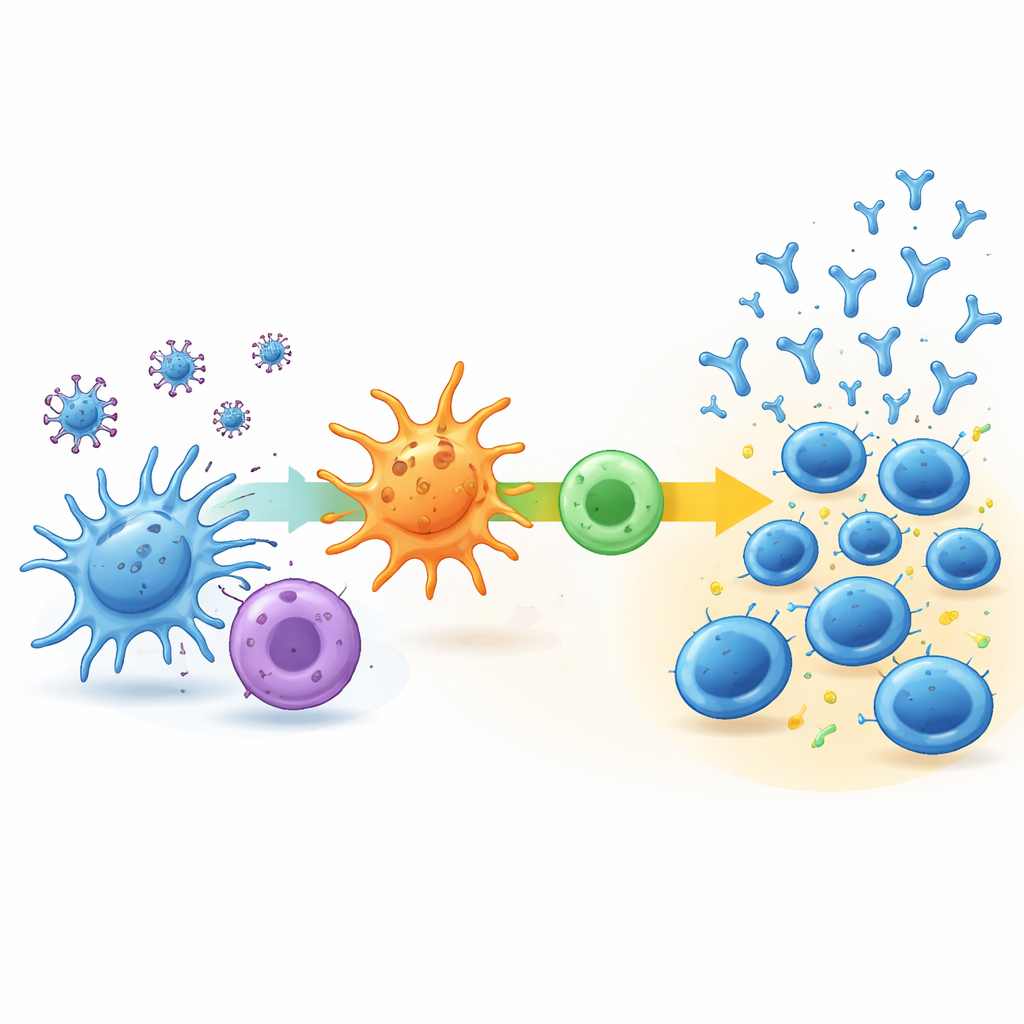
Om te begrijpen wat deze verschillende trajecten aandrijft, analyseerde het team de genetische activiteit van immuuncellen in het bloed bij aanvang en een week na de tweede prik. In de laag-vertraagde groep veranderde er weinig: belangrijke immuunroutes werden nauwelijks geactiveerd en de samenstelling van immuunceltypen in het bloed bleef grotendeels hetzelfde. Daarentegen toonden de snel-stabiele en continu-toenemende groepen duidelijke tekenen van vroege immuunactivatie. Bij de sterkste responders was er gecoördineerde activiteit in routes die virale fragmenten verwerken, deze presenteren aan andere immuuncellen en een type helper-T-celrespons ondersteunen dat bekendstaat om de antilichaamproductie te versterken. Deze mensen hadden ook vaak meer naïeve B-cellen en helper-T-cellen die paraat stonden om te reageren, en toonden later wat sterkere virus-specifieke T-celactiviteit.
Verborgen lagen van controle in RNA en B-cellen
Voorbij eenvoudige aan/uit-veranderingen van genen bekeken de wetenschappers subtielere lagen van regulatie die in RNA zijn ingebed, de tussengelegen moleculen tussen DNA en eiwit. In de top-responder groep vertoonden immuungenen die betrokken zijn bij het presenteren van virale fragmenten aan het immuunsysteem andere "splicing"-patronen en kortere staartregio’s aan het einde van hun RNA. Men denkt dat deze kenmerken het voor cellen makkelijker maken bepaalde eiwitten te produceren en sterke signaalvoering te behouden. Het team reconstrueerde ook het repertoire van B-celreceptoren—de unieke antennes op antilichaam-producerende cellen—uit dezelfde bloedmonsters. Hoewel de algemene diversiteit vergelijkbaar leek tussen de groepen, gebruikte elk responspatroon licht verschillende combinaties en vormen van deze receptoren, en de sterkste responders vertoonden een voorkeur voor receptortypes die eerder in verband zijn gebracht met krachtige antilichamen tegen het coronavirus spike-eiwit.
Laag-responders van tevoren opsporen
Aangezien mensen in de laag-vertraagde groep na een standaard vaccinatieschema mogelijk minder beschermd zijn, vroegen de onderzoekers of het mogelijk zou zijn hen vooraf te herkennen. Ze concentreerden zich op een kleine set genen die bij aanvang licht verschilden tussen de zwakste en sterkste responders. Met behulp van machine-learning bouwden ze een model op basis van de activiteit van slechts acht genen gemeten vóór vaccinatie. Dit model kon laag-vertraagde responders in hun dataset met hoge nauwkeurigheid onderscheiden, waarbij twee genen die betrokken zijn bij basale cel‑signalering en ontsteking het grootste deel van het voorspellende vermogen leverden. Hoewel dit werk nog getest moet worden in grotere en meer diverse groepen, suggereert het dat een eenvoudige bloedtest op een dag meer gepersonaliseerde vaccinplannen zou kunnen aansturen.
Wat dit betekent voor toekomstige vaccins
In het algemeen laat deze studie zien dat mensen niet simpelweg een "sterke" of "zwakke" antilichaamrespons hebben; ze volgen verschillende tijdsverlopen die worden gevormd door vroege, moeilijk waarneembare immuunprocessen. De best beschermde individuen schakelen gecoördineerde netwerken van genen en cellen in die hen helpen het vaccin snel te herkennen en duurzame antilichamen op te bouwen, terwijl lage responders een verzwakte vroege reactie tonen. Door deze interne verschillen in kaart te brengen en instrumenten te ontwikkelen om te voorspellen wie mogelijk slecht reageert, legt dit werk de basis voor gepersonaliseerde vaccinatie—zoals eerdere boosterdoses of alternatieve formuleringen voor risicogroepen—zodat de belofte van vaccins gelijkmatiger gedeeld kan worden.
Bronvermelding: Wu, Q., Hu, H., Qin, L. et al. Refined phenotyping of vaccine responses reveals transcriptomic determinants of neutralizing antibody heterogeneity. npj Vaccines 11, 61 (2026). https://doi.org/10.1038/s41541-026-01386-z
Trefwoorden: vaccinreacties, neutraliserende antilichamen, COVID-19 vaccinatie, immunologische heterogeniteit, gepersonaliseerde vaccins