Clear Sky Science · nl
Immunogeniciteit en bescherming van octavalente influenza-vaccinkandidaten met geadjuvante eiwitten of mRNA-LNPs in naïeve muizen
Waarom een beter griepvaccin ertoe doet
Seizoensgebonden griepvaccins redden veel levens, maar hun bescherming kan van jaar tot jaar sterk variëren. Een reden is dat huidige prikken het immuunsysteem vooral trainen om één viraal eiwit te herkennen, waardoor andere nuttige doelwitten onderbenut blijven. Deze muizenstudie onderzoekt volgende-generatie griepvaccins die het immuunsysteem leren twee belangrijke virale eiwitten tegelijk te herkennen en vergelijkt een traditionele op eiwitten gebaseerde aanpak met een nieuwere mRNA-technologie, vergelijkbaar met die in recente COVID-19-vaccins.
Twee doelwitten in plaats van één
De huidige griepprikken richten zich vooral op hemagglutinine, of HA, een eiwit dat het virus helpt aan onze cellen te hechten. De onderzoekers voegden een tweede viraal eiwit toe, neuraminidase, of NA, dat het virus helpt ontsnappen uit geïnfecteerde cellen en zich te verspreiden. Door vier varianten van HA en vier varianten van NA uit de seizoensstammen van 2018–2019 te combineren, bouwden ze een "octavalent" vaccin bedoeld om twee types influenza A en twee lijnen van influenza B te dekken. Deze acht componenten verpakte men vervolgens op twee verschillende manieren: als gezuiverde eiwitten gemengd met een immuunversterkend ingrediënt, en als mRNA ingekapseld in kleine lipidebelletjes (mRNA-LNPs) die de eigen cellen van het lichaam aanzetten de virale eiwitten te produceren.
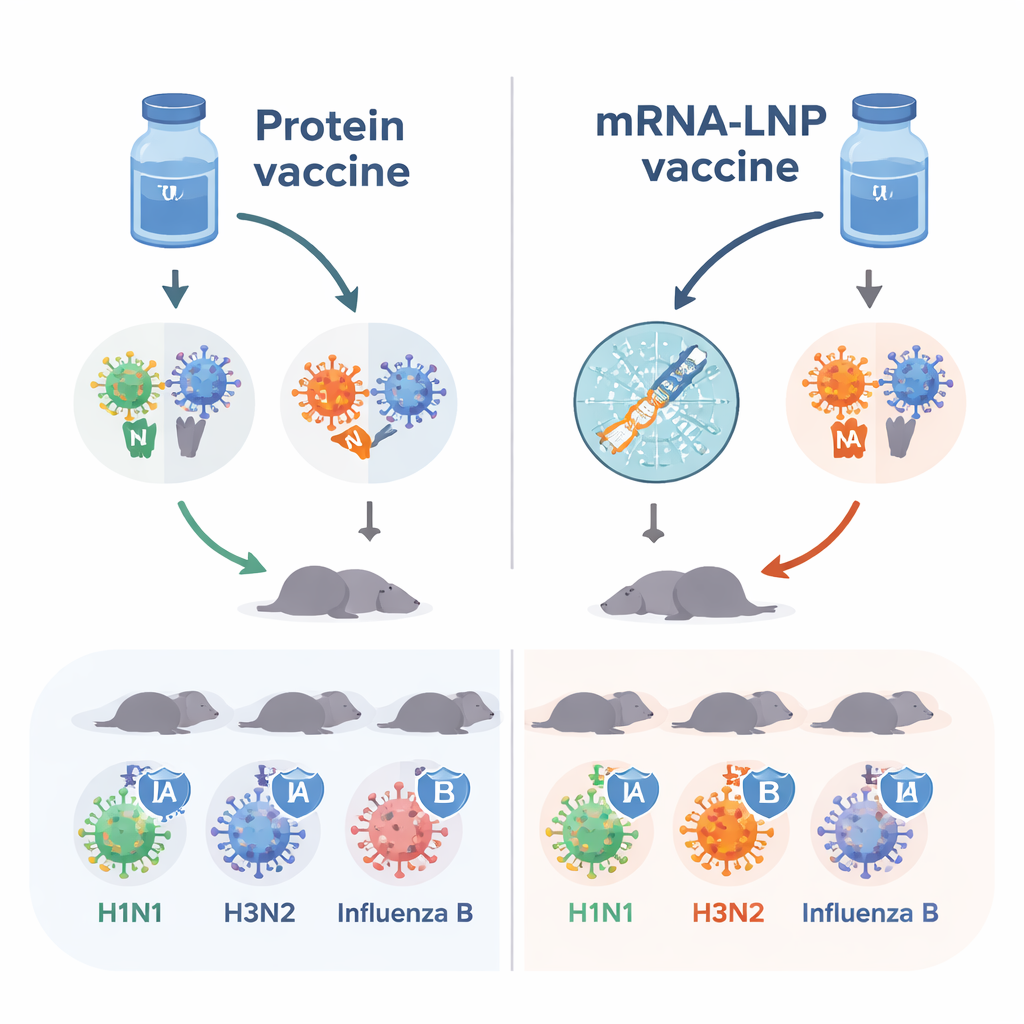
Sterkere antilichaamreacties met mRNA
Naïeve muizen—dieren die nog nooit door influenzavirussen of vaccins waren blootgesteld—kregen twee doses van ofwel het eiwitvaccin of de mRNA-LNP-versie. Het team mat antilichamen die HA en NA in het bloed herkennen. Beide vaccins veroorzaakten zinvolle reacties, maar de mRNA-LNP-injecties produceerden consequent hogere niveaus antilichamen tegen de meeste HA- en NA-componenten. Vooral antilichamen die de activiteit van NA blokkeren, waarvan bekend is dat ze onafhankelijk bijdragen aan bescherming, waren over het algemeen sterker na mRNA-LNP-vaccinatie. Deze bevindingen suggereren dat, althans in dit diermodel, het mRNA-platform dezelfde virale doelwitten beter zichtbaar maakt voor het immuunsysteem.
Bescherming tegen overeenkomende en actuele stammen
De echte test was of deze vaccins muizen konden behoeden voor ernstige ziekte. Bij doses geschaald om vergelijkbaar te zijn met een menselijke griepprik, beschermden beide vaccinformats de dieren volledig tegen dodelijke infectie met H1N1- en influenza B-virussen die nauw overeenkwamen met de vaccinkomponenten, evenals tegen geconstrueerde H3N2-achtige virussen die werden gebruikt wanneer standaard menselijke stammen muizen niet ziek maken. Gevaccineerde muizen behielden hun lichaamsgewicht en overleefden, terwijl niet-gevaccineerde dieren gewicht verloren en vaak overleden. Voor deze nauwe stammen presteerden de traditionele eiwitvaccins en de mRNA-LNP-vaccins vergelijkbaar wat overleving betreft, ook al verschilden de details van de antilichaamreacties.
Voordeel tegen oudere, niet-overeenkomende griepvirussen
Waar de mRNA-LNP-aanpak uitsprong, was in zwaardere "mismatch"-testen. De onderzoekers daagden gevaccineerde muizen uit met historische H3N2-stammen uit 1968, 1975 en 1982—virussen die verschillen van moderne stammen die het vaccin nabootst. Alle niet-gevaccineerde muizen en de meeste dieren die eiwitvaccins kregen, stierven, maar iedere muis die het octavalente mRNA-LNP-vaccin had ontvangen overleefde, hoewel ze nog steeds ziekteverschijnselen toonden. Dit overlevingsvoordeel bleef bijna een jaar na vaccinatie bestaan, wat wijst op langdurige bescherming. Toen het team serum van gevaccineerde dieren overdroeg naar niet-gevaccineerde muizen, beschermde alleen serum met antilichamen opgewekt door mRNA-LNP-vaccins tegen HA tegen de dood door een niet-overeenkomend virus, wat wijst op kruisreactieve HA-antilichamen als een belangrijke factor.
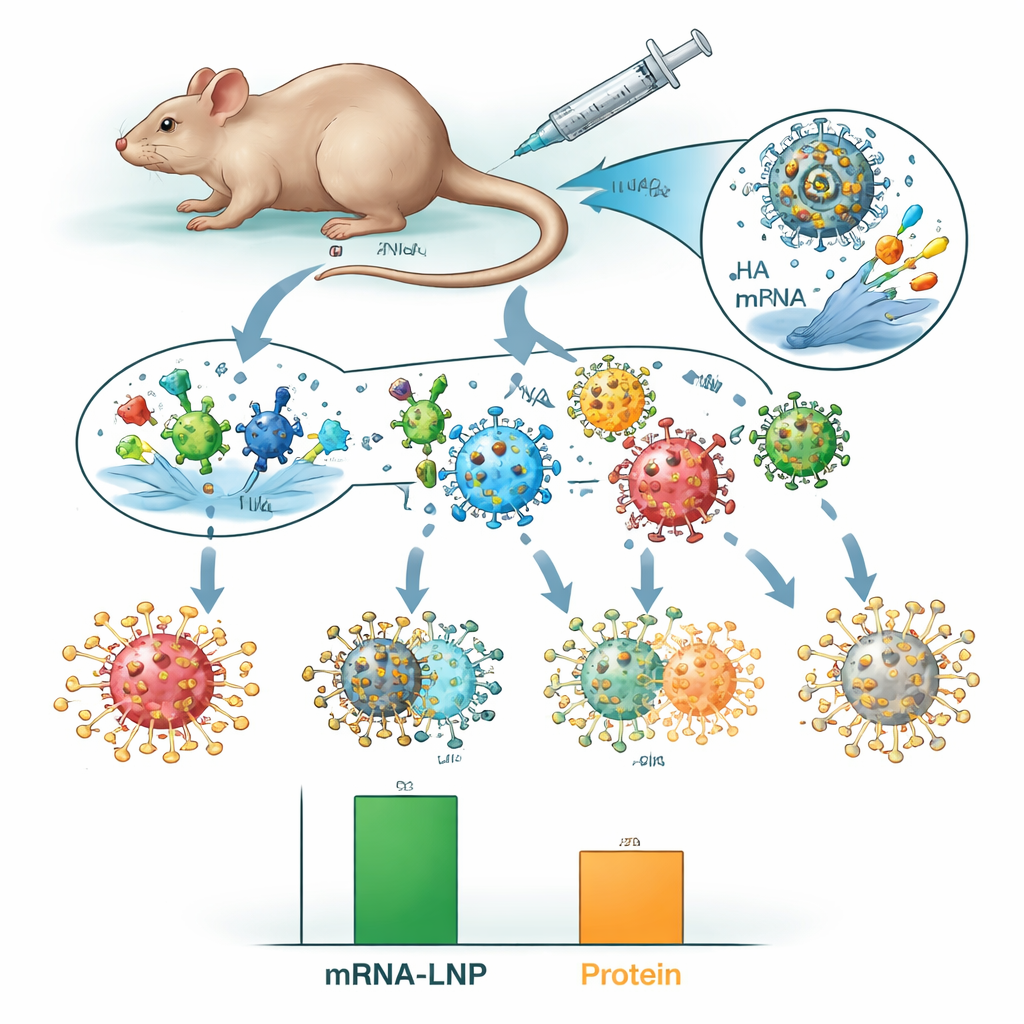
Wat dit betekent voor toekomstige griepprikken
Voor niet-specialisten komt de boodschap erop neer dat beide vaccinstijlen muizen beschermden tegen de griepstammen waarvoor ze waren ontworpen, maar dat de mRNA-LNP-versie ook bredere en langduriger bescherming bood tegen oudere, verouderde virussen. Door beide belangrijkste oppervlakeiwitten van het griepvirus op te nemen en mRNA te gebruiken om ze aan het immuunsysteem te presenteren, kan deze strategie helpen de kloof te verkleinen tussen goede en slechte griepseizoenen. Hoewel muisresultaten geen garantie zijn voor succes bij mensen, en sterkere adjuvantia eiwitvaccins mogelijk nog kunnen verbeteren, ondersteunt dit werk het idee dat multicomponent mRNA-griepvaccins op termijn meer betrouwbare bescherming kunnen bieden tegen een bredere reeks circuleerende en opkomende influenzastammen.
Bronvermelding: Catani, J.P.P., Smet, A., Ysenbaert, T. et al. Immunogenicity and protection of octavalent influenza vaccine candidates using adjuvanted proteins or mRNA-LNPs in naïve mice. npj Vaccines 11, 57 (2026). https://doi.org/10.1038/s41541-026-01378-z
Trefwoorden: griepvaccin, mRNA-LNP, hemagglutinine, neuraminidase, kruisbescherming