Clear Sky Science · nl
Antigeen‑crosspresentatie versterkend adjuvans voor kankervaccins ter uitbreiding van T‑cellen en synergie met anti‑PD‑1
Het immuunsysteem omvormen tot een precieze tumorkrijger
Kankervaccins worden vaak beschreven als een manier om het immuunsysteem te leren tumoren te herkennen en te vernietigen, maar in de praktijk hebben ze zelden die belofte waargemaakt. Deze studie onderzoekt een nieuwe methode om zulke vaccins te “superchargen”, zodat ze sterker en langduriger cytotoxische T‑cellen kunnen opwekken en beter samenwerken met gangbare immunotherapieën zoals anti‑PD‑1. Voor lezers die geïnteresseerd zijn in hoe toekomstige kankerbehandelingen biologische geneesmiddelen, vaccins en immuunengineering kunnen combineren, biedt dit werk een inkijkje in hoe next‑generation, zeer gerichte immunotherapie eruit zou kunnen zien.
Waarom kankervaccins betere ondersteuning nodig hebben
Therapeutische kankervaccins zijn niet bedoeld om ziekte te voorkomen, maar om mensen met bestaande tumoren te behandelen door krachtige, tumorschrijnende immuunresponsen op te wekken. De sleutelspelers zijn CD8‑“killer” T‑cellen, die kankercellen kunnen herkennen en vernietigen die karakteristieke antigenen tonen. Helaas geven tumorantigenen vaak zwakke stimulatie omdat ze grotendeels lijken op licht gewijzigde versies van eigen lichaamsproteïnen. Aanhoudende blootstelling tijdens tumorontwikkeling kan T‑cellen uitgeput of tolerant maken, waardoor vaccins minder effectief zijn. Om dit te overwinnen moeten vaccins gepaard gaan met adjuvanten—hulpcomponenten die het aangeboren immuunsysteem activeren, antigenpresentatie verbeteren en een grote, veerkrachtige populatie tumorspecifieke T‑cellen opbouwen.
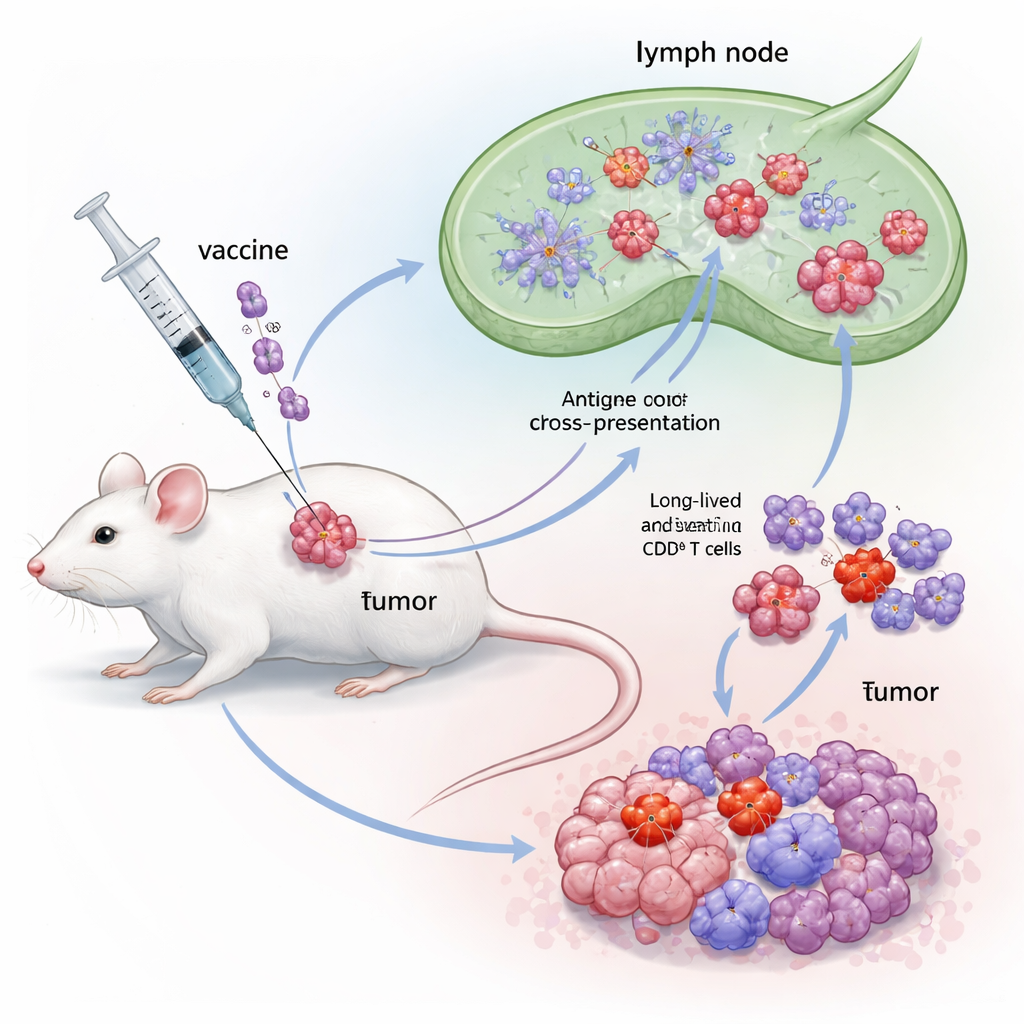
Een hybride immuunversterker opgebouwd uit twee krachtige signalen
De onderzoekers ontwierpen een hybride adjuvans genaamd Flt3L‑FlaB, of FB, door twee immuunstimulerende moleculen tot één eiwit te fuseren. De ene helft, Flt3L, is een natuurlijk groeifactor die een gespecialiseerde groep dendritische cellen, bekend als cDC1, doet uitbreiden. Deze cellen zijn bedreven in “cross‑presentatie” – ze verwerken tumorfragmenten en presenteren die aan CD8‑T‑cellen op een manier die sterke responsen opwekt. De andere helft, FlaB, is een bacterieel flagellinefragment dat de aangeboren sensor TLR5 activeert en fungeert als een krachtig gevaarsignaal. Door ze te koppelen wilden de auteurs zowel cDC1 uitbreiden als ze in een hoogactieve staat brengen, waardoor tumorantigenen effectiever aan T‑cellen worden getoond en de stimulatie langer aanhoudt.
De nieuwe adjuvans testen in tumormodellen
Om FB te testen gebruikte het team een goed vastgesteld muizentumormodel gebaseerd op cellen die geavanceerd waren om kankerverwekkende eiwitten van het humaan papillomavirus (HPV) te dragen. Muizen kregen eerst een kleine tumorimplantatie en vervolgens een therapeutisch vaccin met een HPV E7‑antigeen, gecombineerd met ofwel alleen Flt3L, alleen FlaB, of de nieuwe FB‑fuse. Alle vaccins werden nabij de tumor toegediend. Hoewel elk individueel adjuvans de tumorgroei enigszins vertraagde, stak het FB‑gebaseerde vaccin met kop en schouders boven de rest uit: het vertraagde tumorgroei veel meer, verlengde de overleving significant en liet een opvallend aandeel muizen volledig tumorvrij achter. Immunologische analyses toonden dat FB‑vaccinatie uitzonderlijk sterke E7‑specifieke CD8‑responsen opwekte in bloed, lymfeklieren en milt, met hoge niveaus interferon‑gamma en robuuste T‑celproliferatie—bewijs dat de fusie meer deed dan alleen de effecten van de afzonderlijke componenten optellen.
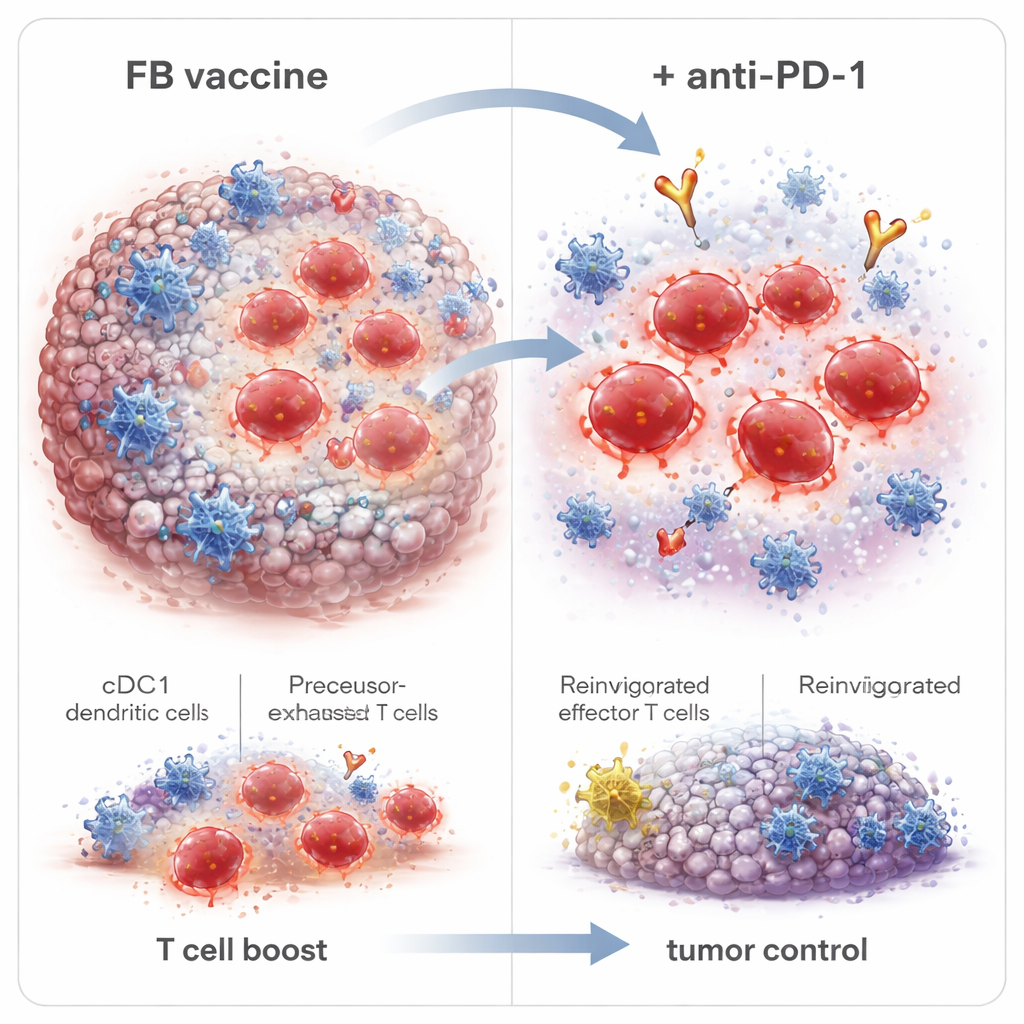
Duurend immuungeheugen opbouwen en een betere partner voor anti‑PD‑1
Dieper gravend vonden de wetenschappers dat FB niet alleen het aantal CD8‑T‑cellen veranderde, maar ook het type. Het versterkte kortlevende effectorcellen die tumoren direct aanvallen, evenals geheugen‑precursoren en stam‑achtige geheugencellen die kunnen aanhouden en later opnieuw reageren. Belangrijk is dat FB ook een groep binnen tumoren uitbreidde die precursor‑uitgeputte T‑cellen (Tpex) worden genoemd—cellen die zich op de grens bevinden tussen uitputting en volledige activiteit en bijzonder responsief zijn voor anti‑PD‑1‑middelen. Wanneer tumorvrije overlevers lange tijd na vaccinatie werden blootgesteld aan hogere doses kankercellen, weerstond de meeste hergroei, wat duidt op duurzaam immuungeheugen. Blokkering van het vertrek van immuuncellen uit lymfeklieren wist de voordelen van FB uit, wat aangeeft dat tumor‑dodelijke T‑cellen in die knopen door cDC1 werden geprimed en daarna in de tumor migreerden.
Sterker samen: vaccins plus checkpointblokkeerders
Aangezien anti‑PD‑1‑therapie het beste werkt wanneer er al een reservoir van responsieve T‑cellen aanwezig is, combineerde het team FB‑geadjuveerde vaccinatie met een anti‑PD‑1‑antilichaam. In het HPV‑tumormodel vertraagde het toevoegen van anti‑PD‑1 bovenop FB‑vaccinatie de tumorgroei verder, verhoogde het aantal muizen dat hun kanker volledig uitrolde, en bood het volledige bescherming tegen een extreem hoge dosis tumor‑heruitdaging. Fijnafstelling van de timing was van belang: het starten van anti‑PD‑1 na de tweede in plaats van de eerste vaccinatieverbeterde de complete tumoruitroei licht, consistent met wachten tot Tpex‑cellen waren uitgebreid. Het FB‑adjuvans verbeterde ook de respons op peptidegebaseerde vaccins, inclusief tumorspecifieke neoantigenen in een colonkankermodel, wat suggereert dat deze strategie breder toepasbaar kan zijn dan alleen HPV‑gerelateerde aandoeningen.
Wat dit kan betekenen voor toekomstige kankerzorg
Voor niet‑specialisten is de kernboodschap dat dit werk verfijnt hoe het immuunsysteem “geïnstrueerd” wordt om kanker te bestrijden. Door een dendritische‑cel‑groeifactor te combineren met een sterk gevaarsignaal in één stabiel eiwit, creëert het FB‑adjuvans meer van de juiste antigen‑presenterende cellen, helpt het hen tumorantigenen effectiever tonen en vormt het een populatie killer‑T‑cellen die zowel nu krachtig zijn als klaarstaan om later op checkpointtherapie te reageren. Hoewel deze resultaten in muizen zijn en nog veel stappen nodig zijn voordat toepassing bij mensen mogelijk is, schetst de studie een helder stappenplan: slimmer ontworpen adjuvanten die cross‑presentatie en T‑cel‑stam‑eigenschappen orkestreren, kunnen therapeutische kankervaccins veel betere partners maken voor middelen zoals anti‑PD‑1, wat mogelijk leidt tot diepere en langduriger tumorcontrole bij patiënten.
Bronvermelding: Dang, G.C., Loeurng, V., Pa, P. et al. Antigen cross-presentation potentiating cancer vaccine adjuvant for T cell expansion and synergy with anti-PD-1. npj Vaccines 11, 56 (2026). https://doi.org/10.1038/s41541-026-01376-1
Trefwoorden: kankervaccins, immunotherapie, dendritische cellen, PD‑1 blokkade, HPV‑gerelateerde tumoren