Clear Sky Science · nl
Universeel breedspectrum mucosaal vaccinontwerp voor humane coronavirussen geïnspireerd door kunstmatige antilichamen
Waarom een beter coronavaccin nog steeds van belang is
Zelfs nu COVID-19 richting een seizoensgebonden infectie verschuift, verschijnen er voortdurend nieuwe varianten en veroorzaken meerdere andere humane coronavirussen nog steeds ernstige ziekte. Huidige vaccins doen het goed in het voorkomen van zware ziekte, maar zijn minder effectief in het blokkeren van infectie en transmissie, vooral in de neus en keel waar deze virussen eerst voet aan de grond zetten. Deze studie beschrijft een nieuw soort intranasaal vaccin, geïnspireerd door ontworpen antilichamen, dat bedoeld is langdurige, brede bescherming te bieden tegen veel coronavirussen aan de mucosale frontlinie van het lichaam.
Een slimmer vaccin-scaffold bouwen
De onderzoekers begonnen met een bekend molecuul: humaan IgG1, het belangrijkste antilichaamtype dat in veel goedgekeurde antilichaammedicijnen wordt gebruikt. Ze herontwierpen de zware keten zodat deze kon fungeren als een flexibel “scaffold” voor het presenteren van receptor-bindende domeinen (RBD’s) van het coronavirus-spike-eiwit — de delen die het virus gebruikt om onze cellen vast te pakken. Door de gebruikelijke lichte keten te verwijderen en specifieke mutaties toe te voegen, verminderden ze de binding aan immuunreceptoren die aan bijwerkingen zoals cytokinestormen kunnen bijdragen, terwijl ze de binding aan de neonatale Fc-receptor (FcRn) versterkten. FcRn is overvloedig aanwezig op mucosale oppervlakken en helpt antilichamen over de barrière te vervoeren en langer in het weefsel te behouden. Op deze geoptimaliseerde ruggengraat plaatste het team één, twee, drie of vier verschillende RBD’s van SARS, MERS, seizoensgebonden coronavirussen en meerdere SARS‑CoV‑2-varianten, inclusief Omicron-lijnen, waarmee mono-, bi-, tri- en tetravalente kandidaatvaccins werden gecreëerd.
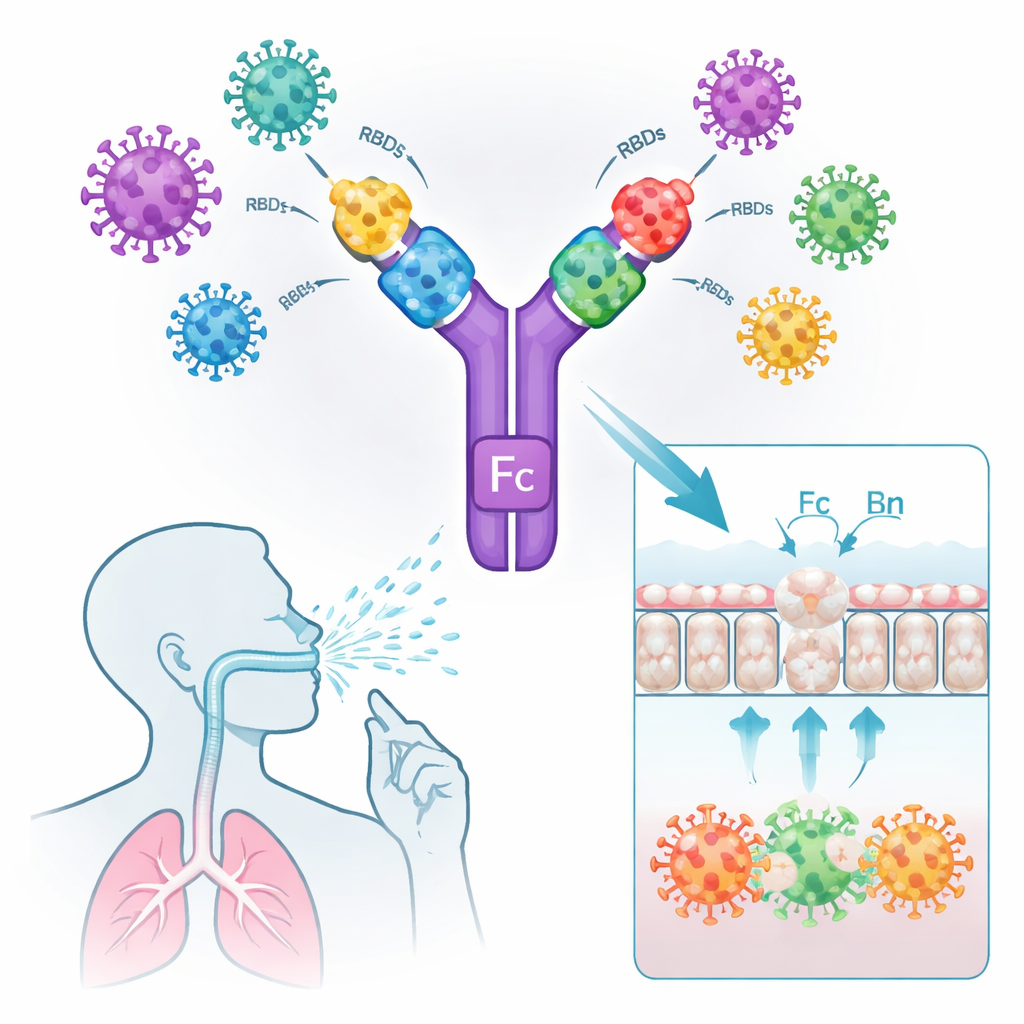
De mucosale barrière passeren en lokale afweer activeren
Om als neusspray te werken, moeten de vaccing antigenen de luchtwegbekleding bereiken, daar blijven hangen en efficiënt door immuuncellen worden opgemerkt. In kweekcelsystemen bonden de Fc-bevattende constructen sterk zowel aan ACE2 (de SARS‑CoV‑2-ingangsreceptor) als aan menselijke of muizen-FcRn, en werden ze actief over een laag mucosale cellen heen getransporteerd. Een vergelijkbare RBD-dimeer zonder het Fc-gedeelte slaagde er niet in de barrière te passeren. Wanneer gefluoresceerde versies van de vaccins in de neuzen van muizen werden toegediend, bleven de Fc-bevattende antigenen urenlang in het longmucosa aanwezig, terwijl de kale RBD-dimeer snel verdween. Microscopie toonde dat de Fc-gemodificeerde vaccins antigeen-presenterende cellen net onder het mucosale oppervlak aantrokken en activeerden, zoals aangegeven door hogere niveaus van de immuunmarker CD80 en colocalisatie met FcRn.
Antistoffen en T-cellen versterken waar ze nodig zijn
Het team vergeleek vervolgens immuunresponsen na intramusculaire injectie versus intranasale toediening bij muizen. Over meerdere formuleringen veroorzaakten de Fc-gebaseerde vaccins zeer hoge niveaus van IgG-antilichamen in het bloed tegen zowel de oorspronkelijke SARS‑CoV‑2-stam als Omicron XBB.1.5. Intranasale toediening, vooral in combinatie met een moderne STING-agonist adjuvans (CF501), viel op doordat het sterke IgA-responsen opwekte, niet alleen in het bloed maar ook in neussecreties en longspoelingen — precies daar waar mucosale bescherming het belangrijkst is. De Fc-bevattende constructen veroorzaakten ook krachtiger cellulaire reacties dan kale RBD-dimeren, met uitbreiding van helper-T-cellen, cytotoxische T-cellen en langlevende weefselresident geheugen-T-cellen in de longen. Van deze celtypen wordt gedacht dat ze cruciaal zijn voor het opruimen van luchtweginfecties en het voorkomen van verspreiding naar gevoelige organen zoals de hersenen.
Brede bescherming tegen veel varianten en soorten
Een centrale test was of een bivalent vaccin dat RBD’s van het prototypevirus en Omicron XBB.1.5 combineerde (genoemd XBB.1.5 + PT‑Fc) dieren tegen meerdere virusuitdagingen kon beschermen. In muizen die menselijk ACE2 tot expressie brachten en twee lage intranasale doses kregen, induceerde deze kandidaat sterke neutraliserende antilichamen en beschermde dieren volledig tegen dodelijke infectie met zowel het oorspronkelijke virus als XBB.1.16: gevaccineerde muizen behielden hun gewicht, overleefden en hadden geen detecteerbaar virus in hersenen, longen of neusslijmvlies, terwijl controle-dieren ziek werden en stierven. Hetzelfde vaccin verhinderde ziekte en overlijden wanneer muizen werden uitgedaagd met andere belangrijke varianten, waaronder Beta, Delta en meerdere Omicron-sublineages. Bij hamsters, die goed geschikt zijn voor transmissiestudies, hadden gevaccineerde dieren dramatisch lagere virusbelastingen na directe uitdaging en waren ze in co-housingexperimenten grotendeels beschermd tegen luchtweginfectie via overdracht. Antistofniveaus en geheugen-T-cellen in zowel muizen als hamsters bleven hoog gedurende ten minste 48 weken, en dieren waren nog steeds volledig beschermd tegen dodelijke uitdagingen bijna een jaar na vaccinatie.
Op weg naar een universele coronavaccin-neusspray
Ten slotte brachten de onderzoekers het platform in de richting van een werkelijk universeel ontwerp. Ze mengden meerdere bivalente constructen die SARS‑CoV‑2, SARS, MERS en verschillende seizoensgebonden coronavirussen besloegen, en bouwden ook tetravalente moleculen die vier verschillende RBD’s of spike-fragmenten op één scaffold droegen. Deze combinaties wekten antilichamen op die een breed panel van humane coronavirussen herkenden en verminderden in muizenchallenge-experimenten de virusbelastingen voor meerdere vertegenwoordigers, waaronder een endemisch virus (NL63). Hoewel verder testen in modellen die dichter bij de mens staan en uiteindelijk klinische proeven nodig is, toont het werk aan dat een ontworpen antilichaam-ruggengraat op veilige wijze diverse coronavirusantigenen over de neusbarrière kan vervoeren, sterke lokale en systemische immuniteit kan stimuleren en brede, duurzame bescherming kan bieden. Voor niet‑specialisten is de boodschap dat toekomstige “universele” coronavirusbooster(s) mogelijk geen injecties zijn, maar milde neussprays gebouwd op dezelfde antilichaamramen die al veilig zijn gebleken in veel geneesmiddelen.
Bronvermelding: Wu, Y., Lu, J., Fang, L. et al. Universal broad-spectrum mucosal vaccine design for human coronaviruses inspired by artificial antibodies. npj Vaccines 11, 55 (2026). https://doi.org/10.1038/s41541-026-01375-2
Trefwoorden: intranasal vaccin, breedspectrum coronavirus, mucosale immuniteit, kunstmatig antilichaam-scaffold, SARS-CoV-2-varianten