Clear Sky Science · nl
Het overwinnen van door het vasculaire micro‑milieu veroorzaakte TKI‑resistentie bij acute myeloïde leukemie door remming van miR‑126
Waarom dit belangrijk is voor kankerpatiënten
Acute myeloïde leukemie (AML) behoort tot de meest agressieve bloedkankers, en zelfs met moderne gerichte middelen krijgen veel patiënten een terugval. Deze studie stelt een schijnbaar eenvoudige vraag met grote implicaties: is het probleem niet alleen de kankercel zelf, maar ook de "buurt" waarin ze leeft in het beenmerg? Met een gedetailleerd computermodel dat is gebaseerd op laboratoriumgegevens, onderzoeken de auteurs hoe kleine bloedvaten leukemiestamcellen kunnen afschermen tegen geneesmiddelen — en hoe het blokkeren van één klein RNA‑signaal die bescherming kan ontmantelen.
Het verborgen veilige onderkomen in het beenmerg
AML ontstaat in het beenmerg, waar kwaadaardige blasten de normale bloedvorming verdringen. Binnen deze massa schuilt een kleinere populatie leukemiestamcellen die zichzelf kunnen vernieuwen en behandeling kunnen overleven, en zo een terugval kunnen inleiden. Deze stamcellen drijven niet vrij rond; ze nestelen zich in gespecialiseerde pocketen rond kleine arteriën en capillairen, gezamenlijk het vasculaire niche genoemd. De studie richt zich op patiënten wiens leukemiecellen FLT3‑ITD‑mutaties dragen, die behandeld worden met tyrosinekinaseremmers (TKI’s). Hoewel deze middelen de tumorlast sterk kunnen verminderen, krijgen veel patiënten toch een terugval, wat suggereert dat sommige cellen verborgen of beschermd worden.
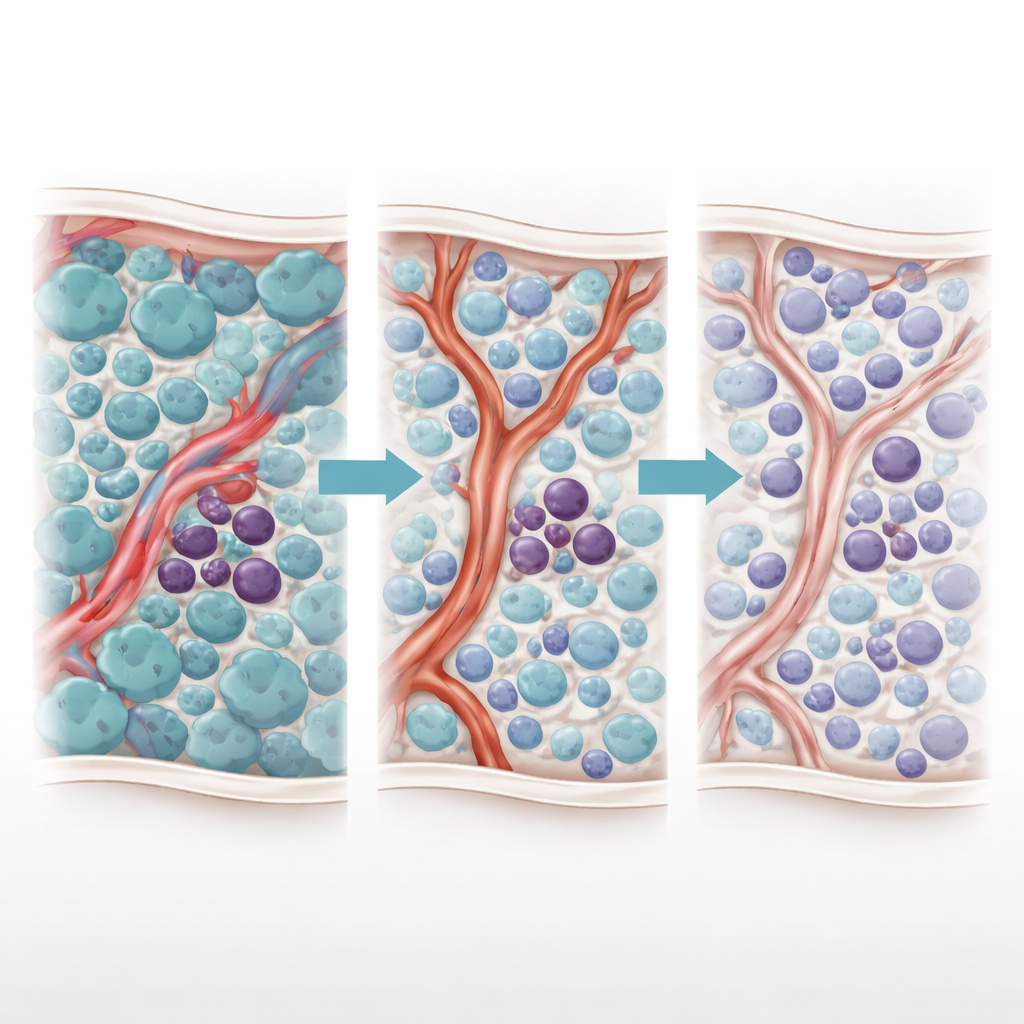
Een dubbelzijdig behandel‑effect
De auteurs beschreven eerder een raadselachtig "Janus‑fenomeen" — een dubbelzinnige reactie op TKI‑therapie. Terwijl TKI’s snel delende blasten doden, dalen de niveaus van het ontstekingsmolecuul TNF‑α. Deze daling maakt het onverwacht mogelijk dat nabije bloedvatcellen de productie van een klein regulatorisch RNA, miR‑126, opdrijven. Dat miR‑126 wordt van endotheelcellen naar leukemiestamcellen overgedragen en duwt die in een rustige, niet‑delende staat die hen sterk resistent maakt tegen geneesmiddelen. Met andere woorden: de behandeling die de meeste kankercellen wegvaagt, herschrijft het beenmerg op een manier die de gevaarlijkste cellen beschermt.
Het bouwen van een virtueel beenmerg
Om deze dynamiek te ontleden bouwde het team een agentgebaseerd computermodel van het AML‑beenmerg. Elke belangrijke speler — blasten, leukemiestamcellen en endotheelcellen die bloedvaten bekleden — wordt voorgesteld als een individuele "agent" die biologisch geïnformeerde regels volgt. Diffunderende moleculen zoals TNF‑α, miR‑126, de TKI AC220 en een miR‑126‑blokkerend middel genaamd miRisten verspreiden zich door het gesimuleerde weefsel. Het model werd gekalibreerd met muizenbeeldvormingsgegevens die echte vasculaire patronen in kaart brengen, inclusief gebieden rijk aan of arm aan miR‑126‑producerende vaten. In simulaties reproduceerde de standaard TKI‑behandeling consequent het Janus‑effect: blasten namen af, TNF‑α daalde, miR‑126 uit vaten schoot omhoog, stamcellen trokken zich terug in beschermende niches en de ziekte kwam later terug.
De beschermlaag uitschakelen met precieze timing
Met dit virtuele systeem testten de onderzoekers manieren om de vicieuze cirkel te doorbreken. Het gelijktijdig toevoegen van miRisten met de TKI hielp, maar genas het model zelden. Een strategischer aanpak bleek krachtiger: een korte "voorbehandeling" met alleen miRisten om vasculair miR‑126 te dempen, gevolgd door ofwel alleen de TKI of voortgezette combinatietherapie. Over veel gesimuleerde vasculaire indelingen bleek zelfs een paar dagen miRisten‑voorbehandeling vóór aanvang van AC220 de terugval dramatisch te verminderen of te voorkomen, terwijl de totale geneesmiddelblootstelling beperkt bleef. Het model toonde ook aan dat de afstand van leukemiestamcellen tot bloedvaten sterk bepaalt wat er met hen gebeurt — cellen die dicht tegen vaten aanliggen krijgen de meeste bescherming, tenzij miR‑126 wordt geblokkeerd.
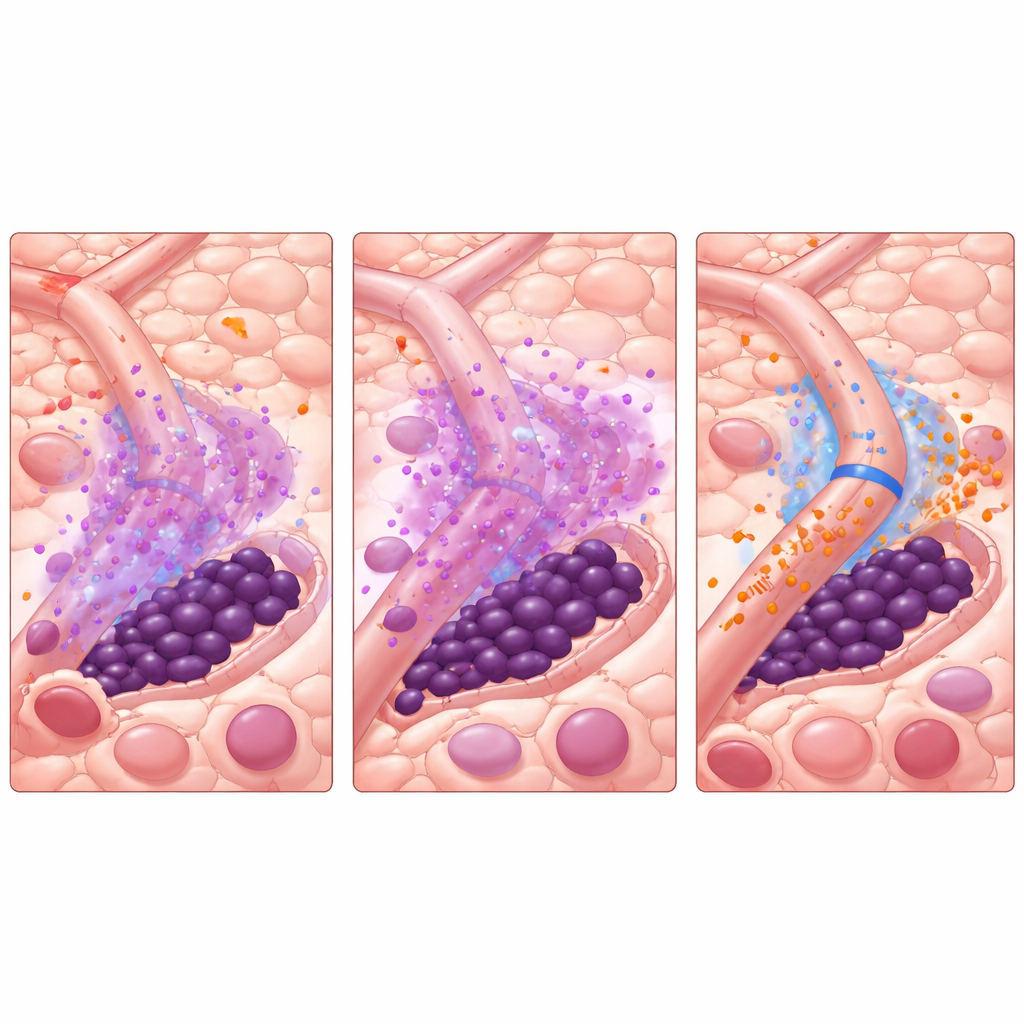
Wat dit kan betekenen voor toekomstige zorg
Simpel gezegd suggereert de studie dat sommige leukemiestamcellen overleven niet omdat TKI’s te zwak zijn, maar omdat de kleine bloedvaten in het beenmerg tijdens de behandeling tijdelijk in een "beschermer"‑modus schakelen. Door kort een enkel signaal, miR‑126, uit te schakelen voordat de TKI wordt toegediend, zou het mogelijk zijn dit schild weg te nemen, stamcellen uit hun schuilplaatsen te forceren en ze vatbaar te maken voor bestaande geneesmiddelen. Hoewel dit werk gebaseerd is op computersimulaties die verankerd zijn in laboratoriumgegevens — en nog niet op klinische studies — biedt het een concrete strategie: timing van een micro‑milieu‑gerichte medicatie net vóór en tijdens de standaardtherapie. Als dit wordt gevalideerd, kan deze aanpak niet alleen de uitkomsten verbeteren voor mensen met FLT3‑gemuteerde AML, maar ook vergelijkbare tactieken inspireren bij andere bloed- en vaste tumoren waarbij de tumoromgeving helpt te ontsnappen aan behandeling.
Bronvermelding: Froid, M., Branciamore, S., Chen, Z. et al. Overcoming vascular niche–mediated TKI resistance in acute myeloid leukemia through miR-126 inhibition. npj Syst Biol Appl 12, 38 (2026). https://doi.org/10.1038/s41540-026-00675-6
Trefwoorden: acute myeloïde leukemie, leukemiestamcellen, bindmerg micro‑milieu, resistentie tegen tyrosinekinaseremmers, remming van miR‑126