Clear Sky Science · nl
Deep-learningmodellen identificeren veranderingen in de hersenen tijdens de voortgang van de ziekte van Alzheimer
Waarom het volgen van hersenverandering in de tijd ertoe doet
De ziekte van Alzheimer berooft mensen geleidelijk van geheugen en denkvermogen, maar de schade in de hersenen bouwt zich jaren op voordat alledaagse symptomen duidelijk worden. Artsen baseren hun oordeel meestal op één enkele hersenscan of testuitslag om vast te stellen of iemand Alzheimer heeft, terwijl de ziekte zich in de tijd ontvouwt. Deze studie stelt een eenvoudige vraag met grote gevolgen: als we scans van iemands hersenen meerdere jaren volgen en een geavanceerd computermodel van die veranderingen laten leren, kunnen we dan niet alleen Alzheimer nauwkeuriger detecteren, maar ook zien welke hersengebieden het eerst en het meest worden getroffen?
Het verhaal van het brein volgen, niet alleen een momentopname
De onderzoekers gebruikten structurele MRI-scans, die gedetailleerde hersenanatomie weergeven, van meer dan 280 oudere volwassenen, waaronder mensen met Alzheimer en cognitief normale leeftijdsgenoten. Cruciaal is dat elke persoon drie scans had die ongeveer een jaar uit elkaar lagen, waardoor het team kon volgen hoe hersenweefsel zich over twee jaar ontwikkelde. In plaats van elke scan als een afzonderlijke foto te behandelen, bouwden ze een deep-learningmodel dat alle tijdstippen samen neemt. Het model was ontworpen om aandacht te besteden aan grijze stof—het hersenweefsel met cellichamen van neuronen—alsook aan witte stof en cerebrospinale vloeistof, en om te leren hoe patronen in deze weefsels evolueren naarmate de ziekte vordert.
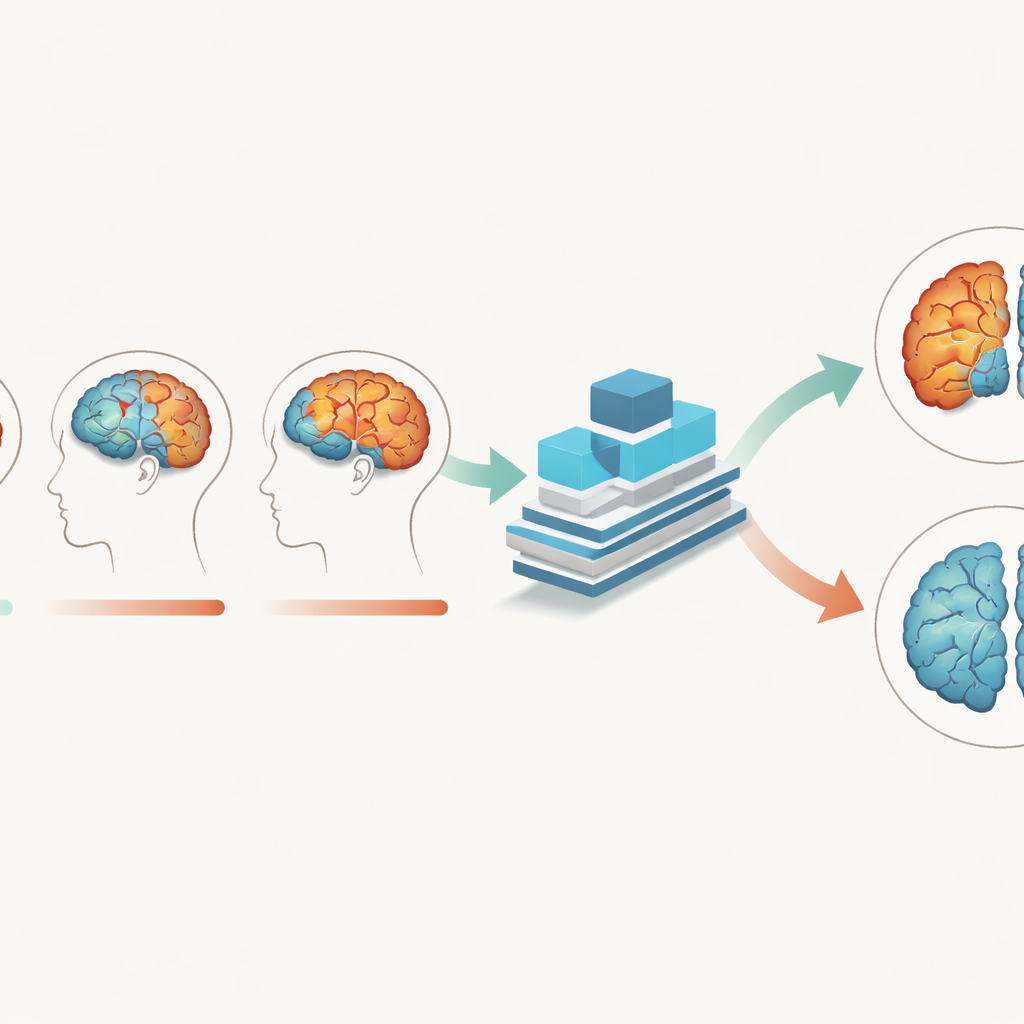
Een deep-learningmodel afgestemd op hersenritmes
Om deze subtiele verschuivingen vast te leggen creëerde het team een Multi-Branch Fusion Channel Attention Network, een 3D-convolutioneel neuraal netwerk dat MRI-volumes verwerkt in plaats van platte beelden. Separate takken verwerken verschillende weefsels of tijdstippen en fusen vervolgens hun informatie, terwijl een "attention"-mechanisme het model helpt te focussen op de meest informatieve regio’s in driedimensionale ruimte. Voornamelijk getraind op grijze-stofgegevens, leerde het netwerk Alzheimer-hersenen te onderscheiden van normaal verouderende hersenen met ongeveer 93% nauwkeurigheid en perfecte specificiteit in één dataset, waarmee het meerdere bestaande AI-methoden overtrof. Het generaliseerde ook goed naar een onafhankelijke Australische dataset, wat suggereert dat het niet eenvoudigweg eigenaardigheden van één studie uit het hoofd leerde maar bredere ziektekens vastlegt.
Zien welke hersenregio’s de doorslag geven
Hoge nauwkeurigheid alleen is niet genoeg voor de geneeskunde; clinici moeten begrijpen wat de beslissingen van een model aandrijft. De onderzoekers gebruikten daarom een interpreteerbaarheidstechniek genaamd SHAP, die een belangrijkheidsscore toekent aan elk klein driedimensionaal pixel—of voxel—in de MRI. Het groeperen van deze voxels in anatomische regio’s onthulde een dynamisch beeld van de ziekte. In een vroeg stadium stak de amygdala, een regio die betrokken is bij emotie en geheugen, vooral bovenuit als belangrijk voor het onderscheiden van patiënten van gezonde leeftijdsgenoten. In de loop van de tijd kregen de hippocampus, de parahippocampale gyrus en vooral de achterste delen van de temporale kwab meer invloed, terwijl de relatieve rol van de amygdala afnam. Na twee jaar waren de verschillen tussen patiënten en controles veel scherper en meer geclusterd, met name aan de linkerkant van de hersenen.
Patronen die overeenkomen met symptomen en klinische scores
Om te controleren of de focus van het model overeenkwam met de biologie, voerde het team traditionele analyses van hersenvolume en statistische toetsen uit. Ze vonden dat de grijze stof in de gemarkeerde regio’s sneller krimpte bij mensen met Alzheimer dan bij normaal verouderende volwassenen, en dat lager volume in deze gebieden nauw samenhing met slechtere scores op standaard cognitieve tests zoals de Mini-Mental State Examination en de Clinical Dementia Rating. Het pad van schade—van interne temporale structuren naar buiten toe naar achterste taal- en associatiegebieden—spiegelde klassieke pathologische indelingsschema’s voor Alzheimer. Er trad ook een linkszijdige voorkeur op, in overeenstemming met de dominantie van de hersenen voor taal en bepaalde geheugenfuncties aan die zijde. Voxel-gebaseerde morfometrie liet zien dat vroege veranderingen verspreid en klein waren, en later groter en geconcentreerder werden in de achterste temporale en frontale regio’s naarmate de ziekte vorderde.
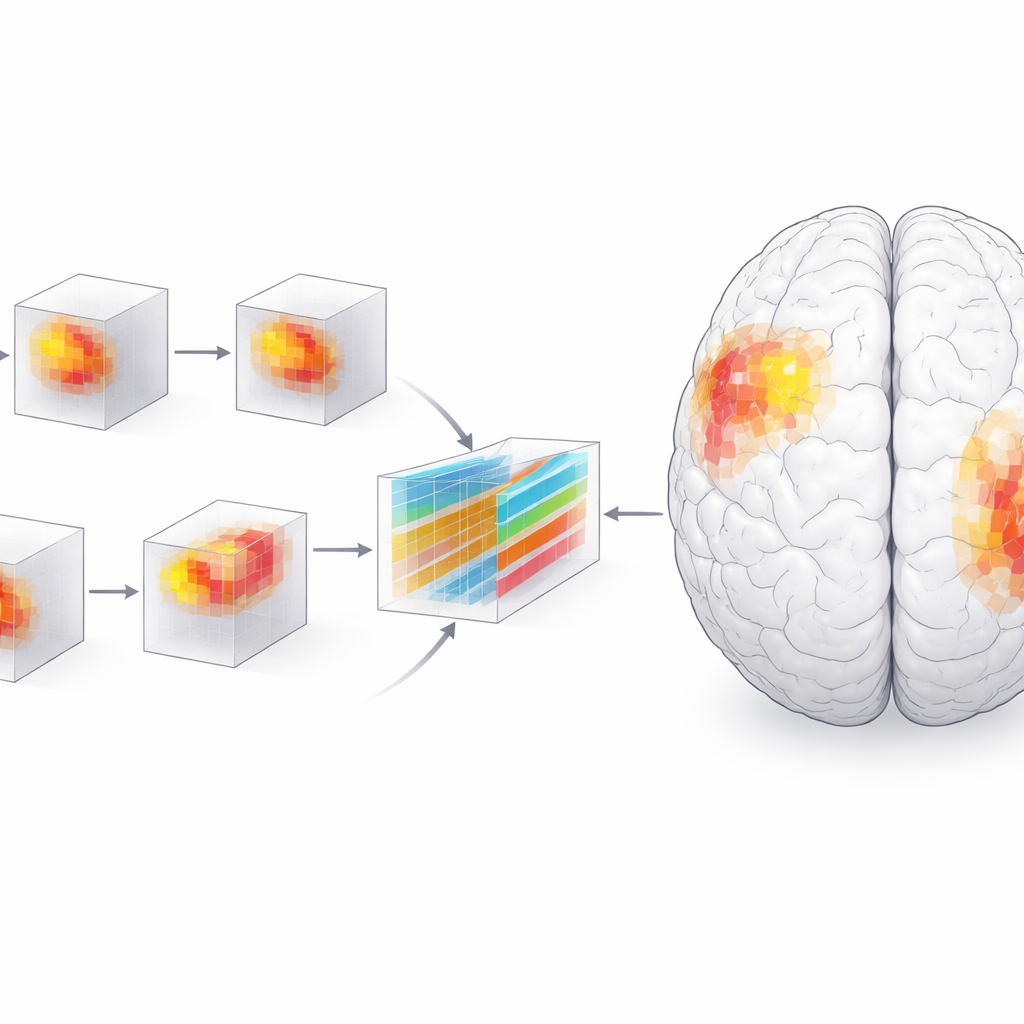
Wat dit betekent voor patiënten en artsen
Voor niet-specialisten is de kernboodschap dat Alzheimer zich niet gedraagt als een eenvoudige aan–uit-schakelaar in de hersenen; het volgt een ordelijke maar versnellende route en laat in de loop van de tijd herkenbare sporen achter. Door een deep-learningmodel te leren niet alleen te lezen waar de hersenen anders zijn, maar hoe die verschillen over meerdere jaren groeien, biedt deze studie een manier om Alzheimer nauwkeuriger en eerder in het beloop te signaleren. Het wijst ook op een kleine set hersengebieden—waaronder de amygdala, hippocampus, parahippocampale gyrus en de achterste temporale cortex—wiens veranderende grootte en structuur sterk samenhangen met cognitieve achteruitgang. Hoewel meer werk nodig is, vooral met aanvullende beeldvormingstechnieken en grotere datasets, brengt deze benadering ons dichter bij het gebruik van tijd-resolved hersenscans en interpreteerbare AI als praktische hulpmiddelen voor vroege diagnose, monitoring en uiteindelijk het sturen van interventies tegen de ziekte van Alzheimer.
Bronvermelding: Sun, J., Han, JD.J. & Chen, W. Deep learning models identify brain changes during the progression of Alzheimer’s disease. npj Syst Biol Appl 12, 42 (2026). https://doi.org/10.1038/s41540-026-00666-7
Trefwoorden: Ziekte van Alzheimer, hersenen MRI, deep learning, longitudinale beeldvorming, neurodegeneratie