Clear Sky Science · nl
Ontwikkeling van een ernstig rattenmodel voor refeedingsyndroom en wiskundige modellering van de bijbehorende hypofosfatemie
Waarom weer eten gevaarlijk kan zijn
Wanneer ernstig ondervoede mensen eindelijk voedsel of intraveneuze voeding krijgen, moeten artsen voorzichtig te werk gaan. Een plotselinge instroom van calorieën kan het zogenaamde „refeeding syndrome” veroorzaken, een complicatie die de elektrolytenbalans verstoort en het hart, de spieren en de longen kan schaden. Een belangrijke speler is fosfor, een mineraal dat in elke cel nodig is voor energie. In deze studie gebruikten onderzoekers ratten en computermodellen om te achterhalen waarom het fosforgehalte in het bloed tijdens refeeding zo dramatisch kan instorten en hoe we die gevaarlijke daling beter kunnen voorkomen.
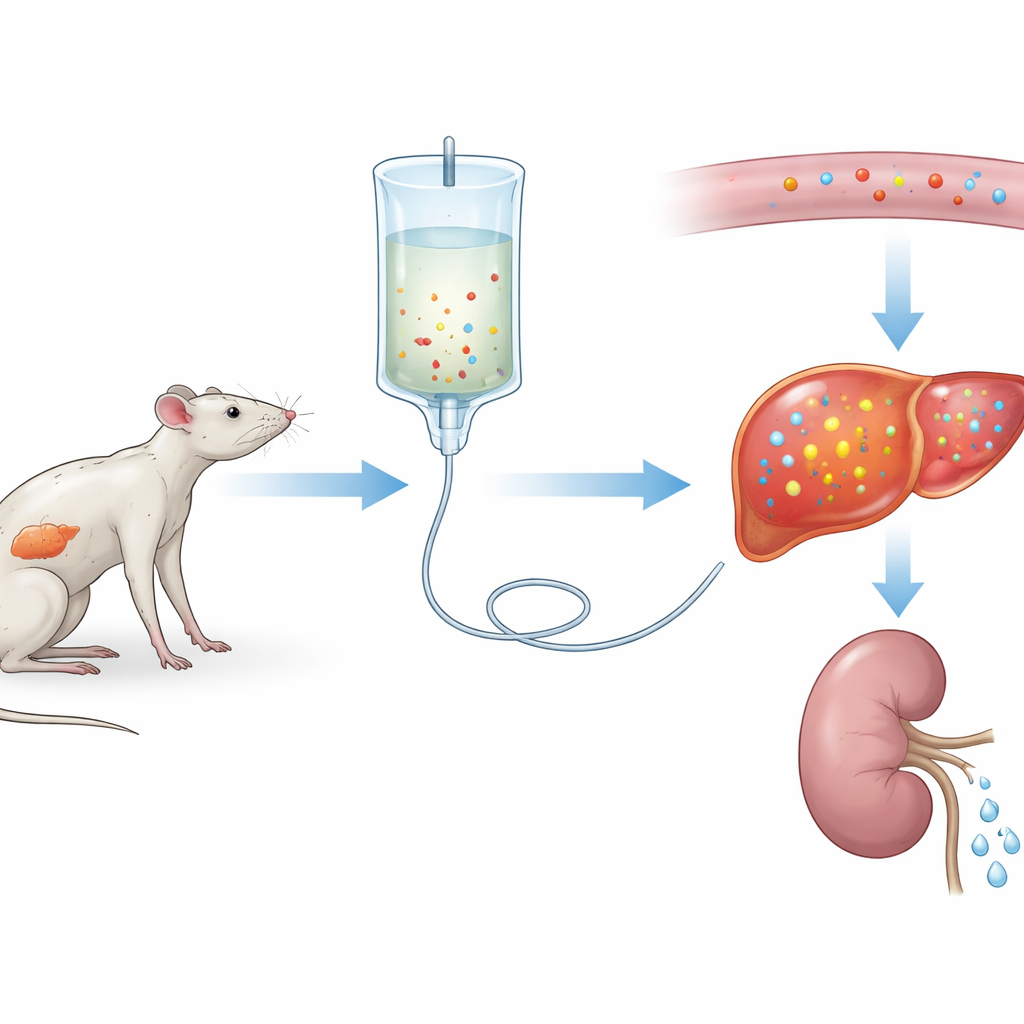
Een nadere blik op refeeding-problemen
De onderzoekers creëerden eerst een ernstige vorm van het refeedingsyndroom bij ratten. Drie weken lang kreeg de ene groep een normaal dieet, terwijl de andere groep zeer weinig eiwit kreeg, wat langdurige ondervoeding nabootst. Beide groepen kregen vervolgens drie dagen dezelfde intraveneuze voeding. Ratten op het eiwitarme dieet lieten een sterke daling van het bloedfosfor zien—ongeveer 75%—samen met verschuivingen in andere elektrolyten en tekenen van orgaanschade, met name in de lever en spieren. Deze veranderingen kwamen overeen met ernstig refeedingsyndroom bij patiënten, wat aangeeft dat het team een betrouwbaar experimenteel model had ontwikkeld.
Wat er met fosfor gebeurt tijdens refeeding
Om te begrijpen hoe fosfor zich in het lichaam in de loop van de tijd verplaatst, namen de wetenschappers herhaaldelijk bloed- en urinemonsters van dezelfde ratten. Ze ontdekten dat het bloedfosfor daalde in zowel normale als eiwit-ondervoede dieren nadat de voeding begon, maar de daling was veel dieper en langduriger in de ondervoede groep. Verrassend genoeg verminderden de nieren juist het fosforverlies in de urine direct na refeeding, dus het mineraal werd niet uitgescheiden. In plaats daarvan werd fosfor uit de bloedbaan naar weefsels getrokken, vooral naar de lever, waar de voorraden na weken van slecht dieet waren uitgeput. Berekeningen met de computer bevestigden dat de ondervoede ratten begonnen met veel lagere intracellulaire fosforvoorraden en die vervolgens agressief aanvulden zodra voedingsstoffen beschikbaar kwamen.
Insuline is niet het hele verhaal
Omdat refeeding de bloedsuiker en het hormoon insuline verhoogt, schreven artsen insuline lange tijd de schuld toe voor het naar cellen drijven van fosfor. Het team testte dit idee door de insulineafgifte te dempen met het hormoon somatostatine. Zoals verwacht steeg de bloedsuiker, maar de inzinking van het bloedfosfor verbeterde nauwelijks. Tegelijkertijd namen de concentraties vrije aminozuren—de bouwstenen van eiwitten—toe. In een apart experiment verwijderden de wetenschappers aminozuren uit de infusie. Nu bleven de fosforwaarden veel stabieler en werd de ernstige crash voorkomen, hoewel de insulinespiegels vergelijkbaar waren. Deze resultaten wijzen op een gecombineerde werking: zowel insuline als aminozuren, en niet alleen insuline, zetten cellen ertoe aan extra fosfor op te nemen tijdens refeeding.
Een verborgen regelnetwerk in lever en nier
Dieper gravend onderzochten de onderzoekers leverproteïnen die betrokken zijn bij nutriëntendetectie, met de nadruk op een pathway bekend als mTOR, die reageert op insuline en aminozuren. Bij de eiwitarme ratten activeerde refeeding deze pathway sterk en nam het niveau toe van een fosfaattransporter genaamd Pit2, die levercellen helpt fosfor op te nemen. Het patroon kwam overeen met het gedrag dat hun wiskundige model voorspelde, waarin dit netwerk werd samengevat in een enkele regelsignaal dat ze „simTOR” noemden. Het model vereiste ook een aparte feedbackfactor om te verklaren hoe de nieren het fosforverlies in de urine aanpassen. Metingen van een door bot afgeleid hormoon, FGF-23, pasten goed bij deze rol: de concentraties doken in nadat het eten begon, waardoor fosforuitscheiding beperkt werd, en daarna verschilden ze tussen normale en ondervoede ratten op een manier die het gesimuleerde feedbacksignaal spiegelde.
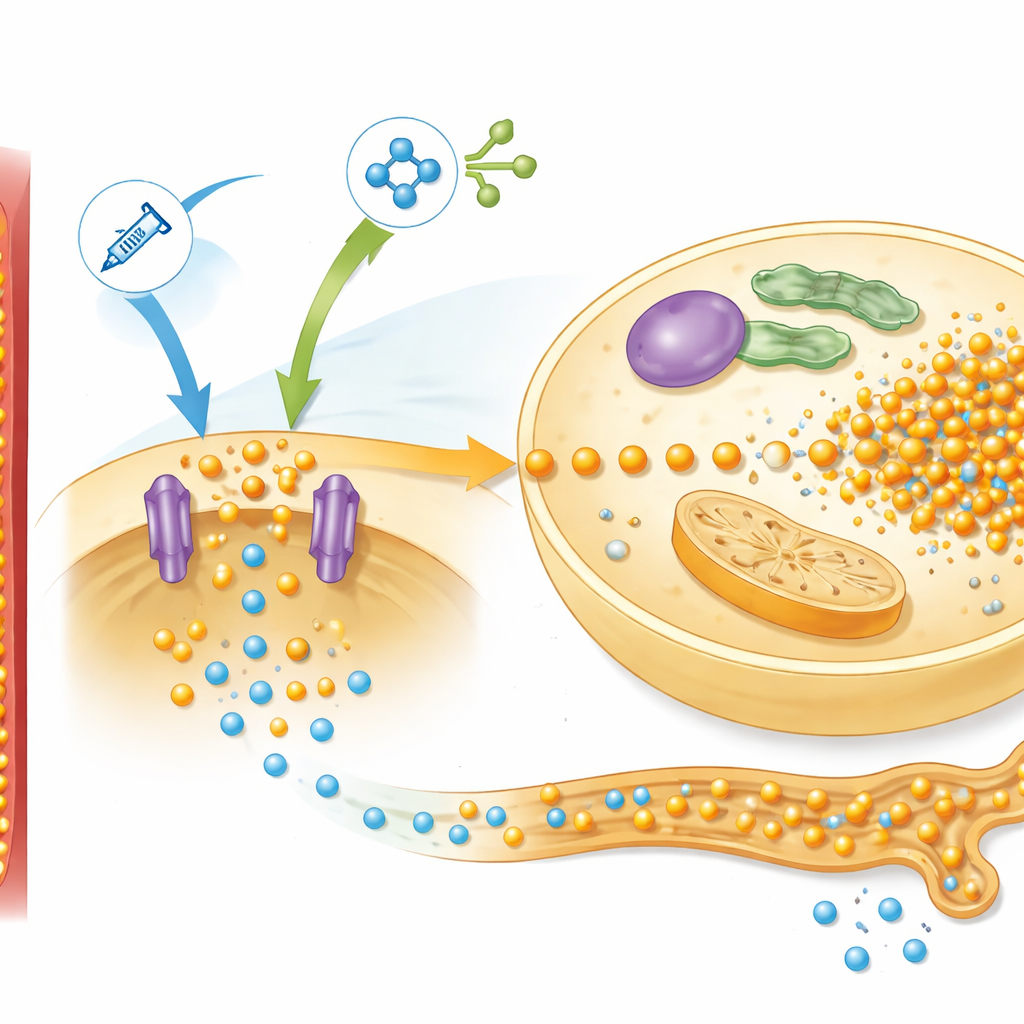
Wiskunde gebruiken om preventiestrategieën te testen
Door aan verschillende knoppen in hun computermodel te draaien, konden de auteurs „wat-als”-vragen stellen die moeilijk of riskant direct bij patiënten te testen zouden zijn. De analyse benadrukte drie belangrijke invloeden op de diepte en het herstel van de fosfordaling: het aanvankelijke intracellulaire fosfor, de sterkte van het mTOR-gedreven opnamesysteem en de snelheid van fosforinname via voeding. Simulaties suggereerden dat het simpelweg toedienen van een grote hoeveelheid fosfaat op het moment van refeeding moeilijk veilig te balanceren zou zijn. Extra fosfor geven vóór refeeding—waardoor organen rustig hun interne voorraden kunnen herbouwen—zou echter de latere inzinking in bloedwaarden kunnen verzachten. Het verminderen van de aminozuurlast, met name die aminozuren die mTOR en insuline sterk activeren, bleek ook beschermend in de dierproeven.
Wat dit betekent voor patiënten
Voor mensen met risico op refeedingsyndroom—zoals personen met langdurige eetstoornissen of ernstige zwakte—suggereert dit werk dat het gevaar meer is dan alleen een piek in de bloedsuiker. Uitgehongerde organen beginnen refeeding met lege fosfortanks en nemen onder de gecombineerde aandrang van insuline en aminozuren snel het mineraal uit het bloed op, terwijl de nieren het kort vasthouden. Het resultaat is een scherpe, tijdelijke tekort aan circulerend fosfor dat vitale weefsels kan beschadigen. Het rattenmodel en het wiskundige kader die hier zijn ontwikkeld wijzen op meer gerichte preventie: behoedzaam vroegtijdig gebruik van fosfoorsuppletie, zorgvuldige controle van aminozuurrijke voeding en aandacht voor hormonen die de nieruitscheiding regelen. Samen kunnen deze benaderingen artsen helpen kwetsbare patiënten veiliger te voeden.
Bronvermelding: Kato, H., Yamaoka, I. & Kubota, H. Development of a severe rat refeeding syndrome model and mathematical modeling of the associated hypophosphatemia. npj Syst Biol Appl 12, 34 (2026). https://doi.org/10.1038/s41540-026-00658-7
Trefwoorden: refeeding syndrome, hypofosfatemie, fosformetabolisme, mTOR-signaaltransductie, parenterale voeding