Clear Sky Science · nl
Ruimtelijke FBA onthult heterogene Warburg-niches in nier tumoren en lactaatconsumptie bij colorectale kanker
Waarom tumormetabolisme in de ruimte ertoe doet
Kankercellen gedragen zich niet allemaal hetzelfde, zelfs niet binnen één tumor. Sommige zitten dicht bij bloedvaten, andere diep in slecht doorvoede gebieden, en die locaties bepalen hoe ze brandstof verwerven en gebruiken. Deze studie introduceert een nieuwe manier om die verborgen “metabole kaart” af te lezen uit geavanceerde ruimtelijke genexpressiegegevens. Daardoor ontdekken de auteurs verrassende patronen in hoe verschillende tumoren met een sleutelmolecuul, lactaat, omgaan, wat de klassieke opvatting uitdaagt dat kankers uitsluitend lactaat als afvalproduct afvoeren.
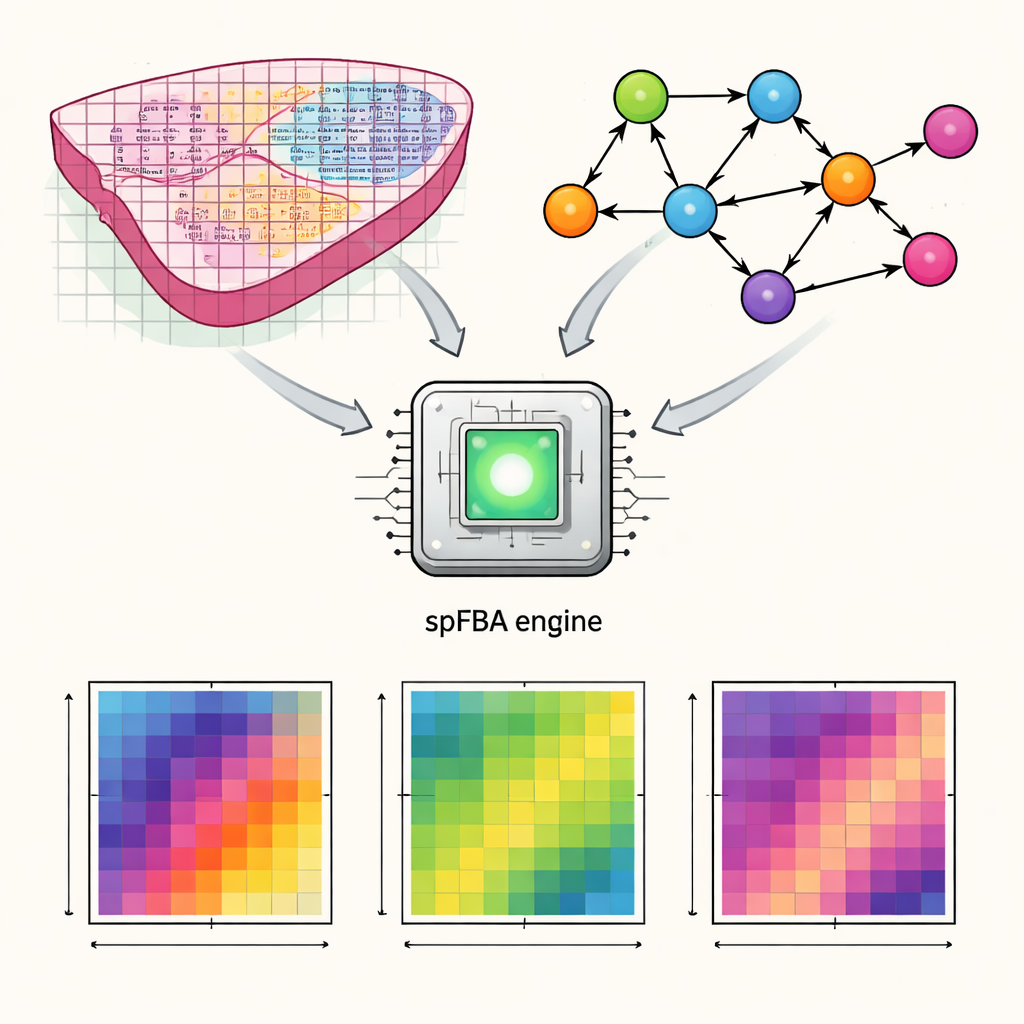
Genkaarten omzetten in metabole activiteit
De auteurs ontwikkelden een computationeel raamwerk genaamd ruimtelijke Flux Balance Analysis, of spFBA. Ruimtelijke transcriptomica-technologieën meten welke genen actief zijn op duizenden kleine punten over een dun weefselplaatje. spFBA combineert deze ruimtelijke genactiviteitskaarten met gedetailleerde modellen van de menselijke stofwisseling, die beschrijven hoe voedingsstoffen zoals glucose, zuurstof en aminozuren binnen cellen worden omgezet. In plaats van aan te nemen dat elk gebied van een weefsel hetzelfde metabole doel deelt, behandelt spFBA elk punt onafhankelijk en onderzoekt welke reacties daar mogelijk zijn volgens de wetten van de scheikunde en massabalans. De output is een reeks “fluxverrijkingsscores” die voor elke locatie aangeven hoe sterk verschillende metabole reacties waarschijnlijk stromen en in welke richting.
De methode testen in niertumoren
Om te beoordelen of spFBA biologisch zinvolle resultaten oplevert, richtte het team zich eerst op clear cell niercelcarcinoom, een nierkanker die bekendstaat om sterk te vertrouwen op suikerafbraak (glycolyse) en lactaatafgifte, een fenomeen dat het Warburg-effect wordt genoemd. Met gepubliceerde ruimtelijke gegevens van tien niertumormonsters vroegen ze of de voorspelde metabolische patronen overeenkwamen met de bekende weefselstructuur. Ze vonden dat locaties die gegroepeerd waren op basis van hun afgeleide metabole fluxen goed overeenkwamen met de histologische organisatie onder de microscoop en met clusters gebaseerd op alleen genexpressie. Belangrijk was dat spFBA het verwachte metabole contrast tussen tumor en normaal nierweefsel reproduceerde: tumorgebieden vertoonden hoger glucosegebruik, sterkere biomassa-productie (een proxy voor celgroei) en robuuste lactaatsecretie. Tegelijk bleef zuurstofgebruik aanzienlijk, wat aantoont dat verschillende delen van dezelfde tumor fermentatie en respiratie kunnen combineren afhankelijk van de lokale bloedvoorziening.
Colorectale kankers tonen een ander lactaatverhaal
Vervolgens pasten de onderzoekers dezelfde pijplijn toe op nieuwe hoogresolutie-ruimtelijke datasets van een patiënt met een primaire colorectale tumor en bijbehorende levermetastasen, evenals op een onafhankelijk openbaar colorectaal dataset gemaakt met een andere technologie. Hier waren de resultaten opvallend anders. In plaats van lactaat uit te voeren als afval, werd voorspeld dat de meeste colorectale kankergebieden — zowel in de oorspronkelijke colon-tumor als in levermetastasen — lactaat uit hun omgeving opnemen. Stromale cellen in het nabije ondersteunende weefsel lijken kleine hoeveelheden lactaat vrij te geven, terwijl tumorcellen sterke consumenten waren. Door reactieniveau-fluxpatronen te volgen, laten de auteurs zien dat deze metastatische cellen lactaat niet simpelweg verbranden in de gebruikelijke energieproducerende cyclus in de mitochondriën. In plaats daarvan zetten ze lactaat om in bouwstenen die instromen in routes voor de aanmaak van vetten en andere componenten die nodig zijn voor celgroei, een “pseudo-omgekeerd Warburg-effect” waarin lactaat grondstof wordt voor biosynthese.
Metabole niches en de tumor-stroma grens
Aangezien spFBA de ruimtelijke indeling behoudt, kan het aangeven waar specifieke metabole uitwisselingen plaatsvinden. In niertumoren onthulde de methode naast elkaar bestaande metabole “buurten”: beter geoxygeneerde, bloedrijke interfaces waar kankercellen zowel respireren als fermenteren, en diepere, slecht gevasculariseerde kernen die sterker op fermentatie vertrouwen. In colorectale levermetastasen benadrukte spFBA scherpe contrasten aan de grens tussen tumor en stroma, waar de omgang met glutamaat en lactaat van richting veranderde, wat wijst op intense uitwisseling aan het invasieve front. In alle datasets correleerden voorspelde groeigerelateerde fluxen met onafhankelijke gengebaseerde maatstaven voor proliferatie, wat de biologische realiteit van het model ondersteunt. Cruciaal is dat hetzelfde algoritme lactaatsecretie in nierkanker voorspelde maar lactaatopname in colorectale kanker, wat aangeeft dat de waargenomen verschillen uit de gegevens voortkomen en niet uit een ingebouwde modelbias.
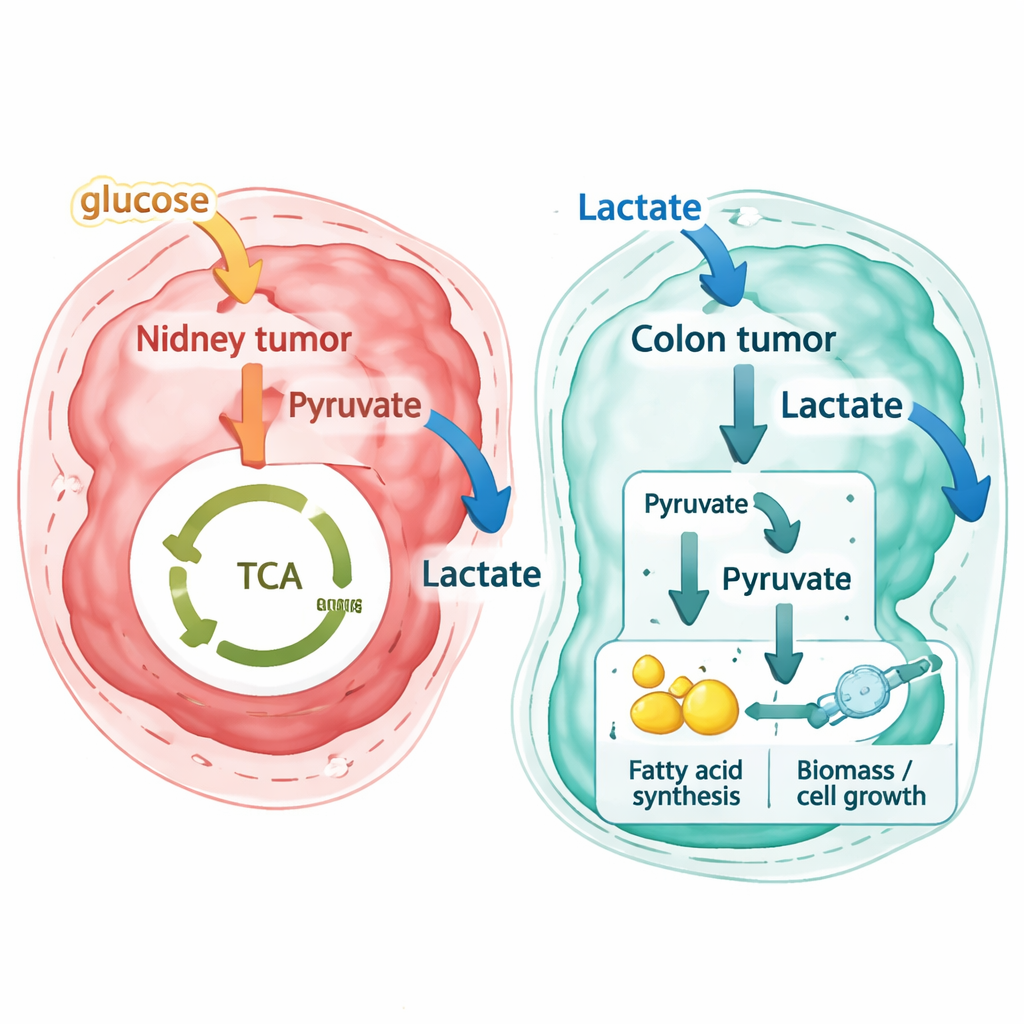
Wat dit betekent voor het begrijpen en behandelen van kanker
Voor niet-specialisten is de kernboodschap dat kankermetabolisme niet alleen abnormaal is — het is ook sterk lokaal. Dezelfde tumor kan meerdere metabole niches herbergen, en tumoren die er vergelijkbaar uitzien in verschillende organen kunnen dezelfde moleculen op tegengestelde manieren gebruiken. Dit werk laat zien dat door ruimtelijke genexpressie te combineren met gedetailleerde metabole modellen, onderzoekers kunnen afleiden waar tumoren waarschijnlijk hongerig zijn naar bepaalde voedingsstoffen zoals lactaat. Bij colorectale kanker roept de ontdekking dat tumorcellen lactaat in hoge mate consumeren en doorsturen naar groeigerelateerde processen nieuwe vragen op over hoe dieet, darmmicroben en de eigen stofwisseling van de lever de ziekteprogressie beïnvloeden, en of het blokkeren van lactaatgebruik deze tumoren gevoeliger voor therapie zou maken.
Bronvermelding: Maspero, D., Marteletto, G., Lapi, F. et al. Spatial FBA reveals heterogeneous Warburg niches in renal tumors and lactate consumption in colorectal cancer. npj Syst Biol Appl 12, 32 (2026). https://doi.org/10.1038/s41540-026-00654-x
Trefwoorden: kankermetabolisme, ruimtelijke transcriptomica, lactaat, Warburg-effect, colorectale kanker