Clear Sky Science · nl
Dynamische netwerkanalyse onthult langafstandsresidu‑koppelingen op het pMHC‑oppervlak die verbeterde immunogeniciteit onderliggen
Hoe piepkleine virale fragmenten onze afweer sturen
Onze killer‑T‑cellen patrouilleren het lichaam op zoek naar tekenen van infectie of kanker. Ze doen dat door naar piepkleine eiwitfragmenten, peptides genoemd, te kijken die door MHC‑klasse I‑moleculen op celoppervlakken worden gepresenteerd. Deze studie stelt een subtiele maar belangrijke vraag: hoe kan één kleine verandering in zo’n peptide ervoor zorgen dat T‑cellen veel sterker reageren — of juist helemaal niet? Het antwoord blijkt niet alleen in de statische structuur te liggen, maar in hoe het gehele moleculaire complex in de tijd beweegt en buigt.
Het slot, de sleutel en de bewegende onderdelen
Om het werk te begrijpen, helpt het om het peptide–MHC (pMHC)‑complex als een slot voor te stellen en de T‑celreceptor (TCR) als de sleutel. Het peptide ligt in een groeve op het MHC‑molecuul en samen vormen ze het oppervlak dat de TCR onderzoekt. Eerder onderzoek heeft laten zien dat zowel de exacte peptide‑volgorde als de specifieke MHC‑variant sterk bepalen of een T‑cel reageert. Wetenschappers hebben ook “veranderde peptide‑liganden” geconstrueerd met kleine aanpassingen om immuunreacties te sturen, onder andere in kankerimmunotherapie. Maar ondanks dat we veel weten over de statische vormen van deze complexen, weten we veel minder over hoe bewegingen op één punt in het peptide invloed kunnen hebben op verre delen van het oppervlak waar de TCR bindt.
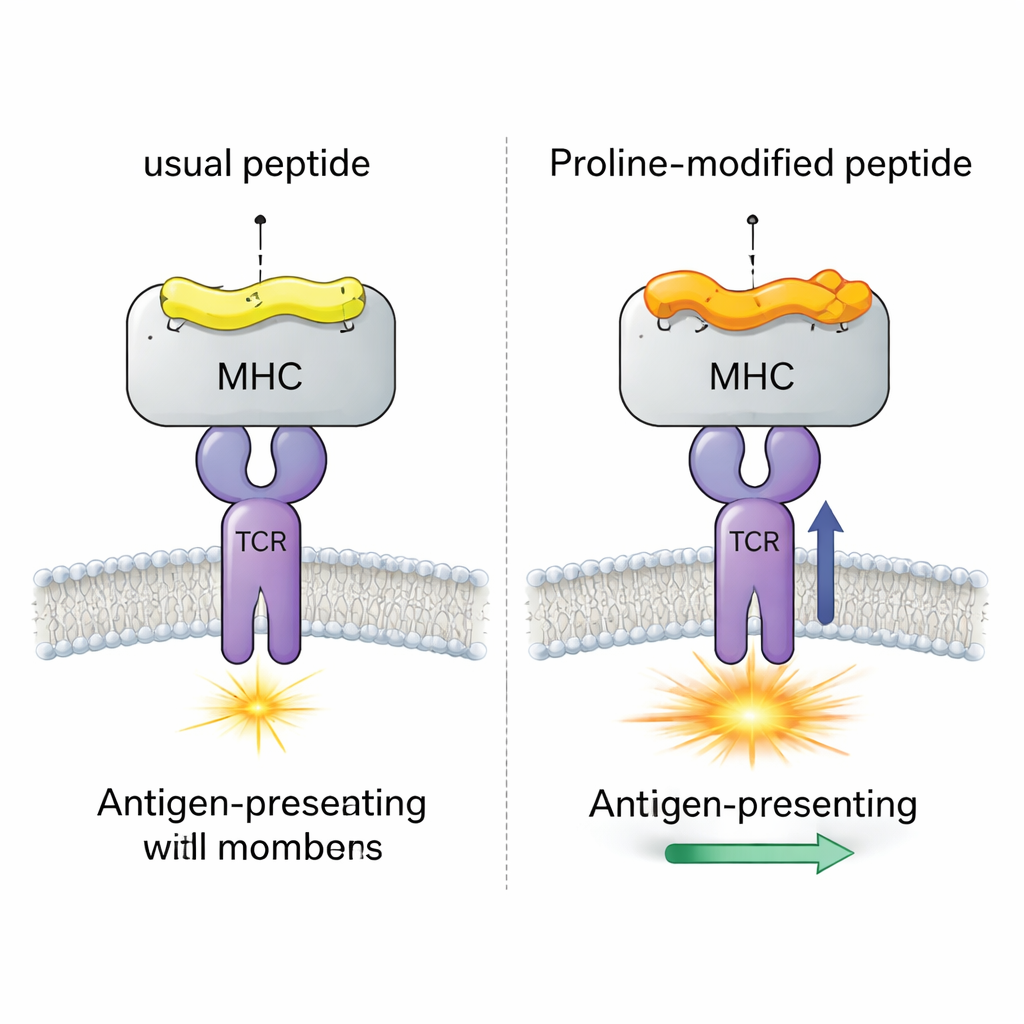
Een viraal testgeval met vier bijna identieke peptides
Het team richtte zich op een goed bestudeerd muizenvirus (LCMV) systeem met het peptide gp33, dat normaal sterke CD8+ T‑celresponsen opwekt. Ze vergeleken vier nauw verwante versies van dit peptide, allemaal gebonden aan hetzelfde MHC‑molecuul (H‑2Db). Eén versie is het oorspronkelijke virale peptide; één draagt een immuunontwijkende mutatie die T‑cellen nauwelijks herkennen; en twee zijn “proline‑gewijzigde” vaccin‑kandidaten waarin één aminozuur nabij het begin van het peptide is vervangen door proline. Eerdere experimenten toonden aan dat deze proline‑wissel de stabiliteit van het peptide–MHC‑complex verhoogt en de reactie van een model‑TCR (genoemd P14) versterkt, maar het gedetailleerde mechanisme bleef onduidelijk.
Moleculen zien wiebelen: simulaties gecombineerd met kristallografie
Om te achterhalen wat er gebeurt, combineerden de auteurs hoogresolutie kristalstructuren met lange, atoom‑voor‑atoom computersimulaties van elk pMHC‑complex in beweging. Ze onderzochten hoe sterk elk aminozuurresidu in de loop van de tijd fluctueert en hoe deze fluctuaties veranderen wanneer de derde positie in het peptide in proline wordt omgezet. Door bewegingspatronen over vele gekoppelde simulaties te correleren, bouwden ze een "dynamische kaart" van welke residuen samen bewegen, ook als ze ver van elkaar in de ruimtelijke structuur liggen. Ze zetten die kaart daarna om in een netwerk, waarin elk residu een knoop is en randen statistisch gekoppelde bewegingen representeren, en analyseerden dit netwerk met grafentheorie‑tools vergelijkbaar met die in sociale netwerkanalyse.
Langafstandscommunicatie binnen het immuunslot
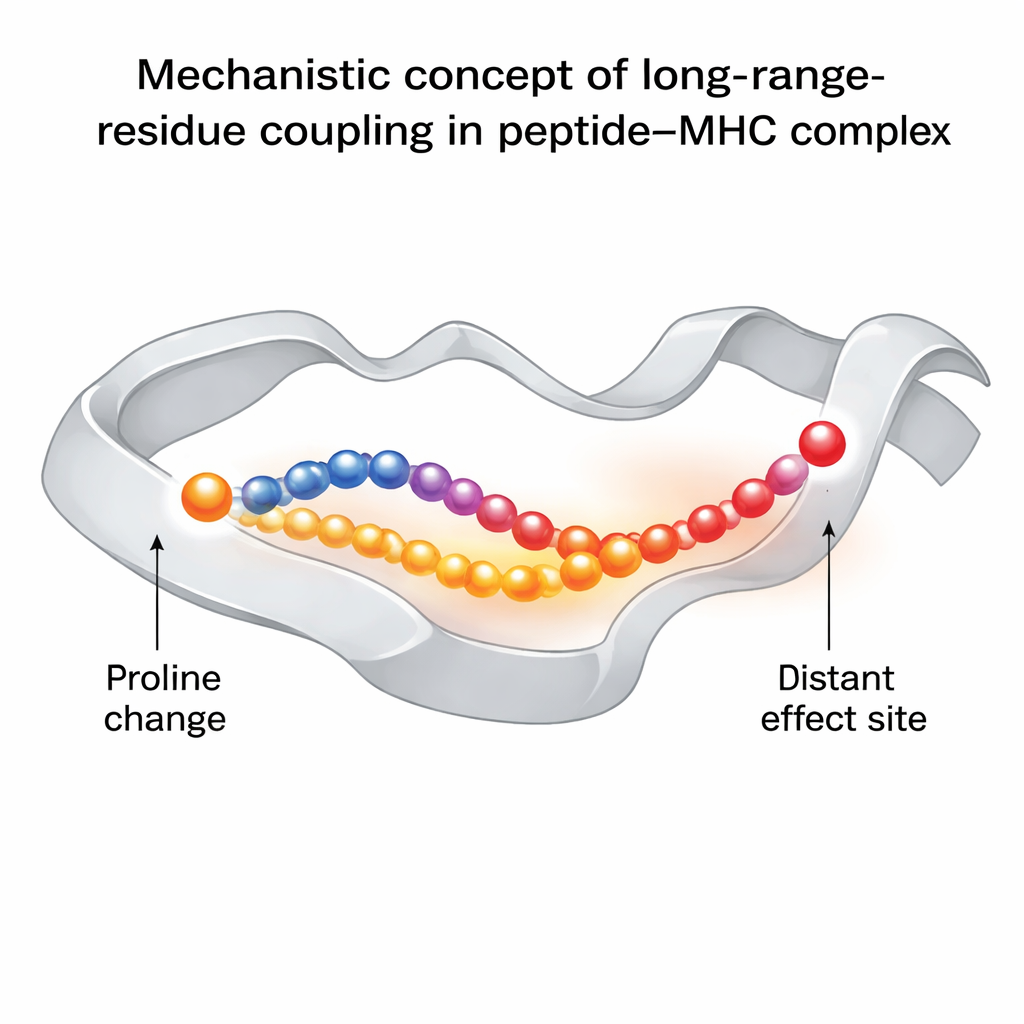
De centrale bevinding is dat het veranderen van het derde peptide‑residu naar proline meer doet dan alleen die lokale plek verkrampen. Het verandert hoe bewegingen worden doorgegeven langs één van de MHC‑helixen die de peptidebindingsgroeve begrenzen. Dat beïnvloedt op zijn beurt het gedrag van een ander peptide‑residu, positie zes, dat direct onder het TCR‑contactgebied ligt en cruciaal is voor herkenning. In de “goede” proline‑gewijzigde versies neemt dit residu een breder scala aan conformaties aan, inclusief die welke optimaal zijn voor TCR‑binding. In de immuunontwijkende variant zonder proline zit dat residu veel meer vast en neemt het zelden de TCR‑vriendelijke oriëntatie aan. Netwerkanalyse laat zien dat deze invloed via specifieke aminozuren in de MHC‑groeve reist, waarbij een keten van dynamisch gekoppelde residuen het wijzigingspunt met het TCR‑contactgebied verbindt.
Waarom dit ertoe doet voor vaccins en immunotherapie
Deze resultaten tonen aan dat immunogeniciteit — hoe sterk een peptide T‑cellen activeert — niet alleen gaat om of vormen op een enkel moment passen, maar ook om hoe het complex in de tijd ademt en buigt. Een subtiele verandering op één positie kan door het moleculaire netwerk heen golven en ervoor zorgen dat sleutelcontactresiduen vaker in TCR‑compatibele houdingen verschijnen. De rekenkundige workflow van de auteurs biedt een manier om zulke langafstands‑koppelingen systematisch te detecteren, wat kan helpen bij het ontwerpen van gewijzigde peptides voor vaccins en kankertherapieën. Simpel gezegd laten ze zien dat je door zorgvuldig te kiezen waar je een peptide aanpast, het hele slot in een meer "klaar‑om‑te‑openen" dynamische toestand voor het immuunsysteem kunt duwen.
Bronvermelding: Resink, T., Sala, B.M., Sun, R. et al. Dynamical network analysis reveals long-range residue couplings at the pMHC interface underlying enhanced immunogenicity. npj Syst Biol Appl 12, 15 (2026). https://doi.org/10.1038/s41540-026-00653-y
Trefwoorden: T-celherkenning, peptide MHC, proteïnedynamica, veranderde peptide‑liganden, immunogeniciteit