Clear Sky Science · nl
In silico modellering van differentiatie van anterior foregut endoderm naar long-epitheliale voorlopercellen
Stamcellen omzetten in longbouwcellen
Wetenschappers leren hoe ze de eigen stamcellen van een patiënt kunnen aanzetten tot het vormen van vervangend longweefsel, dat op den duur schade door ziekten zoals COPD, fibrose of ernstige infecties zou kunnen herstellen. Dit artikel onderzoekt hoe onderzoekers computermodellering gebruikten om een cruciale stap in dat proces in kaart te brengen en te verfijnen: het omzetten van een tussenliggende celtype, het anterior foregut endoderm, naar vroege long-epitheliale voorlopercellen—de startcellen die uiteindelijk de luchtwegen en longblaasjes kunnen vormen.
Waarom longstartcellen belangrijk zijn
Menselijke geïnduceerde pluripotente stamcellen (iPSC's) kunnen uit volwassen weefsels worden herprogrammeerd en vervolgens worden geleid naar veel verschillende orgaansystemen. Om longweefsel te bouwen, passeren deze cellen eerst meerdere ontwikkelingsstations. Een daarvan is het anterior foregut endoderm, een laag die tijdens de embryonale ontwikkeling normaal gesproken onderdelen van het ademhalings- en spijsverteringsstelsel vormt. Vanuit daar kunnen cellen, met de juiste chemische signalen, long-epitheliale voorlopercellen worden, die vroege longmarkers dragen en later kunnen rijpen tot gespecialiseerde luchtweg- of alveolaire cellen. Omdat toekomstige celtherapieën miljarden van deze cellen zullen vereisen, hebben onderzoekers manieren nodig om opbrengsten betrouwbaar te verhogen en protocollen aan verschillende patiëntcellijnen aan te passen zonder eindeloos proefondervindelijk werk in het laboratorium.
Een virtuele versie van celdifferentiatie bouwen
Het team breidde een eerder wiskundig raamwerk uit om wat, voor zover zij weten, het eerste populatieniveau-model van deze specifieke overgang van foregut endoderm naar longvoorlopers is te bouwen. Ze beschouwden twee manieren om de cellen te representeren: een eenvoudige versie die alleen het totale aantal levende cellen bijhoudt, en een meer gedetailleerde versie die het anterior foregut-celtype en de longvoorlopers afzonderlijk volgt. In beide gevallen volgt het model ook glucose en lactaat in het kweekmedium, als representanten van voedingsstoffen en afval. Met hulpmiddelen uit de systeembiologie stelden de onderzoekers veel kandidaatvergelijkingen op voor hoe cellen groeien, sterven en differentiëren, en gebruikten vervolgens identificeerbaarheidstests om modellen weg te strepen waarvan de parameters zelfs met perfecte data nooit bepaald konden worden.
Slimmere experimenten ontwerpen met het model
In plaats van louter de beschikbare data te passen, lieten de onderzoekers het model bepalen hoe nieuwe experimenten het beste uitgevoerd konden worden. Ze gebruikten gesimuleerde data om te onderzoeken hoe vaak ze celgetallen en voedingsniveaus moesten meten om modelparameters nauwkeurig te schatten, waarbij ze statistische precisie afwogen tegen de kosten en arbeid van frequente bemonstering. Dat leidde tot een praktisch plan: dagelijkse metingen voor glucose en lactaat, en celtelling elke één tot twee dagen, onder vier condities die varieerden in hoe rigoureus de kweek op dag 10 werd gesplitst en of het groeimedium dagelijks werd vernieuwd. Ze voerden deze experimenten vervolgens uit en maten zowel de totale celpopulatie als, via flowcytometrie, de fracties die foregut-cellen bleven of longvoorlopers waren geworden.
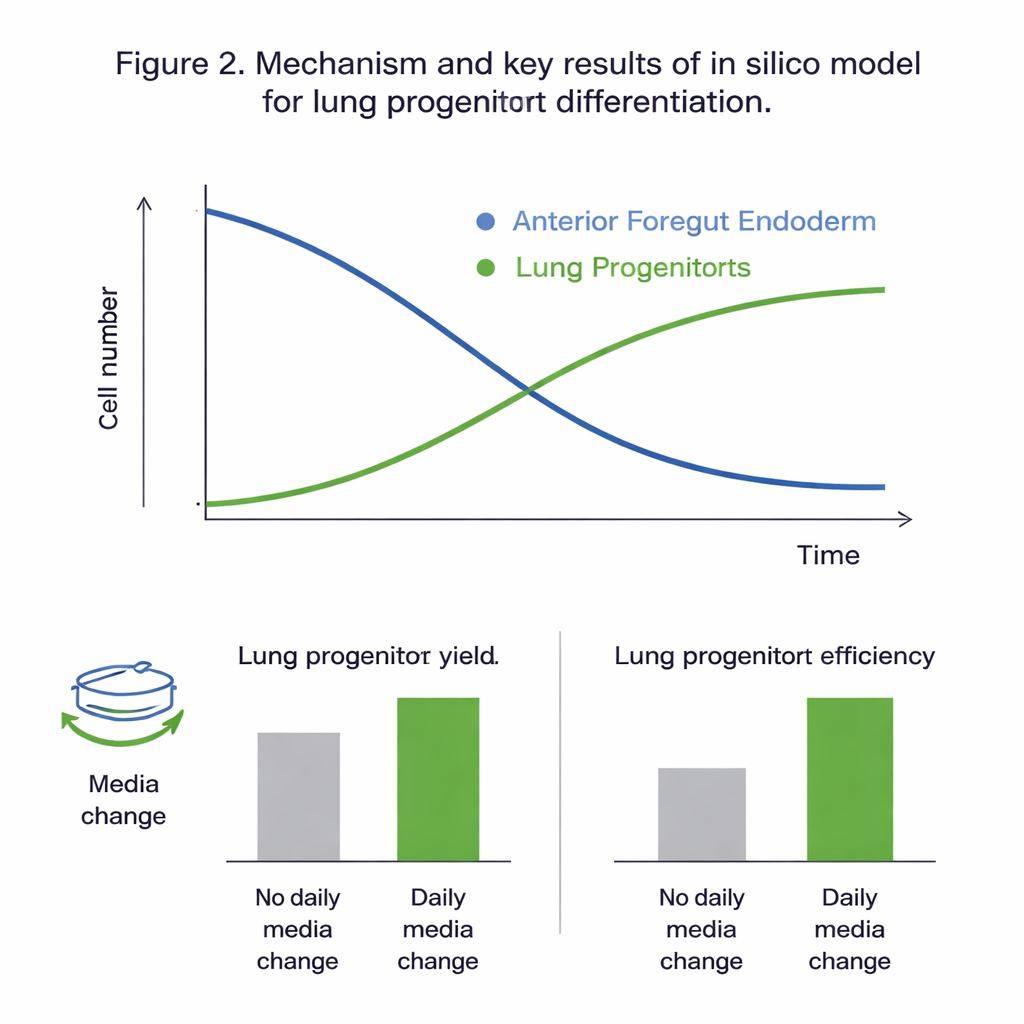
Wat de virtuele experimenten onthulden
Het passen van alle kandidaatmodellen op de experimentele data liet zien dat het tweetrapsmodel, dat foregut- en longvoorlopercellen apart volgt, betrouwbaar gekalibreerd kon worden en het waargenomen gedrag het beste vastlegde. Statistische controles gaven aan dat over het bestudeerde tijdvenster (dagen 11 tot 15 van het protocol) de dynamiek vooral werd gedreven door proliferatie en differentiatie van de foregut-cellen, terwijl de proliferatie van de longvoorlopers zelf weinig bijdroeg. Globale gevoeligheidsanalyse versterkte dit beeld en wees op groei-, sterfte- en differentiatiesnelheden van foregut-cellen—en de invloed van glucose—als de belangrijkste hefbomen die de uitkomst bepalen. Het gekalibreerde model reproduceerde niet-gebruikte data met fouten vergelijkbaar met de natuurlijke variabiliteit van de experimenten, wat suggereert dat het nauwkeurig genoeg was om ’wat-als’-scenario's in silico te verkennen.
Optimaliseren van mediumverversingen en splitsing
Met een betrouwbaar virtueel systeem testte het team hoe twee praktische protocolkeuzes de resultaten beïnvloeden: hoeveel de kweek wordt verdund (de split-ratio) op dag 10, en of het groeimedium iedere dag wordt vervangen. De simulaties voorspelden dat dagelijkse mediumverversing het aantal longvoorlopercellen en de opbrengst per startcel bijna verdubbelt, voornamelijk doordat nutrientuitputting en ophoping van afval en instabiele signaalmoleculen worden voorkomen. De experimenten kwamen goed overeen met deze voorspellingen. Het model suggereerde ook dat het gebruik van hogere split-ratio's—het meer uitdunnen van cellen op dag 10—de “opbrengst per inputcel” met ongeveer een kwart verbetert, ook al verlaagt het het absolute aantal cellen. In beide gevallen hadden deze aanpassingen weinig effect op de uiteindelijke proportie longvoorlopers binnen de kweek; ze veranderden vooral hoeveel cellen efficiënt geproduceerd konden worden.
Wat dit betekent voor toekomstige longtherapieën
Voor een niet‑specialist is de kernboodschap dat de auteurs een soort vluchtsimulator hebben gebouwd voor een kritische stap in het kweken van longcellen uit stamcellen. Door zorgvuldig ontworpen experimenten te combineren met rigoureuze wiskundige modellering laten ze zien hoe eenvoudige protocolkeuzes—zoals hoe vaak het kweekmedium wordt ververst en hoe dicht cellen worden uitgezet—dramatisch kunnen beïnvloeden hoeveel longbouwcellen worden geproduceerd, zonder de kwaliteit te veranderen. Dit type in silico-modellering kan toekomstige protocollen helpen stroomlijnen, experimenteel giswerk verminderen en uiteindelijk betrouwbaardere en schaalbaardere productie van longvoorlopers ondersteunen voor onderzoek, ziekte-modellering en op termijn regeneratieve therapieën.
Bronvermelding: Mostofinejad, A., Romero, D.A., Brinson, D. et al. In silico modeling of anterior foregut endoderm differentiation towards lung epithelial progenitors. npj Syst Biol Appl 12, 29 (2026). https://doi.org/10.1038/s41540-026-00650-1
Trefwoorden: longvoorlopercellen, geïnduceerde pluripotente stamcellen, in silico modellering, cel differentiatie, regeneratieve geneeskunde