Clear Sky Science · nl
Associatie tussen kopieaantalveranderingen en het immuun-transcriptomische landschap bij kanker
Waarom onze genen ertoe doen voor kankerimmunotherapie
Kankerimmunotherapie werkt door het immuunsysteem te helpen kankertumoren te herkennen en aan te vallen, maar slechts een minderheid van de patiënten profiteert langdurig. Deze studie stelt een fundamentele vraag met grote klinische gevolgen: hoe vormt de genetische chaos binnen tumorcellen – in het bijzonder grootschalige DNA-winst en -verlies, zogenoemde kopieaantalveranderingen – de immuunreactie tegen kanker, en kunnen we die effecten afleiden uit patronen van genexpressie?
Een panoramisch overzicht van kankergegevens
Om dit aan te pakken verzamelden de onderzoekers een enorme collectie van 294.159 genexpressieprofielen uit tumoren en andere weefsels. Deze profielen, afkomstig uit meerdere grote openbare databanken, leggen vast welke genen aan- of uitgezet zijn in duizenden monsters die vele kankertypes en experimentele condities bestrijken. In plaats van individuele genen één voor één te bekijken, gebruikte het team een wiskundige methode om elk profiel op te splitsen in onderliggende “componenten” – terugkerende groepen genen die samen stijgen en dalen en elk een biologisch proces weerspiegelen, zoals een immuunrespons of het effect van een DNA-verandering.
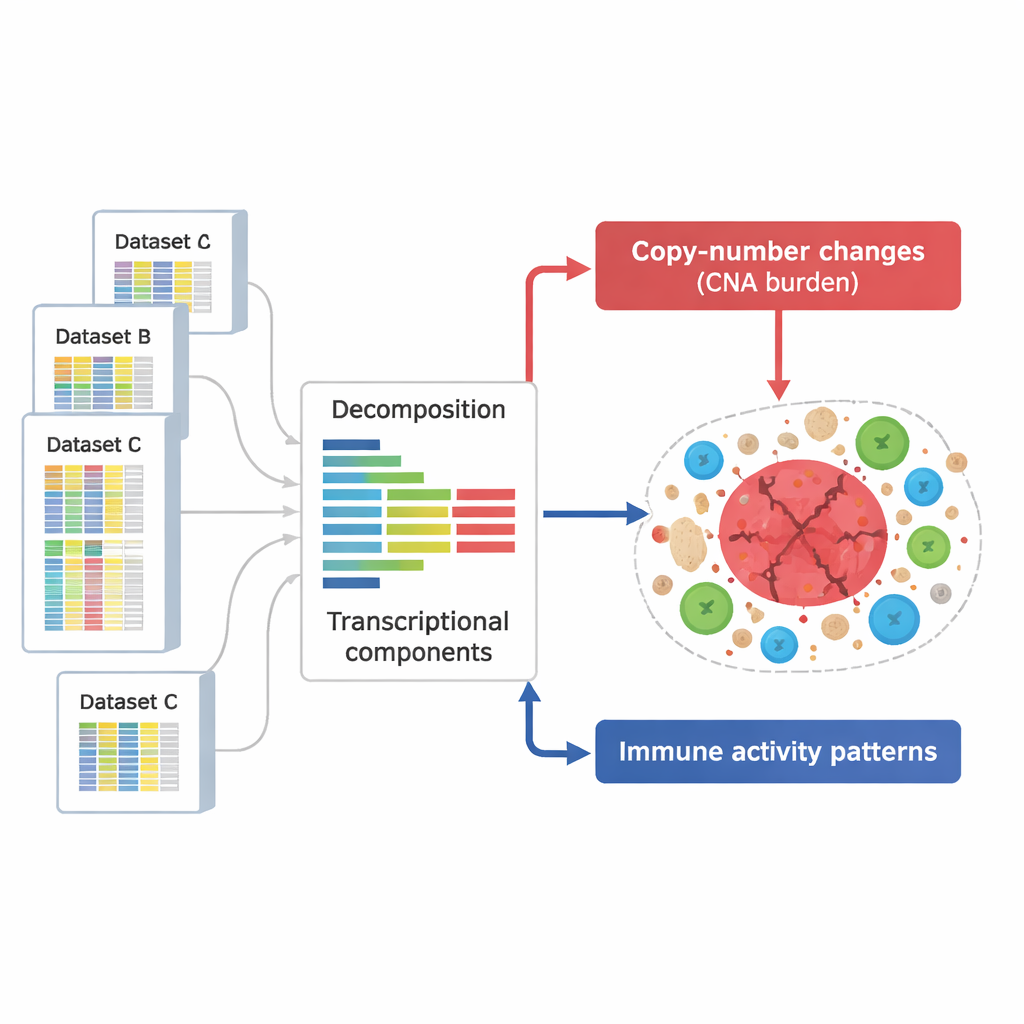
DNA-schade signalen scheiden van immuunsignalen
Uit deze componenten definieerden de wetenschappers twee sleutelgroepen. De ene groep ving de effecten van kopieaantalveranderingen op — chromosoomdelen die herhaaldelijk worden gewonnen of verloren in kankercellen. Deze patronen besloegen bijna het hele genoom, wat aangeeft dat de meeste regio’s die door zulke veranderingen zijn getroffen een detecteerbaar merkteken op genexpressie achterlieten. Een tweede groep componenten was verrijkt voor genen betrokken bij immuunfuncties, zoals T-celactivatie, natuurlijke-killer-celactiviteit en antigeenpresentatie. In totaal identificeerden ze 657 DNA-gerelateerde componenten en 283 immuungerelateerde componenten, waarvan veel reproduceerbaar waren in onafhankelijke datasets en technologieën, wat suggereert dat het robuuste, algemene kenmerken van tumorgeneeskunde zijn.
Patronen koppelen aan behandelrespons
Het team vroeg zich vervolgens af of deze immuungerelateerde patronen konden helpen voorspellen wie reageert op immuuncheckpointremmers, een belangrijke klasse van kankerimmunotherapiegeneesmiddelen. Met gegevens uit 13 klinische studies met in totaal 1.167 patiënten van zeven kankersoorten trainden ze computermodellen om respondenten te onderscheiden van niet-respondenten uitsluitend op basis van de activiteit van de immuuncomponenten in pretreatment tumormonsters. Sommige modellen presteerden sterk, ook wanneer ze werden getest op volledig onafhankelijke patiëntengroepen; bijvoorbeeld een model getraind op een borstkankercohort voorspelde responsen nauwkeurig in een apart borstkankercohort en liet nuttige prestaties zien in meerdere andere kankers. Een kleine set immuunpatronen, waaronder die gekoppeld aan interferonresponsen, natuurlijke-killer-cellen en T-celactivatie, droeg het sterkst bij aan deze voorspellingen.
Hoe genetische chaos de tumorimmuniteit hervormt
Met dit raamwerk brachten de onderzoekers systematisch de totale kopieaantalveranderingslast – een maat voor hoe uitgebreid het DNA van een tumor wordt gewonnen of verloren – in verband met de activiteit van elk immuunpatroon over vele kankertypes. De meeste immuunpatronen toonden een inverse relatie: tumoren met een hoge DNA-alteratielast hadden de neiging een lagere activiteit te vertonen van componenten die geassocieerd zijn met gunstige immuunfuncties, zoals antigeenpresentatie en infiltratie door sleutelimmuuncellen. Een opmerkelijke minderheid van patronen bewoog echter in de tegenovergestelde richting. Tumoren met een hoge alteratielast hadden vaak verhoogde signalen van immunosuppressieve celtypen, waaronder regulatorische T-cellen en bepaalde macrofagen, evenals van inflammatoire cellen die tumorgroei kunnen bevorderen in plaats van vernietiging. Ruimtelijke analyses van tumordoorsneden bevestigden dat gebieden met zware DNA-veranderingen vaak samenvielen met lage activiteit van behulpzame immuunpatronen en met “immuun-uitgesloten” zones waar immuuncellen beperkt bleven tot de randen van de tumor.
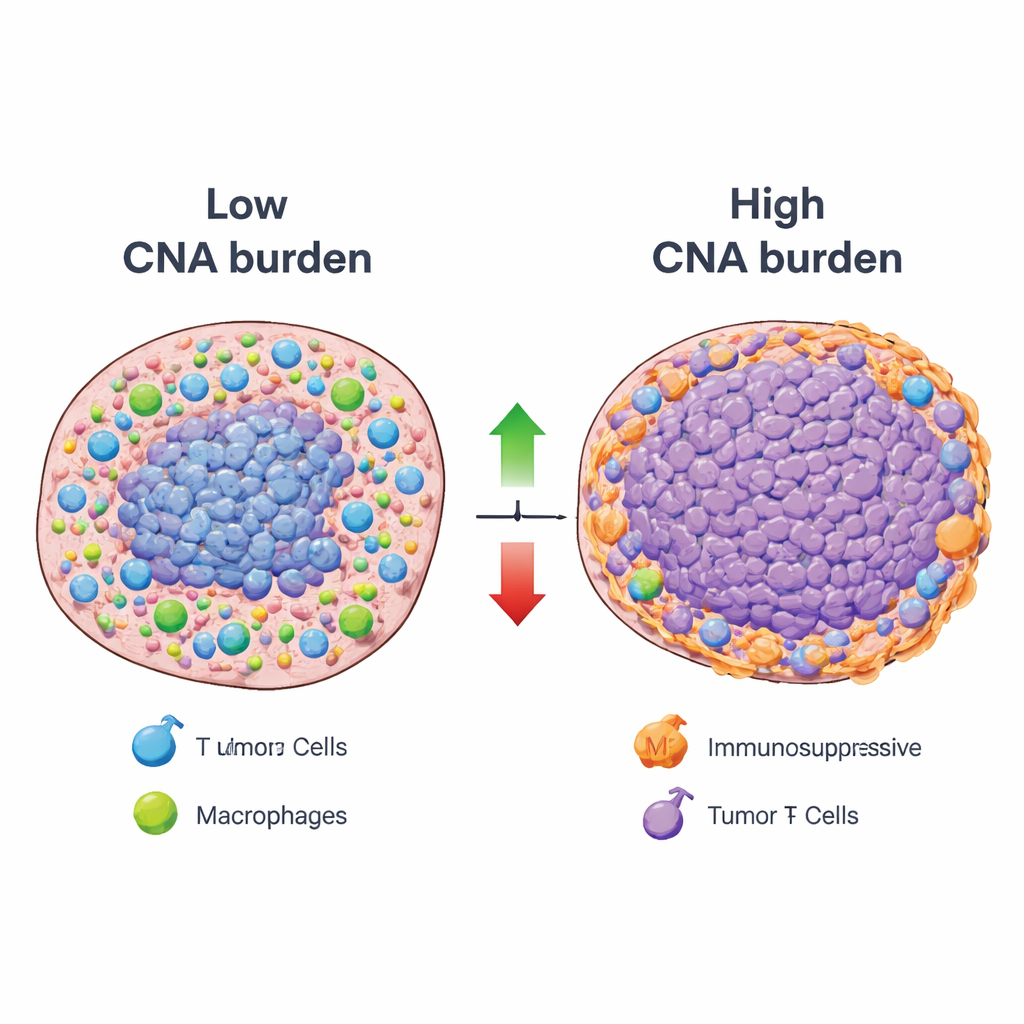
Wat dit betekent voor toekomstige kankerbehandeling
Simpel gezegd toont de studie aan dat tumoren die belast zijn met grootschalige DNA-winst en -verlies er zowel in slagen behulpzame immuunreacties te verzwakken als om remmende of tumorbevorderende immuunomgevingen te bevorderen. Toch zijn ze niet immuologisch stil; in plaats daarvan vertonen ze specifieke, terugkerende immuunstatussen die kwetsbaar kunnen zijn voor gerichte therapieën, zoals middelen die IL-17- of IL-23-signaaloverdracht blokkeren of strategieën die bepaalde macrofagen herprogrammeren. Door deze DNA–immuunrelaties doorheen kankers in kaart te brengen en de bron publiek beschikbaar te maken, biedt het werk een gedetailleerde gids voor waarom sommige genetisch instabiele tumoren weerstand bieden aan huidige immunotherapieën en suggereert het nieuwe combinatietherapieën om het immuunsysteem te helpen die weerstand te overwinnen.
Bronvermelding: Loipfinger, S., Bhattacharya, A., Urzúa-Traslaviña, C.G. et al. Association of copy number alterations with the immune transcriptomic landscape in cancer. npj Syst Biol Appl 12, 28 (2026). https://doi.org/10.1038/s41540-026-00649-8
Trefwoorden: kankerimmunotherapie, kopieaantalveranderingen, tumormicro-omgeving, immuuncheckpointremmers, transcriptomica